La cicatrisation des plaies

Pr. P. WAUTHY - La cicatrisation des plaies – Année académique 2012-2013 1/10
La cicatrisation des plaies
La cicatrisation des plaies est un processus complexe et évolutif qui comporte
l’ensemble des phénomènes physiologiques nécessaires à la réparation tissulaire. La
cicatrice en est son résultat final et souvent une préoccupation majeure de la part des
patients. La cicatrisation fait partie intégrante de la chirurgie : la possibilité de
guérison des tissus conditionne les résultats des traitements chirurgicaux. La
cicatrisation est fortement influencée par l’état de santé des patients. La
compréhension des mécanismes de base de celle-ci est fondamentale pour trouver les
solutions en vue d’aider l’organisme en difficulté à produire cette cicatrisation.
La cicatrisation concerne tous les tissus de l’organisme. Pour tous existent des principes
de base communs que nous allons évoquer dans ce chapitre. Pour des raisons de
commodité et de simplification, la cicatrisation dans ce chapitre sera généralement
considérée pour la peau mais bon nombre de notions fondamentales s’appliquant à cet
organe le plus développé de notre organisme, s’applique également aux autres tissus.
Il existe plusieurs causes de plaies au niveau de notre tissu cutané :
1. Les plaies traumatiques liées à l’effet d’un objet tranchant ou à une contusion
importante du tissu cutané menant à une rupture de son intégrité.
2. Les brûlures, qu’elles soient physiques par température ou chimiques par
réaction.
3. Les morsures et les piqûres d’animaux.
4. Des tensions excessives au niveau des tissus menant à une déchirure de ceux-ci.
Quelle que soit la cause de la plaie occasionnée, il est tout d’abord primordial d’éliminer
celle-ci avant toute chose en vue d’aider la cicatrisation. Le traumatisme occasionné,
quelle que soit son origine, peut parfois sembler mineur au regard des résultats. Cela
peut être lié à la présence d’un terrain favorisant le développement d’une plaie tel que :
Des troubles vasculaires
Une immunodéficience de l’organisme
La présence d’une malignité
Des affections du tissu conjonctif : maladie d'Ehlers-Danlos, de Marfan, …
Des maladies métaboliques telles que le diabète, des troubles thyroïdiens, …
Des troubles nutritionnels importants
Des causes iatrogènes (la prise de certains médicaments : corticostéroïdes,
cytostatiques, …)
La peau est un des organes les plus développés et en tout cas le plus développé en terme
de surface. Elle permet de remplir plusieurs rôles :

Pr. P. WAUTHY - La cicatrisation des plaies – Année académique 2012-2013 2/10
1. Elle est protectrice et imperméable pour assurer l’intégrité des tissus sous-
jacents.
2. C’est un organe excréteur de la sueur et du sébum.
3. C’est un organe tactile qui permet, grâce à la multitude de récepteurs qu’elle
contient, de déterminer la pression effectuée par des objets extérieurs,
l’intensité et l’importance en surface de celle-ci.
4. C’est un organe qui permet de réguler la température de l’organisme : d’une part
grâce à la sueur elle permet de réduire la température, mais également par
vasoconstriction et protection pileuse d’augmenter éventuellement la
température de l’organisme.
5. C’est un organe de stockage, en particulier des graisses vitales à notre apport
énergétique.
6. C’est un organe qui participe au métabolisme de plusieurs substances dont la
vitamine D.
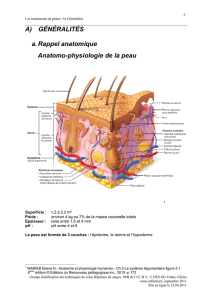
1. Architecture de la peau
La peau se compose typiquement de trois couches :
1. L’épiderme
2. Le derme
3. L’hypoderme
En fonction de sa localisation, l’épaisseur de la peau peut aller de 1 à 4 mm (elle sera fine
au niveau des paupières et épaisse au niveau du dos). C’est certainement l’organe le plus
développé du corps humain et qui y assure une fonction vitale ! La perte d’une quantité
significative de notre recouvrement cutané s’accompagne inéluctablement de notre
décès s’il ne peut être compensé.
a) L’épiderme
L’épiderme est avascularisé. Il est mince de 1/20
e
à 1/10
e
mm et est composé de
multiples couches cellulaires. Les couches cellulaires profondes ont un caractère vivant
alors que les plus superficielles, composées de cellules desquamantes, sont mortes.
L’épiderme est composé de quatre populations cellulaires distinctes : les kératinocytes,
les mélanocytes, les cellules de Langerhans et les cellules de Merkel. Si l’épiderme ne
contient aucun vaisseau, ni lymphatique, il renferme par contre bon nombre de
terminaisons nerveuses libres. Les kératinocytes évoluent au fil de leur migration de la
profondeur vers la superficie : la couche la plus profonde est la couche dite
« germinative ou basale », vient ensuite la couche « à épines ou épineuse » à laquelle
succède la couche « granuleuse » et enfin, la couche « cornée » qui finit par desquamer.
Le cycle des kératinocytes pour passer de la couche basale à la desquamation dure
approximativement un mois.

Pr. P. WAUTHY - La cicatrisation des plaies – Année académique 2012-2013 3/10
Les quatre populations cellulaires de l’épiderme assurent en tout trois fonctions
distinctes :
1. Une fonction de protection assurée par les kératinocytes sécrétant la kératine
ayant un rôle mécanique et imperméable, et les mélanocytes responsables de la
pigmentation de notre peau et protecteurs contre les rayonnements ultraviolets.
2. Un rôle sensoriel avec les cellules de Merkel ou cellules épithéloïdes.
3. Un rôle immunitaire avec les cellules de Langerhans ou cellules
macrophagocytiques. Ces cellules captent les antigènes amenés au contact de la
peau et activent le système immunitaire.
b) Le derme
Le derme est composé d’un tissu de conjonctif de soutien. Il est épais de 1 à 4 mm et
est hautement vascularisé et innervé. Il comporte entre autres des follicules pileux, des
glandes sébacées et des glandes sudoripares. La vascularisation du derme s’effectue de
la profondeur vers la superficie par :
1. Des plexus profonds se ramifiant progressivement au niveau des couches
superficielles de l’hypoderme.
2. Un plexus superficiel présent au sein même du derme dans ses couches
profondes.
3. Des boucles capillaires remontant jusqu’à la base de l’épiderme.
Pour ce qui est de l’innervation du derme, il est à signaler que celle-ci ne s’arrête pas à la
membrane basale et peut remonter jusque dans les couches de l’épiderme. Au niveau du
système nerveux, cinq types de récepteurs sont présents au niveau cutané :
1. Les corpuscules de Pacini qui figurent au niveau de l’hypoderme : ces corpuscules
nous aident à prendre conscience de l’existence d’une pression forte au niveau de
notre surface cutanée.
2. Au niveau des couches superficielles de l’hypoderme, figurent les corpuscules de
Ruffini, responsables de la perception à la chaleur.
3. Au niveau des couches profondes du derme, figurent les corpuscules de Krause,
responsables essentiellement de la perception du froid.
4. Au niveau du derme, figurent également les corpuscules de Golgi, responsables de
la perception des pressions légères.
5. Au niveau superficiel du derme, figurent les corpuscules de Meissner,
responsables de la perception du toucher.
Si ces cinq types de récepteurs nerveux nous aident à percevoir les pressions fortes ou
légères ainsi que les sensations de chaleur ou de froid, il est à noter que des
terminaisons nerveuses libres remontent jusqu’au niveau de l’épiderme pour nous aider à
prendre conscience de la douleur. Au niveau de l’épiderme toujours, des papilles dites de
Merkel nous aident à prendre conscience du toucher léger sur notre peau.

Pr. P. WAUTHY - La cicatrisation des plaies – Année académique 2012-2013 4/10
Pour ce qui est des poils et glandes du derme, les follicules pileux prennent leur origine
dans les couches superficielles de l’hypoderme et concernent toute l’épaisseur du
derme. Dans ce derme, figurent, avoisinant les follicules pileux, les glandes sébacées.
Pour ce qui est des glandes sudoripares, elles prennent origine dans la couche du derme
et remontent jusqu’en surface à l’aide de pores dits de transpiration. Au niveau de
l’hypoderme, figurent certaines structures musculaires dites muscles érecteurs du poil
qui aident s’ancrant aux follicules pileux à hérisser les poils.
Outre ce développement vasculaire, nerveux et de poils et de glandes, le derme est
composé de fibroblastes secrétant le collagène de type I et III, de macrophages et de
lymphocytes.
c) L’hypoderme
L’hypoderme est la couche la plus profonde de la peau et la plus épaisse. Elle est
composée de collagène et d’élastine qui retiennent le derme. Il s’agit de tissu conjonctif.
Il est composé également de cellules adipeuses : les adipocytes emmagasinant les
graisses et constituant dès lors une réserve énergétique considérable.
On peut considérer que de façon synthétique la peau assure quatre fonctions à notre
organisme :
1. Une fonction protectrice contre les blessures et les infections (un rôle de
barrière).
2. Une fonction de thermorégulation.
3. Une fonction d’équilibre hydrique.
4. Une fonction de synthèse de la vitamine D.
Le rôle protecteur de la peau s’étend aux agressions chimiques mais également
physiques.
2. La cicatrisation
La cicatrisation se déroule essentiellement en quatre phases élémentaires :
1. L’hémostase
2. La phase inflammatoire
3. La phase de granulation
4. La phase de remodelage
La phase d’hémostase intervient immédiatement après qu’il y ait eu agression de notre
système cutané et effraction de capillaires artériels et/ou veineux. Le sang s’écoulant
remplit un rôle de nettoyage de la plaie occasionnée. Ce rôle va s’arrêter lorsque
l’hémostase ainsi que la vasoconstriction des vaisseaux va se mettre en route pour
juguler les pertes sanguines. La phase inflammatoire, bien que se mettant
immédiatement en place après effraction de notre organe cutané, va culminer entre le
1
er
et le 4
e
jour post-agression.

Pr. P. WAUTHY - La cicatrisation des plaies – Année académique 2012-2013 5/10
La phase de granulation va culminer quant à elle du 4
e
au 21
e
jour post-agression et la
phase de remodelage va se mettre en route dès le 21
e
jour pour persister jusqu’à deux
ans après initiation du processus de cicatrisation.
a) L’hémostase
Le saignement aigu secondaire à une plaie cutanée va permettre de laver les tissus
effractés. Ce lavage permet d’une part d’évacuer un maximum de corps étrangers
amenés au sein de la peau et éventuellement d’évacuer certains produits chimiques
toxiques et/ou corrosifs. Va survenir dans un premier temps un spasme vasculaire
transitoire qui va avoir pour effet de juguler le saignement actif instauré. Ensuite, les
plaquettes et les facteurs de coagulation vont interagir notamment par dégranulation
plaquettaire qui libère une quantité d’adénosine diphosphate (ADP) qui induit une
adhésion interplaquettaire et entre les plaquettes et le collagène. L’activation de la
coagulation va également avoir pour effet de produire de la thrombine qui va induire la
formation de fibrine à partir du fibrinogène. Cette fibrine va renforcer la structure du
« caillot plaquettaire » pour mener au développement d’un clou hémostatique.
b) La phase inflammatoire
La phase inflammatoire a pour principal but de parfaire le nettoyage entamé par
l’hémorragie. La phase inflammatoire se caractérise par les quatre composantes
classiques de son développement, à savoir : l’apparition d’une chaleur localisée, d’une
rougeur, d’une tuméfaction et d’une douleur. La phase inflammatoire est médiée
essentiellement par deux grands facteurs.
Les facteurs cellulaires induits par les neutrophiles et les polymorphonucléaires. Cette
première phase de l’inflammation va créer une fuite de plasma du réseau intravasculaire
vers le réseau extravasculaire ainsi qu’une migration de cellules neutrophiles et de
polymorphonucléaires. Ensuite, va apparaître suite à cette première phase une activation
des mastocytes locaux.
Les deuxièmes facteurs identifiés sont des facteurs chimiotactiques. Plusieurs facteurs
vont être excrétés par les cellules mises en action lors de la phase inflammatoire :
EGF : facteur de croissance épidermique
FGF : facteur de croissance fibroblastique
TGFβ : facteur de croissance de transformation β
IL1 : interleukine 1
IL6 : interleukine 6
L’ensemble de ces facteurs va initier une réponse immunitaire qui va s’opposer à
l’agression instaurée. Elle va également mettre en place une néoangiogénèse qui aura
pour effet d’augmenter l’apport sanguin dans le site de la cicatrice multipliant par là-
même les réactions immunitaires instaurées.
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%