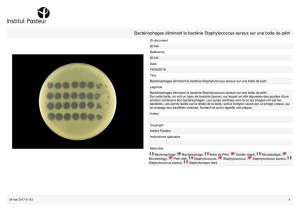
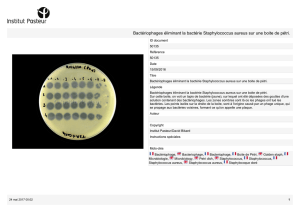
Ostéites du pied diabétique aspects fondamentaux. - Infectio

Ostéites du pied diabétique
aspects fondamentaux.
Dr F. Baudoux, Diabétologie, CHRU Lille

Microbiologie de l’ostéite
Domination constante S.aureus
Escherichia coli, Klebsiella pneumoniae et Proteus spp.
Pseudomonas aeruginosa.
Anaérobies: 5% des patients
Finegoldia magna
Peptococcus anaérobies.
Staphylocoques coagulase négative et Corynebacterium
sp.
ont été décrites comme pathogènes
Retrouvés dans 50% des cas
Wheat, L.J. et al. Diabetic foot infections. Bacteriologic analysis. Arch. Intern. Med 146, 1935-1940 (1986)
Armstrong, D.G., Lanthier, J., Lelievre, P. & Edelson, G.W. Methicillin-resistant coagulase-negative staphylococcal osteomyelitis and its relationship to broad-spectrum oral antibiosis
in a predominantly diabetic population. J Foot Ankle Surg 34, 563-566 (1995).
Senneville, E. et al. Culture of percutaneous bone biopsy specimens for diagnosis of diabetic foot osteomyelitis: concordance with ulcer swab cultures. Clin. Infect. Dis 42, 57-62 (2006).
Lavery, L.A., Sariaya, M., Ashry, H. & Harkless, L.B. Microbiology of osteomyelitis in diabetic foot infections. J Foot Ankle Surg 34, 61-64 (1995).
Newman, L.G. et al. Unsuspected osteomyelitis in diabetic foot ulcers. Diagnosis and monitoring by leukocyte scanning with indium in 111 oxyquinoline. JAMA 266, 1246-1251 (1991).

Technique de prélèvements
corrélation entre prélèvement
superficiel, ponction à l’aiguille fine et
biopsie osseuse est faible.
Biopsie osseuse
81% succès vs 50% après identification
des bactéries situées en superficie.
Armstrong, D.G., Lanthier, J., Lelievre, P. & Edelson, G.W. Methicillin-resistant coagulase-negative staphylococcal osteomyelitis and its relationship to broad-spectrum oral antibiosis
in a predominantly diabetic population. J Foot Ankle Surg 34, 563-566 (1995).
Senneville, E. et al. Outcome of diabetic foot osteomyelitis treated nonsurgically: a retrospective cohort study. Diabetes Care 31, 637-642 (2008).

Recommandations
Plaie
cliniquement infectée
OUI NON
Pas de prélèvement
Plaie superficielle Plaie profonde
Nettoyage
serum physiologique
Curetage/ecouvillonnage
Prélèvement et
conditionnement
Labo de
Bactériologie
Absence de
collection Collection
Aspiration
aiguille fine
Contact osseux
Débridement local
Serum stérile
Os liquéfié Os solide
BO possible BO impossible
Société de pathologie Infectieuse de langue française. Recommandations pour la pratique clinique. Prise en charge du pied diabétique infecté. Med Mal Infect 2077;37:26-50

Biofilms
Organisation bactérienne
Métabolisme ralenti
Adhérence
Résistance aux antibiotiques
Facteur d’échec thérapeutique
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
1
/
32
100%