Une observation d’occlusion coronaire aiguë C OBSERVATION

La Lettre du Cardiologue - n° 352 - février 2002
12
OBSERVATION
Il s’agit d’une femme de 88 ans, hospitalisée pour bilan d’un rétré-
cissement valvulaire aortique. La patiente présente depuis
quelques semaines une dyspnée d’effort d’intensité croissante.
L’auscultation révèle un souffle de rétrécissement aortique avec
abolition du deuxième bruit, l’ECG ne montre pas d’anomalie
de repolarisation.
Une échocardiographie doppler confirme un rétrécissement
aortique calcifié très serré, avec une surface valvulaire aortique
calculée à 0,5 cm2; le ventricule gauche est petit (diamètre dias-
tolique à 3,9 cm), tonique (pourcentage de raccourcissement
31 %), avec une épaisseur diastolique de la paroi libre à 0,8 cm
et du septum à 1,2 cm.
À titre systématique dans le cadre du bilan préopératoire, est réali-
sée une coronarographie au cours de laquelle la valve aortique est
franchie. Un gradient pic à pic de 50 mmHg est alors enregistré
avec une pression intraventriculaire gauche de 212/10-20 mmHg.
Une ventriculographie gauche est réalisée ; elle montre un ven-
tricule gauche tonique avec une fraction d’éjection à 73 % et un
volume ventriculaire diastolique indexé à la surface corporelle de
44 ml/m2. Cette ventriculographie est compliquée d’une effraction
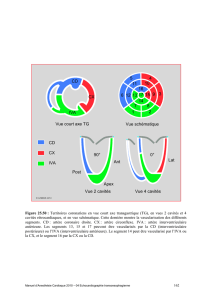
pariétale de contraste au niveau de la paroi antérieure (figure 1).
Environ 3 à 4 minutes après la ventriculographie, la patiente pré-
sente un malaise avec douleur thoracique et hypotension. Une
échographie cardiaque est immédiatement pratiquée, la parié-
tographie faisant craindre un hémopéricarde : l’échographie
montre l’absence d’épanchement péricardique mais révèle une
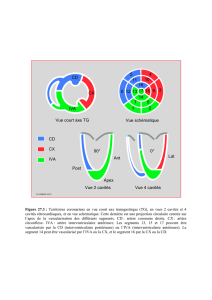
akinésie de la paroi antérieure. L’analyse de la ventriculographie
révèle que le produit de contraste dans la paroi se projette en
regard du trajet de l’artère IVA (figure 2).
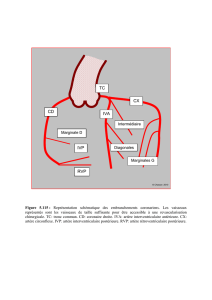
Une coronarographie est réalisée et montre une occlusion de
l’IVA moyenne juste au niveau de la pariétographie (figure 3).
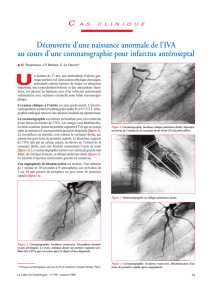
Une désobstruction de l’IVA est rapidement effectuée avec pas-
sage facile d’un guide dans l’IVA distale et rétablissement du flux
dès la pose d’un stent standard de 3 mm de diamètre et 15 mm
de longueur (stent Teneo Biotronix) (figure 4).
Dès la réouverture de l’artère, la douleur angineuse et le susdéca-
lage de ST qui étaient apparus disparaissent, et l’hémodynamique
cardiaque se normalise. La surveillance des marqueurs de
l’ischémie montre un pic d’élévation des CPK à 473 UI et de
troponine I à 12,8 U, sans modification persistante de l’ECG ou
anomalie de contraction à l’échographie cardiaque. L’interven-
tion chirurgicale sur la valve aortique a pu être réalisée un mois
plus tard (arrêt dans le délai habituel, après pose d’un stent, du
traitement par clopidogrel).
CAS CLINIQUE
Une observation d’occlusion coronaire aiguë
●G. Drobinski*
*Service de cardiologie, CHU Pitié-Salpêtrière, Paris.
Figure 1. Visualisation de la myographie.
Figure 2. Lors de la systole ventriculaire, on peut observer la myographie
en regard de l’opacification de l’IVA.

La Lettre du Cardiologue - n° 352 - février 2002
13
CAS CLINIQUE
DISCUSSION
Cette patiente a présenté une occlusion coronaire aiguë sur artère
saine, dont le mécanisme est certainement une compression de
l’artère IVA par un hématome dû à l’effraction de produit de
contraste dans la paroi ventriculaire gauche. Une blessure directe
de l’artère IVA par le jet ou par la pénétration dans la paroi de
l’extrémité de la sonde de ventriculographie (type pigtail 5F) est
également possible. D’autres mécanismes peuvent être discutés,
tels qu’une embolie coronaire ou une occlusion coronaire sur
lésion préexistante à l’occasion d’une baisse du débit cardiaque
à travers le rétrécissement aortique, mais ils ne sont pas expli-
qués par les données de l’observation. Les hématomes myocar-
diques compressifs sont certainement exceptionnels ; toutefois,
nous avons pu en observer deux autres cas, au niveau de l’IVA
après biopsie myocardique chez un greffé cardiaque et au niveau
de la circonflexe après cathétérisme du sinus coronaire pour une
tentative de fulguration d’une voie accessoire latérale gauche.
Chez le greffé cardiaque, la fréquence des blessures coronaires
lors des biopsies est attestée par celle des fistules, le plus souvent
entre l’IVA et la cavité du VD, évaluée à 5,4 % (1). Dans notre
série de 381 coronarographies chez des transplantés cardiaques,
une fistule entre l’IVA et le VD est observée dans 15 cas (3,94 %).
Ces blessures peuvent se compliquer d’ischémie et d’infarctus
du myocarde (2).
Une autre question soulevée par cette observation est l’inté-
rêt du cathétérisme ventriculaire gauche, compte tenu de la
précision des données de l’échographie doppler pour l’évalua-
tion de la sévérité de l’obstacle valvulaire. L’évaluation hémo-
dynamique de l’obstacle aortique reste justifiée en cas d’atteinte
plurivalvulaire ou lorsqu’il existe un doute sur la sévérité ou sur
la localisation valvulaire ou sous-valvulaire de l’obstacle. Elle
complète l’exploration des coronaires chez les patients qui pré-
sentent une suspicion légitime d’atteinte coronaire, nécessitant
une coronarographie préopératoire, ce qui est le cas chez notre
patiente de 88 ans. Le petit volume de la cavité du ventricule
gauche peut avoir favorisé le traumatisme de la paroi qui, par
chance, ne s’est pas compliqué d’hémopéricarde. Cet accident
doit être prévenu par le contrôle soigneux de la position de la
sonde dont le déplacement doit être libre, non gêné par les cor-
dages ou les trabéculations de l’endocarde ; en outre, un cathé-
térisme du ventricule gauche doit pouvoir être effectué en
confiance et sécurité chaque fois qu’il est jugé utile. ■
Bibliographie
1. Henzlova MJ, Nath H, Bucy RP, Bourge RC, Kirklin JK, Rogers WJ. Coronary
artery to right ventricle fistula in heart transplant recipients : a complication of
endomyocardial biopsy. J Am Coll Cardiol 1989 ; 14 : 258-61.
2.Wolf A, Rockson SG. Myocardial ischemia and infarction due to multiple coro-
nary-cameral fistulae : two case reports and review of the literature. Cathet
Cardiovasc Diagn 1998 ; 43 : 179-83.
Figure 3. Occlusion de l’IVA moyenne. Figure 4. Reperfusion de l’IVA après mise en place d’un stent.
1
/
2
100%