NOTICE Duvaxyn IE Plus T 1. NOM ET ADRESSE DU

Bijsluiter – FR versie Duvaxyn IE Plus T
NOTICE
Duvaxyn IE Plus T
1. NOM ET ADRESSE DU TITULAIRE DE L’AUTORISATION DE MISE SUR LE
MARCHÉ ET DU TITULAIRE DE L’AUTORISATION DE FABRICATION
RESPONSABLE DE LA LIBÉRATION DES LOTS, SI DIFFÉRENT
Titulaire de l’autorisation de mise sur le marché :
Eli Lilly Benelux
Division Elanco Animal Health
Markiesstraat 1
B-1000 Brussel
Fabricant responsable de la libération des lots :
Elanco Animal Health Ireland
Finisklin Industrial Estate
Sligo
Ireland
2. DÉNOMINATION DU MÉDICAMENT VÉTÉRINAIRE
Duvaxyn IE Plus T
3. LISTE DES SUBSTANCES ACTIVES ET AUTRES INGRÉDIENTS
Principes actifs:
Virus de la grippe, inactivé, souche A Equi/1 Prague H7N7 15 mcg HA
Virus de la grippe, inactivé, souche A Equi/2 Newmarket H3N8 15 mcg HA
Virus de la grippe, inactivé, souche A Equi/2 Suffolk H3N8 15 mcg HA
Anatoxine tétanique, purifiée 15 Lf
Chez les cobayes, 3 semaines après injection (n = 5) :
Virus de la grippe, inactivé, souche A Equi/1 Prague H7N7 ≥ 1 UR (*)
Virus de la grippe, inactivé, souche A Equi/2 Newmarket H3N8 ≥ 1 UR (*)
Virus de la grippe, inactivé, souche A Equi/2 Suffolk H3N8 ≥ 1 UR (*)
Anatoxine tétanique, purifiée ≥ 1 UR (**)
(*) unité relative définie par rapport à un vaccin de référence démontré efficace reposant sur une sérologie HRS chez le
cobaye vacciné
(**) unité relative définie par rapport à un vaccin de référence présentant une activité de 150 IU/ml reposant sur une sérologie
ELISA chez le cobaye vacciné
Adjuvants:
Hydroxyde d’aluminium 2,2 mg /dose
Carbomère 934 P 4 mg /dose
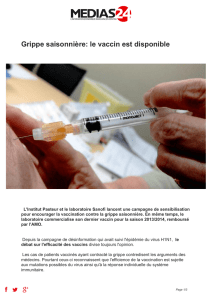
4. INDICATIONS
Immunisation active des chevaux et poneys à partir de l’âge de 5 mois afin de réduire les signes
cliniques et l’excrétion virale causés par le virus de la grippe équine type H7N7 et H3N8 (souches
européennes et américaines), comprenant les souches A/equi-2/South Africa/4/03 et A/equi-
2/Richmond/1/07 ; et immunisation active afin de prévenir la mortalité causée par le tétanos.
1

Bijsluiter – FR versie Duvaxyn IE Plus T
Pour la valence grippe équine, la mise en place de l’immunité a été démontrée par épreuve virulente
pour les souches South Africa 4/03, Richmond 1/07 et Sussex/89 et par des données sérologiques pour
les souches Prague/56, Newmarket 1/93 and Suffolk 89.
La durée d’immunité a été démontrée par épreuve virulente pour la souche Sussex/89 et par des
données sérologiques pour toutes les autres souches.
Mise en place de l’immunité : 2 semaines après administration de la deuxième dose
Durée d’immunité : 6 mois après l’administration de la deuxième dose
12 mois après l’administration de la troisième dose et des
rappels annuels.
5. CONTRE-INDICATIONS
Ne pas vacciner les animaux malade.
6. EFFETS INDÉSIRABLES
L’incidence des effets indésirables après les première et deuxième doses est faible. Après la troisième
dose et les doses suivantes, l’incidence des effets indésirables, particulièrement des réactions locales,
s’accroit.
Très fréquemment ces réactions comprennent des gonflements visibles de moins de 5 centimètres de
diamètre persistant jusqu’à 1 jour, ainsi qu’une hyperthermie pouvant persister jusqu’à 4 jours après
la vaccination. Les réactions locales les plus communes incluent des gonflements palpables
transitoires et des gonflements étendus, éventuellement douloureux, qui se résorbent en quelques
semaines, ainsi qu’un gonflement du cou visible pendant 2 à 4 jours après la vaccination. Dans de rare
cas, une formation d’abcès peut être observée. Aucune information concernant les caractéristiques
microscopiques des réactions au site d’injection n’est disponible.
Les réactions allergiques sont possibles après la vaccination. En cas de réactions allergiques, utiliser
un glucocorticoïde soluble par voie intraveineuse (par exemple du phosphate sodique de
dexaméthasone), de l’adrénaline par voie intramusculaire ou un antihistaminique par voie
intramusculaire.
Si vous constatez des effets indésirables graves ou d’autres effets ne figurant pas sur cette notice,
veuillez en informer votre vétérinaire.
7. ESPÈCES CIBLES
Chevaux et poneys
8. POSOLOGIE POUR CHAQUE ESPÈCE, VOIE ET MODE D’ADMINISTRATION
Une dose de 1,5 ml par animal par voie intramusculaire profonde.
Bien agiter avant utilisation.
Schéma vaccinal
* Primo-vaccination:
Une première dose de Duvaxyn IE Plus T doit être administrée à partir de l’âge de 5 mois, suivie
d’une deuxième dose de Duvaxyn IE Plus T à 4 à 6 semaines d’intervalle, et d’une troisième dose 6
mois plus tard.
La primo-vaccination des poulains nés de juments fortement immunisées contre le virus de la grippe
équine ou le tétanos (par exemple vaccines 2 fois ou plus par an ou durant le dernier trimestre de la
2

Bijsluiter – FR versie Duvaxyn IE Plus T
gestation) doit être retardée jusqu’à l’âge de 6 mois, étant donné que ces poulains peuvent présentés
des taux élevés d’anticorps d’origine maternelle contre le virus de la grippe équine ou contre
l’anatoxine tétanique qui peuvent interférer avec la prise vaccinale.
En cas de risque accru de grippe equine ou de tetanus chez les jeunes poulains, tout particulièrement
quand la prise colostrale a été inadéquate, une dose vaccinale supplémentaire peut être administrée à
partir de l’âge de 3 mois. Les titres en IgG doivent avoir été démontrés comme nuls ou faibles à l’aide
d’un outil de diagnostic adapté avant de procéder à une vaccination précoce. Un programme de
vaccination complet doit être réalisé par la suite à partir de l’âge de 5 mois.
* Vaccination de rappel:
Administrer une dose chaque année.
Il est recommandé qu’une dose unique de rappel soit administrée aux animaux qui ont déjà reçu un
programme de primo-vaccination complet à l’aide d’un vaccin contenant les mêmes types du virus de
la grippe équine. Un programme de primo-vaccination complet doit être envisagé pour les animaux
qui n’ont pas reçu une primo-vaccination appropriée.
9. CONSEILS POUR UNE ADMINISTRATION CORRECTE
Respecter les règles d’asepsie.
Éviter que le vaccin gèle ou soit exposé à la chaleur et/ou au soleil.
Les désinfectants peuvent rendre le vaccin inactif. Ne pas utiliser de matériel d’injection ayant subi
une stérilisation chimique.
10. TEMPS D’ATTENTE
Zéro jour
11. CONDITIONS PARTICULIÈRES DE CONSERVATION
Tenir hors de la vue et de la portée des enfants.
Conserver et transporter réfrigéré entre 2 °C et 8 °C
Protéger de la lumière
Ne pas utiliser après la date de péremption figurant sur l’emballage.
12. MISES EN GARDE PARTICULIÈRES
Précautions particulières pour chaque espèce cible
- Il est recommandé de vacciner tous les animaux présents en respectant le protocole vaccinal.
- La présence d'anticorps d'origine maternelle est susceptible d'interférer avec la prise vaccinale.
Veuillez-vous référer à la section Posologie et mode d’administration pour les recommandations de
vaccination en présence d’anticorps d’origine maternelle.
- Les animaux ayant reçu un sérum tétanique à la dose thérapeutique ne doivent pas être vaccines
durant un intervalle d’au moins 4 semaines après le traitement avec le sérum.
- Dans toute population animale, il peut y avoir un petit nombre d’animaux qui ne répondent pas
correctement à la vaccination.
Précautions particulières d’utilisation chez l’animal
Eviter tout stress chez les animaux avant, pendant et après la vaccination.
Précautions particulières à prendre par la personne qui administre le médicament aux animaux
En cas d’auto-administration, d’ingestion ou de contact cutané accidentel(le), demandez
immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquetage.
3

Bijsluiter – FR versie Duvaxyn IE Plus T
Utilisation en cas de gravidité, de lactation ou de ponte
Peut être utilisé pendant la gestation.
Interactions médicamenteuses ou autres formes d’interactions
Aucune information n'est disponible sur l'innocuité et l'efficacité de l'association de ce vaccin avec un
autre médicament vétérinaire. En conséquence, la décision d'utiliser ce vaccin avant ou après un autre
médicament vétérinaire doit être prise au cas par cas.
Surdosage (symptômes, conduite d’urgence, antidotes)
Aucun effet indésirable autre que ceux mentionnés à section « Effets indésirables » n'a été constaté
après administration d'une double dose de vaccin.
Incompatibilités
Ne pas mélanger avec un autre vaccin ou un autre produit immunologique.
13. PRÉCAUTIONS PARTICULIÈRES POUR L’ÉLIMINATION DES MÉDICAMENTS
VÉTÉRINAIRES NON UTILISÉS OU DES DECHETS DÉRIVÉS DE CES
MÉDICAMENTS, LE CAS ÉCHÉANT
Les médicaments vétérinaires non utilisés ou les déchets dérivés de ces médicaments doivent être
éliminés conformément aux exigences locales.
14. DATE DE LA DERNIERE NOTICE APPROUVEE
Octobre 2014
15. INFORMATIONS SUPPLEMENTAIRES
À délivrer sur ordonnance vétérinaire
BE-V171911
4
1
/
4
100%