Lire l'article complet

La Lettre du Cardiologue - n° 290 - mars 1998
18
DOSSIER
a fréquence de l’endocardite infectieuse a significati-
vement augmenté au cours des deux dernières décen-
nies (1). Celle-ci représente la troisième cause d’insuf-
fisance mitrale, derrière les valvulopathies dégénérative et
rhumatismale (ces dernières étant en net recul).
L’échocardiographie permet désormais de reconnaître les endo-
cardites infectieuses mitrales débutantes. Les indications opéra-
toires reposent sur l’analyse échographique de la valve effectuée
au mieux par voie transœsophagienne.
Cet examen permet de visualiser des lésions spécifiques affirmant
le diagnostic, et procure des renseignements pronostiques essen-
tiels : retentissement de l’infection sur la fonction valvulaire, éva-
luation du risque embolique.
Les progrès de l’échocardiographie associés aux nouvelles pos-
sibilités offertes par la chirurgie conservatrice mitrale ont consi-
dérablement modifié la stratégie thérapeutique au cours de l’en-
docardite mitrale.
L’indication opératoire, classiquement tardive après une longue
période d’évolution sous antibiothérapie, est actuellement posée
précocement, souvent dans la semaine qui suit le diagnostic.
L’INSUFFISANCE MITRALE
L’infection débute au niveau de l’endocarde des feuillets mitraux.
Un abcès valvulaire se constitue, se manifestant par une infiltra-
tion œdémateuse évoluant vers la collection, puis la rupture.
Selon sa localisation, la rupture d’un abcès entraîne une mutila-
tion valvulaire lorsque celui-ci intéresse le bord libre, ou bien une
perforation si l’abcès siège au niveau du corps d’un feuillet, ou
encore des ruptures de cordages lorsque l’endocarde de ces der-
niers est intéressé. L’infection siège avec prédilection dans les
régions commissurales (en particulier la commissure interne), et
l’endocardite mitrale est l’étiologie la plus fréquente de prolap-
sus commissural.
Les ruptures de cordages habituellement localisées sur le feuillet
postérieur au cours des affections dégénératives atteignent avec
une égale fréquence le feuillet antérieur, les commissures ou le
feuillet postérieur au cours de l’endocardite aiguë.
Les abcès de l’anneau se rencontrent moins fréquemment en posi-
tion mitrale qu’en position aortique (2). Ils siègent habituelle-
ment au niveau des portions postérieure et interne de l’orifice. Ils
surviennent souvent au sein de calcifications annulaires témoi-
gnant d’une maladie dégénérative préexistante ou au contact de
la collerette de suture en cas d’endocardite sur prothèse.
Chirurgie précoce au cours de l’endocardite infectieuse
mitrale
●
Dr Ch. Acar
* Chirurgie cardiovasculaire, Hôpital Bichat, 46, rue Henri-Huchard, 75018
Paris.
■Les indications opératoires au cours de l'endocardite
infectieuse mitrale ont été transformées par les progrès de
l'échocardiographie et les nouvelles possibilités offertes par
la chirurgie reconstructrice.
■Dans la majorité des cas, il apparaît licite de proposer un
geste chirurgical avant la survenue de complications neuro-
logiques ou l'évolution vers le choc septique.
■Lorsque l'intervention est réalisée précocement, une plas-
tie mitrale sera possible dans 80 % des cas.
Mots-clés : Végétation – Endocardite – Plastie mitrale.
POINTS FORTS
POINTS FORTS
L
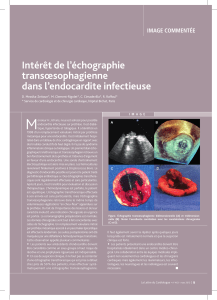
Figure 1. Fréquence des lésions observées au cours de l’endocardite
infectieuse mitrale.
Dossier - Chirurgie - C.A. 6/05/04 16:59 Page 18

La Lettre du Cardiologue - n° 290 - mars 1998
19
La valve mitrale peut être atteinte secondairement au cours de
l’évolution d’une endocardite aortique. Les lésions retrouvées
sont habituellement un abcès de l’anneau aortique étendu à la
jonction aorto-mitrale ou bien un abcès perforé du feuillet anté-
rieur au contact du jet régurgitant de fuite aortique.
La figure 1 (voir page 00) résume la fréquence des lésions au
cours de l’endocardite mitrale aiguë. On peut noter que la clas-
sique perforation valvulaire n’est pas la lésion dominante. La fuite
mitrale est beaucoup plus souvent en rapport avec un prolapsus
par rupture de cordages (3).
Dans un tiers des cas, on retrouve une lésion valvulaire préexis-
tante (4), le cas le plus fréquent étant une valvulopathie mitrale
dégénérative. Au cours de la maladie de Barlow, l’existence d’un
épaississement myxoïde important des feuillets semble être un
facteur de risque prédisposant pour la survenue d’une endocar-
dite (5). La présence de calcifications annulaires constitue éga-
lement un point d’appel à l’infection.
Plus rarement, l’endocardite infectieuse complique l’évolution
d’une maladie mitrale rhumatismale, avec une prédilection pour
les formes fuyantes plutôt que pour les formes sténosantes (4)
(figure 2).
Exceptionnellement, il s’agit d’une valvulopathie mitrale congé-
nitale de type canal atrioventriculaire (6).
Enfin, la lésion préexistante peut elle-même être d’origine infec-
tieuse. Le risque d’endocardite est, en effet, beaucoup plus élevé
chez les patients ayant déjà été sujets à un premier épisode infec-
tieux (1). Ce facteur doit être pris en considération lors du choix
de la technique opératoire, qui doit offrir le risque le plus faible
possible de récidive infectieuse.
LES VÉGÉTATIONS
Les végétations sont constituées de fibrine contenant des leuco-
cytes et des germes, et sont habituellement appendues sur le ver-
sant auriculaire des feuillets mitraux. Elles peuvent avoir un aspect
variable : mobiles et pédiculées (figure 2) ou, au contraire, adhé-
rentes à la surface valvulaire.
Le site d’insertion des végétations est toujours le siège d’un abcès
valvulaire plus ou moins étendu. La paroi de l’oreillette gauche
peut être recouverte de granulations septiques au contact du jet
d’insuffisance mitrale (7).
La consistance et la coloration des végétations varient selon leur
âge : friables et rougeâtres la première semaine, pendant laquelle
le risque embolique est le plus élevé, elles involuent progressi-
vement, devenant plus fermes et jaunâtres avec le temps.
Le risque embolique des végétations est plus élevé s’il s’agit de
formation fraîche plutôt que de végétations anciennes en voie
d’organisation. Le caractère pédiculé favorise également les
migrations, de même que le site d’implantation des végétations
sur un élément mobile des feuillets près des bords libres, qui sont
exposés à d’importantes accélérations de flux au cours du cycle
cardiaque (1).
Enfin, les dimensions de la végétation constituent à elles seules
un élément pronostique ; le seuil de 10 mm doit être considéré
comme associé à un fort risque embolique (25 % des patients pré-
sentent une embolie dans les 10 jours qui suivent le diagnostic et
75 % dans le mois suivant) (1, 8).
Ainsi, l’appréciation par échographie de la taille des végétations
de même que leur site d’implantation et leur caractère mobile
constituent des éléments pronostiques essentiels, permettant de
poser l’indication de chirurgie précoce.
LES EMBOLIES SYSTÉMIQUES
Les embolies cérébrales constituent la complication embolique
majeure des végétations. Elles sont plus fréquentes lorsque l’in-
fection est située sur la valve mitrale plutôt que sur la valve aor-
tique.
Globalement, environ un tiers des patients sont sujets à des com-
plications neurologiques au cours de l’évolution d’une endocar-
dite (1, 9).
Les complications cérébrales surviennent habituellement préco-
cement dans les deux semaines suivant le début de l’infection, en
cas de germe virulent (staphylocoque doré), et plus tardivement
en présence d’un streptocoque. En présence de complications
neurologiques et malgré le traitement, la mortalité de l’endocar-
dite infectieuse s’élève à 40 % (9). Par ailleurs, lorsqu’une inter-
vention chirurgicale est nécessaire, l’œdème cérébral induit par
la circulation extracorporelle risque de détériorer la situation neu-
rologique (9).
Les lésions cérébrales sont de trois types : infarctus cérébral,
hémorragie secondaire à une rupture d’anévrysme mycotique ou
abcès.
En pratique, toutes ces lésions sont la conséquence immédiate ou
secondaire de la migration de végétations. C’est dire l’impor-
tance de la prévention des embolies par la chirurgie à un stade
précoce. Celle-ci élimine complètement le risque de nouvelle
complication cérébrale.
Les artères des membres dont le diamètre est plus important sont
rarement le siège d’embolie dans le cadre des endocardites. Les
embolies des artères coronaires sont exceptionnelles au cours de
l’endocardite mitrale.
Les organes les plus fréquemment atteints par les migrations de
végétations sont la rate et les reins (respectivement 44 et 56 %
dans les séries autopsiques) (7). Ces embolies n’entraînent que
rarement une symptomatologie clinique sous la forme d’un infarc-
tus ou d’un abcès.
Figure 2. Endocardite sur valvulopathie rhumatismale avec végétations.
Dossier - Chirurgie - C.A. 6/05/04 16:59 Page 19

La Lettre du Cardiologue - n° 290 - mars 1998
20
DOSSIER
Leur diagnostic peut être affirmé par le scanner abdominal, dont
la pratique doit être systématique au cours du bilan des endocar-
dites infectieuses (figure 3).
L’ENDOCARDITE SUR PROTHÈSE MITRALE
L’endocardite sur prothèse survient avec une égale fréquence
après remplacement valvulaire aortique ou mitral et son incidence
atteint 3 % au cours de la première année postopératoire (10).
Au cours de la première année, les patients opérés initialement
pour endocardite aiguë présentent un risque d’endocardite sur
prothèse dix fois plus élevé que les patients opérés dans un autre
contexte. Les années suivantes, ce risque diminue mais reste net-
tement supérieur à celui d’une population standard de remplace-
ment valvulaire (11).
Le type de prothèse valvulaire (mécanique ou bioprothèse) ne
semble pas clairement influencer le risque d’endocardite sur pro-
thèse. Certains auteurs ont toutefois noté une incidence plus éle-
vée de cette complication en présence de bioprothèse, dont la fixa-
tion au glutaraldéhyde favoriserait la colonisation bactérienne (11).
L’endocardite sur prothèse est un processus rapidement destruc-
teur. L’infection affecte avec prédilection la collerette de suture
de la prothèse ; il en résulte une désinsertion. Puis la contamina-
tion s’étend aux tissus adjacents, provoquant des abcès annulaires
parfois circonférentiels.
La fréquence des abcès de l’anneau atteint 60 % au cours des
endocardites sur prothèse (10). Les végétations recouvrent la col-
lerette et les éléments mobiles de la valve et, surtout en position
mitrale, peuvent entraîner un tableau d’obstruction de prothèse
(figure 4).
Les germes habituellement responsables sont les staphylocoques
dorés ou les champignons. Si l’échographie permet avec préci-
sion d’évaluer la fonction valvulaire (existence d’un élément obs-
tructif ou d’une désinsertion prothétique), elle est moins précise
dans l’évaluation de l’étendue des lésions infectieuses (abcès
annulaire, végétation).
En effet, l’examen échographique est rendu difficile par les cones
d’ombre induits par la prothèse.
Le risque de désinsertion itérative est particulièrement élevé
compte tenu de la fragilité des tissus environnant la prothèse :
20 % des patients environ seront soumis à une troisième inter-
vention pour déhiscence périprothétique (1).
L’HEURE DE LA CHIRURGIE
Les indications opératoires dépendent du contexte clinique et du
bilan échographique de la valve.
Concernant les indications hémodynamiques, la survenue d’un
œdème pulmonaire difficile à traiter médicalement constitue, à
l’évidence, une indication chirurgicale rapide au cours de l’endo-
cardite mitrale. Cependant, l’existence d’une fuite mitrale volu-
mineuse, même bien tolérée cliniquement, constitue également une
indication opératoire. Lorsque la chirurgie est réalisée à un stade
précoce après quelques jours d’antibiothérapie, une plastie sera
possible dans la grande majorité des cas et les complications évo-
lutives de l’endocardite seront complètement éliminées (12, 13).
En l’absence de fuite importante, l’indication opératoire, classi-
quement posée devant une embolie dans un territoire "majeur"
ou plusieurs embolies dans un territoire “mineur”, doit aujour-
d’hui être portée à un stade plus précoce. Elle repose aujourd’hui
sur l’évaluation du risque embolique par l’échocardiographie.
Il semble logique de ne pas attendre les complications emboliques
qui risquent de laisser des séquelles définitives ou de menacer le
pronostic vital. La présence d’une volumineuse végétation
(> 10 mm) pediculée, développée aux dépens d’un segment
mobile de la valve mitrale (proche du bord libre des feuillets),
doit faire envisager un geste chirurgical rapide (1, 2). L’indica-
tion opératoire sera impérative si le scanner abdominal révèle
l’existence d’embolies spléniques ou rénales.
Lorsque malheureusement le diagnostic est posé devant la sur-
venue de signes neurologiques, deux situations sont possibles :
– Si les signes cliniques ont régressé (amaurose, hémianopsie
latérale homonyme, hémiparésie), une intervention urgente s’im-
pose afin de prévenir de nouvelles embolies (1, 2) (figure 5, voir
page 00).
– À l’inverse, s’il existe un déficit neurologique massif (hémi-
plégie), a fortiori des troubles de la conscience, il convient de sur-
seoir à l’intervention, car la circulation extracorporelle risque
Figure 3. Infarctus rénal secondaire à une migration de végétation.
Figure 4. Endocardite sur prothèse de Starr mitrale. Noter les végéta-
tions sur la collerette et sur les éléments mobiles de la valve entraînant
une obstruction de prothèse.
Dossier - Chirurgie - C.A. 6/05/04 16:59 Page 20

La Lettre du Cardiologue - n° 290 - mars 1998
21
d’aggraver la symptomatologie neurologique. Le pronostic est
désormais lié à la réversibilité des lésions neurologiques plutôt
qu’au traitement de l’endocardite.
Les indications bactériologiques (persistance de l’état septique)
sont les plus difficiles, car témoignant habituellement d’une endo-
cardite évoluée. La chirurgie ne permet qu’inconstamment de res-
taurer l’état hémodynamique, car il existe fréquemment des loca-
lisations infectieuses secondaires (cerveau, embolie périphérique)
et il n’est pas rare de voir évoluer le choc septique malgré l’éra-
dication du foyer infectieux valvulaire. La mortalité opératoire
dans ce contexte est très élevée.
La présence de germes virulents (staphylocoque, champignons)
doit ainsi inciter à une intervention chirurgicale précoce avant la
survenue du choc septique, qui est relativement imprévisible (1).
Enfin, le diagnostic d’endocardite sur prothèse mitrale doit faire
envisager une intervention rapide. La mortalité opératoire, dans
ce contexte, atteint 40 à 75 % selon les séries. Seule une chirur-
gie précoce avant la constitution d’abcès annulaires circonféren-
tiels permettra de réduire ce risque (10, 11).
LA TECHNIQUE OPÉRATOIRE
L’intervention est réalisée sous circulation extracorporelle et la
protection du myocarde est assurée par une cardioplégie froide.
Il convient d’effectuer, dans un premier temps, une ablation com-
plète des tissus infectés. Ainsi, les portions de feuillet et les cor-
dages atteints par les abcès valvulaires ou recouverts de végéta-
tions doivent être totalement excisés afin d’obtenir une
stérilisation parfaite de la valve. S’il existe un abcès de l’anneau,
celui-ci doit être détergé. En fonction de l’étendue de la résec-
tion nécessaire, la stratégie opératoire s’orientera soit vers une
plastie, soit vers un remplacement valvulaire.
Plastie
En présence d’une rupture de cordages sur le feuillet postérieur,
une résection quadrangulaire de la zone prolabée est effectuée.
Les ruptures de cordages du feuillet antérieur sont traitées par
transposition de cordages.
Les perforations valvulaires nécessitent toujours, à la phase aiguë,
un débridement important, car elles surviennent au sein d’un
abcès. Elles sont fermées à l’aide d’un patch de péricarde auto-
logue préalablement fixé dans un bain de glutaraldéhyde. Une
alternative au patch de péricarde consiste à utiliser un segment
de feuillet antérieur mitral obtenu à partir d’une homogreffe cryo-
préservée.
La mise en place d’un anneau prothétique au cours de la phase
aiguë de l’endocardite a été longtemps controversée. L’anneau
mitral n’est habituellement pas dilaté si l’endocardite survient sur
une valve native normale.
Toutefois, l’annuloplastie confère une plus grande fiabilité à la
plastie : renforcement des sutures effectuées sur le feuillet pos-
térieur, augmentation de la surface de coaptation entre les
feuillets.
Le type d’annuloplastie ne semble pas déterminant : il pourra
s’agir d’un anneau flexible (Duran) ou d’un anneau rigide (Car-
pentier).
L’utilisation d’annuloplastie préparée à l’aide de péricarde auto-
logue permet d’éliminer complètement l’introduction de maté-
riel prothétique et pourrait, dans le futur, constituer un matériau
intéressant.
Lorsque les lésions sont étendues à un tiers de la valve environ,
affectant à la fois les feuillets et les cordages, une plastie conven-
tionnelle n’est pas techniquement réalisable.
Dans ces conditions, après la phase de débridement, il est pos-
sible d’envisager la reconstruction de la valve à l’aide d’un seg-
ment d’homogreffe mitrale. L’utilisation d’homogreffe partielle
est particulièrement utile dans le cadre de l’endocardite car les
lésions prédominent habituellement dans les régions commissu-
rales et sur les feuillets adjacents qui dépendent d’un même pilier
mitral (figure 6). Le remplacement sélectif d’une portion de la
valve par une homogreffe partielle avec ses cordages et son chef
de pilier permet de réaliser une chirurgie reconstructrice en pré-
sence de lésions atteignant jusqu’à la moitié de l’appareil mitral
(remplacement d’une hémi-valve) (figures 6a, b, c, d).
Remplacement valvulaire
Lorsque l’ensemble de la valve est intéressé par l’endocardite, un
remplacement valvulaire doit être effectué. Le choix du substitut
valvulaire tiendra compte de l’âge du patient et des possibilités
d’anticoagulation. Il n’existe pas d’argument formel pour utili-
ser une prothèse mécanique plutôt qu’une bioprothèse.
Dans les deux cas, il existe un risque d’endocardite récurrente et
de désinsertion conduisant à des interventions itératives (10, 11).
De nombreuses études ont montré la supériorité des homogreffes
au cours de l’endocardite aiguë aortique (14, 15). L’utilisation
d’homogreffe réduit considérablement le risque d’infection réci-
divante précoce, qui est maximal au cours de la première année.
La récidive d’endocardite est ainsi 3 à 6 fois moins fréquente si
une homogreffe est implantée plutôt qu’une prothèse (14, 15).
Les homogreffes constituent ainsi un substitut valvulaire résis-
Figure 5. Survie en présence de complications neurologiques, d’après
Hortskotte et coll. (1). La chirurgie tardive (8 à 40 jours) procure des
résultats identiques au traitement médical seul. La chirurgie précoce
(< 8 jours) améliore le pronostic.
Dossier - Chirurgie - C.A. 6/05/04 16:59 Page 21

La Lettre du Cardiologue - n° 290 - mars 1998
22
DOSSIER
tant à l’infection et il semble logique d’étendre leur utilisation à
l’endocardite mitrale (16). Elles présentent l’avantage d’être
dépourvues de collerette synthétique et de réduire l’introduction
de matériel prothétique en milieu septique.
LES RÉSULTATS
Sur une période de 5 ans, 78 patients ont été opérés précocement
dans le cadre d’une endocardite infectieuse mitrale. L’interven-
tion a été réalisée en moyenne 8 jours après le diagnostic et le
début de l’antibiothérapie et, dans la plupart des cas, au cours de
la première semaine.
Les indications opératoires ont été les suivantes : fuite mitrale
volumineuse associée ou non à une instabilité hémodynamique
répondant mal au traitement médical (59 %), fièvre ou hémocul-
ture positive malgré l’antibiothérapie (11 % des cas), volumi-
neuse végétation mobile reconnue à l’échographie (30 % des cas)
ayant ou non été responsable d’embolie systémique.
Le germe responsable de l’endocardite a été retrouvé dans 92 %
des cas.
L’agent responsable a été respectivement : streptocoque (48 %),
staphylocoque (31 %), bacille à Gram négatif (13 %), champi-
gnons (5 %), autres (3 %).
La technique opératoire a été adaptée en fonction de l’étendue
des lésions : plastie mitrale (51 cas), homogreffe partielle (14 cas),
homogreffe totale (7 cas), prothèse (6 cas). Dans 5 cas, l’endo-
cardite affectait également l’orifice aortique nécessitant un rem-
placement valvulaire (prothèse mécanique n = 3, homogreffe
n = 2). Cinq patients sont décédés au cours de la première année
postopératoire. Dans tous les cas, il s’agissait de complications
infectieuses : choc septique persistant, évolution d’une compli-
cation neurologique.
À distance (suivi moyen à 2 ans), une récidive de l’endocardite
a été notée dans 7 cas (dont 2 endocardites sur prothèse). En cas
de plastie, l’infection intéressait préférentiellement l’anneau pro-
thétique, et ces patients ont été traités soit par une simple abla-
tion de l’anneau, soit par la mise en place d’une homogreffe
mitrale. Un patient qui présentait une récidive d’endocardite loca-
lisée à l’anneau a été traité médicalement avec succès.
Un patient est décédé au décours d’une réintervention pour endo-
cardite sur prothèse mitrale. Un patient a été réopéré à distance
pour sténose sur plastie mitrale. Les 55 autres patients sont en
classe fonctionnelle I ou II. La plupart ne suivent aucun traite-
ment hormis la prévention occasionnelle d’une récidive d’endo-
cardite. L’échographie de contrôle a mis en évidence un fonc-
tionnement normal de leur valve mitrale avec une surface
fonctionnelle dépassant habituellement 2 cm2sans fuite ou avec
une fuite résiduelle minime.
Figure 6. Homogreffe mitrale partielle.
6a. Volumineuse végétation appendue à un abcès dans une région com-
missurale.
6b. Résection complète des lésions infectées.
6c. Homogreffe mitrale partielle comportant la région commissurale
avec ses cordages et son chef de pilier.
6d. Résultat de la reconstruction après mise en place d’un anneau pro-
thétique.
Dossier - Chirurgie - C.A. 6/05/04 16:59 Page 22
 6
6
1
/
6
100%