Contrôle de transformations

Contrôle de
transformations
I. Changement d’un réactif
!"
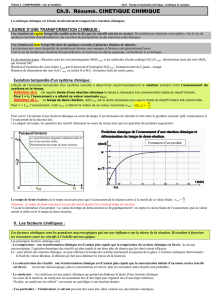
Réaction d’estérification
• Présentation des anhydrides d’acide
Formule générale :
Nomenclature : le nom s’obtient en remplaçant le mot acide de
l’acide dont il provient par anhydride.
Exemple :
• Estérification avec un anhydride d’acide
On peut remplacer l’acide par l’anhydride d’acide :
Equation-bilan :
Contrairement à la réaction d’estérification avec un acide, la
réaction est rapide et l’avancement maximal est atteint.
!"
L’hydrolyse basique de l’ester ou saponification
La saponification est la réaction entre un ester et l’ion hydroxyde :
la base forte hydroxyde remplace l’eau.
Elle donne un ion carboxylate et un alcool.
!"
Equation-bilan :
Cette réaction est lente mais l’avancement maximal est atteint.
Anhydride propanoïque
II. Fabrication d’un savon
Pour fabriquer des savons on utilise comme matière première des
corps gras, qui sont des triesters du glycérol et des acides gras.
Leur saponification donne les savons.
!"
Réaction de saponification à partir d’un triester du
glycérol
!"
Relargage
Afin de séparer le savon du glycérol et de la soude en excès, on
procède au relargage. Cette opération consiste à placer le
mélange obtenu dans de l’eau salée, ce qui sature la solution et fait
précipiter les carboxylates de sodium.
!"
Lavage
De manière à éliminer le reste de soude très caustique pour la
peau, on lave le solide obtenu.
Les techniques expérimentales relatives aux réactions de
saponification se trouvent dans le MemoPage intitulé
« techniques de laboratoire en chimie organique ».
III. Mode d’action des savons
!"
Un savon est composé de molécules tensioactives :
les carboxylates
Une molécule tensioactive est constituée d’une tête hydrophile
(lipophobe) et d’une longue chaîne carbonée hydrophobe
(lipophile).
La tête hydrophile correspond au groupement : - COO –
Le corps hydrophobe correspond à la chaîne carbonée.
!"
Mode d’action des savons
1. Une tâche de graisse a été faite sur un tissu.
2. Les molécules tensioactives du savon entrent en contact avec
la tâche, les parties hydrophobes se placent au contact du
corps gras alors que les têtes hydrophiles sont à l’extérieur.
3. Lors du rinçage, l’eau entraîne les micelles ainsi formées.
IV. La catalyse
Définition : La catalyse est le phénomène d’accélération d’une
réaction chimique sous l’action d’une substance chimique appelée
catalyseur.
Il existe différents types de catalyses :
• la catalyse hétérogène où les réactifs et le catalyseur
n’appartiennent pas à la même phase ( par exemple un
catalyseur solide et des réactifs liquides ).
• la catalyse homogène où les réactifs et le catalyseur
appartiennent à la même phase ( liquide ou gazeuse )
• la catalyse enzymatique où ce sont ces protéïnes qui
catalysent les réactions ( dans les organismes vivants ).
• Remarques : Les enzymes appartenant à la même phase que
les réactifs dont ils catalysent la réaction, la catalyse
enzymatique est une catalyse homogène.
MemoPage.com SA © / nov. 2002 / Auteur : Emmanuel Parras / ISSN : en cours
Avec le , personnalisez votre mobile
Encore plus de choix sur le 3214 !
Service ouvert aux téléphones fixes et mobiles, recommandé par Bouygues Telecom
*0,34 €/mn + tarif de votre opérateur. Voir liste des opérateurs, tarifs et mobiles compatibles au 0 805 907907 (appel gratuit
depuis un fixe). Service disponible au 10/03/2003 et susceptible d’évoluer. Bouygues Telecom – 20 quai du Point du Jour –
92100 Boulogne Billancourt. SA au capital social de 606 661 789,28 € 397 480 930 RCS Nanterre.
1
/
1
100%