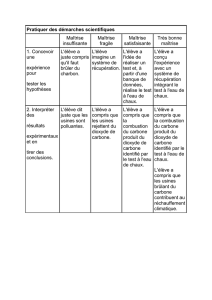
A) Chimie organique

CH 6: LA COMBUSTION DES MATERIAUX ORGANIQUES
Objectifs:
*Prendre conscience du danger de la combustion de certaines
matiè
res plastiques.
*Reconna
î
tre la formation de carbone et de dioxyde de carbone.
*Savoir que, lors d'une combustion, il se forme de l'eau et parf
ois
des produits toxiques.
Noter sur le cahier de texte pour la séance prochaine
Ex
7,9,10,11,
p64
-
65
ED et FM:p63
Ex
7,9,10,11
p64
-
65
ED et FM:p63

I) Mati
è
res ou d
é
chets organiques.
CHIMIE:
A)Chimie organique
-
Chimie g
é
n
é
rale ou chimie physique.
-
Chimie min
é
rale.
-
Chimie des syst
è
mes biologiques ou biochimie.
-
Chimie organiques .
( chimie du carbone ).
La chimie organique
é
tudie
essentiellement
les propri
é
t
é
s des
mol
é
cules et des compos
é
s contenant essentiellement
les atomes de carbone
C
et accessoirement
{
H
,
O,
Cl, P,S,
N
}
.
B) Origine des substances
( ou d
é
chets ) organiques.
*Animale:
*Ou de synth
è
se : obtenue par r
é
action chimique.
*Végé
tale:
On dé
fini un compos
é
organique toute esp
è
ce chimique provenant d
’
un
matériau d
’
origine vivante.
-
autres chimies
…

Remarques: Extraits de la d
é
finition de la chimie organique .
Le terme de
chimie organique
appara
î
t pour la premi
è
re fois en 1807 gr
â
ce au su
é
dois
Jacob
Berz
é
lius
. Il d
é
finit comme compos
é
organique toute esp
è
ce chimique provenant
d’un mat
é
riau d
’
origine vivante. D'autres chimistes, tels que
Friedrich W
ö
hler
ou
August K
é
kul
é
, ont beaucoup oeuvr
é
pour le d
é
veloppement de la chimie organique.
Plus tard, de nombreuses synth
è
ses organiques permettent l
’
obtention de
compos
é
s
synth
é
tiques
, une nouvelle d
é
finition est alors n
é
cessaire. La chimie organique est
aujourd
’
hui la chimie des compos
é
s carbon
é
s, naturels ou synth
é
tiques.
Outre le carbone, les esp
è
ces organiques ne contiennent qu
’
une gamme r
é
duite
d’élé
ments
: l
’
hydrog
è
ne H, l
’
oxyg
è
ne O, l
’
azote N ou plus rarement le soufre S, le
phosphore P et le chlore Cl.
Tous les compos
é
s organiques naturels ont une origine biologique. Ainsi, la
photosynth
è
se
permet aux plantes, sous l
’
effet de la lumi
è
re, de transformer l
’
eau puis
é
e
dans le sol et le dioxyde de carbone CO
2
de l
’
air en
glucides
(cat
é
gorie de compos
é
s
organiques essentiels
à
l'alimentation de tout
ê
tre vivant) et en dioxyg
è
ne O
2
.
De nos jours, beaucoup de compos
é
s organiques sont extraits
à
partir du
p
é
trole
,
mélange de plus de deux cents mol
é
cules d
’
hydrocarbures
(compos
é
s organiques form
é
s
uniquement de carbone et d
’
hydrog
è
ne).
La chimie organique s
’
emploie
à
la fois
à
«
copier
»
la nature, et donc
à
reproduire des
compos
é
s existants sur Terre, mais aussi
à
l
’
enrichir par la synth
è
se de nouveaux
é
difices
atomiques.

Expé
riences.
le dioxyg
è
ne ne r
é
agit pas sur les mat
é
riaux organiques.
A) Froid:
II)Les produits de la combustion des mati
è
res organiques.
Proposer un dispositif expérimental
( avec matériel et mode opératoire )
qui vous permet d'identifier les
produits de la combustion complète des
matières organiques .

B)
Combustion compl
è
te des mati
è
res organiques.
1)
combustion du papier.
SUPPORT
Tige de
fixation
Entonnoir
Tube plastique
EAU de
CHAUX
soucoupe
Papier
Eau de chaux
troubl
é
e
Cendres
Bu
é
e
Eau de chaux troubl
é
e:
gaz
( C
O
2
).
Buée :
vapeur d
’
eau
(
H
2
O
).
Expé
riences.
le dioxyg
è
ne ne r
é
agit pas sur les mat
é
riaux organiques.
A) Froid:
II)Les produits de la combustion des mati
è
res organiques.
B.R:
dioxyde de carbone
+
eau
E.B:
?
+
CO
2
+
H
2
O
C
C
x
H
H
y
O
O
O
z
papier
+
dioxyg
è
ne
O
2
 6
6
 7
7
 8
8
 9
9
1
/
9
100%