Facteurs génétiques impliqués dans la prédisposition et la

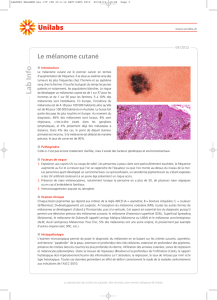
Figure 1. Gène CDKN2A et contrôle du cycle cellulaire. Le gène CDKN2A code pour
2 transcrits, P16INK4A et P14ARF, qui contrôlent le cycle cellulaire par 2 voie complé-
mentaires, la voie cycline D1-CDK4-Rb et la voie MDM2-P53.
RB-E2F p53
MDM2
CDK4-cycline D
CDK6
p16 INK4a p14 ARFCDKN2A
Oncogènes
Dégradation
Gènes suppresseurs
de tumeur
E2F
p21 Bax
Apoptose
+
+
–
p
G2
G1
M
S
Point START
544 | La Lettre du Cancérologue ̐ Vol. XX - n° 9 - novembre 2011
DOSSIER THÉMATIQUE
Oncodermatologie
Facteurs génétiques impliqués
dans la prédisposition et
la progression du mélanome
Genetic factors involved in melanoma predisposition
and progression
N. Soufir*
* Service de génétique, hôpital Bichat
Claude-Bernard, Paris ; Inserm U976,
centre de recherche sur la peau,
hôpital Saint-Louis, Paris ; université
Paris-VII.
D
es progrès considérables ont été accom-
plis dans la connaissance de la prédisposi-
tion génétique au mélanome au cours de la
dernière décennie. Une histoire familiale de mélanome
est parmi les facteurs de risque les plus établis : il
est estimé que 10 % des cas de mélanome résultent
d’une prédisposition héréditaire (1). Deux gènes de
forte pénétrance prédisposant au mélanome ont été
identifiés à ce jour, CDKN2A et CDK4 (2-4), mais de
nombreux autres biomarqueurs à risque, dont la péné-
trance est moindre, ont également été caractérisés.
Parallèlement, des progrès considérables ont été
accomplis en ce qui concerne les événements
génétiques se produisant à l’intérieur des tumeurs,
permettant de caractériser de nouvelles cibles théra-
peutiques, avec pour la première fois l’obtention
de réponses thérapeutiques encourageantes aux
nouveaux traitements (thérapies ciblées).
Par ailleurs, le terrain génétique de l’hôte semble
également jouer un rôle important dans l’évolution
du mélanome, et notamment dans la qualité de la
réponse immunitaire.
Facteurs génétiques impliqués
dans la susceptibilité
au mélanome
Gènes de susceptibilité
de forte pénétrance
◆CDKN2A
Mélanome familial
En 1994, le gène CDKN2A a été identifié comme le
premier gène de susceptibilité au mélanome de forte
pénétrance. Des mutations germinales de CDKN2A
sont présentes dans environ 20 % des familles de
mélanome (5).
Le gène CDKN2A, situé sur le chromosome 9p21,
code pour 2 protéines structurellement distinctes
agissant comme suppresseurs de tumeurs (figure 1).

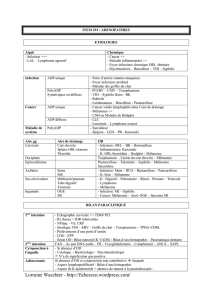
Figure 2. Exemple typique
d’une famille prédisposée
au mélanome. Huit malades
sont atteints de mélanome
et trois d’entre eux ont déve-
loppé plusieurs mélanomes.
Le cas index est indiqué par
une flèche, et une mutation
du gène CDKN2A a été iden-
tifiée chez lui. Cette muta-
tion a ensuite été retrouvée
chez plusieurs membres de
la famille (*).
5 mélanomes
*
***
2 mélanomes 2 mélanomes
La Lettre du Cancérologue ̐ Vol. XX - n° 9 - novembre 2011 | 545
Points forts
»Des progrès considérables ont été réalisés dans la génétique du mélanome.
»
Trois gènes majeurs de prédisposition ont été identifiés (CDKN2A, CDK4, BAP1), mais ils concernent
une faible proportion de malades (mélanome familial, mélanome multiple sporadique). Cela a permis de
mettre en place un conseil génétique dans les familles à risque et une surveillance optimale des sujets
porteurs d’une mutation prédisposante.
»De nombreux polymorphismes génétiques augmentant le risque ont aussi été caractérisés, concernant
la majorité des mélanomes, et appartenant principalement à des gènes de pigmentation (récepteur de
type 1 à la mélanocortine, SLC45A2).
»La génétique somatique du mélanome a également énormément progressé. Un élément capital est la
découverte des mutations activatrices de l’oncogène BRAF, ayant permis la mise en œuvre de thérapies
ciblées et révolutionnant le traitement du mélanome métastatique.
Mots-clés
Mélanome
Prédisposition
Progression
CDKN2A
BAP1
MC1R
BRAF
KIT
Highlights
»
Considerable progresses
have been made in melanoma
genetics.
»
Three major susceptibility
genes have been identified
(CDKN2A, CDK4, BAP1), but
which are involved in a small
proportion of patients (familial
melanoma, sporadic multiple
melanoma ). This has allowed
to organize genetic counseling
in at risk families and optimal
monitoring of subjects carrying
a predisposing mutation.
»
Many genetic variants
increasing melanoma risk have
also been characterized. These
variants concern the majority
of sporadic melanomas, and
belong mainly to pigmenta-
tion genes (type 1 melanocortin
receptor, SLC45A2...).
»
Genetic somatic events
melanoma has also consider-
ably progressed. A key factor
was the identification of an
activating mutation in the BRAF
oncogene. This has allowed the
discovery of specific targeted
therapy, and has revolutionized
the treatment of metastatic
melanoma.
Keywords
Melanoma
Predisposition
Progression
CDKN2A
CDK4
BAP1
MC1R
BRAF
KIT
Les exons 1α, 2 et 3 codent pour p16INK4a, tandis
qu’un exon 1 alternatif, l’exon 1β, est transcrit en
utilisant un promoteur différent, épissé aux exons 2
et 3, dans un cadre de lecture différent, permettant
de coder pour la protéine p14ARF (ARF, aussi appelé
p19ARF chez la souris). P16INK4a joue un rôle clé
dans le cycle cellulaire en contrôlant le point de tran-
sition G1-S, par l’intermédiaire de la protéine du réti-
noblastome (PRB). L’autre produit du locus CDKN2A,
p14ARF, agit aussi comme un gène suppresseur de
tumeur. ARF agit notamment via une interaction
avec MDM2, entraînant une stabilisation ainsi qu’une
accumulation de la protéine TP53 et aussi de sa cible
en aval, p21, un inhibiteur non seulement de CDK4
et CDK6, mais aussi des autres CDK (6).
La fréquence des mutations de CDKN2A augmente
avec le nombre d’apparentés atteints et avec la
présence de mélanomes multiples chez le même
patient (figure 2) [7] ainsi que de cas de cancer du
pancréas dans la famille (7, 8). Par opposition, la
prévalence des mutations germinales de CDKN2A
dans la population générale est extrêmement faible.
Dans une étude australienne (état du Queensland),
J. Aitken et al. (9) l’estiment à seulement 0,2 % de
tous les cas de mélanome. La plupart des mutations
affectent également la protéine P14ARF car elles
sont situées dans l’exon 2. Des mutations spécifiques
d’ARF ont également été décrites, certaines associées
à un syndrome particulier, le syndrome mélanome-
astrocytome (OMIM 155755), dans lequel on observe
une co-ségrégation de mélanomes et de tumeurs du
système nerveux central (10).
Mélanome multiple sporadique
Le second groupe de malades porteurs de muta-
tions de CDKN2A est celui des patients atteints de
mélanomes multiples sporadiques. Les résultats de
4 grandes études montrent un taux de mutations
allant de 9 à 15 % (11).
Augmentation du risque d’autres cancers dans les
familles mutées CDKN2A
Il y a clairement un risque accru de cancer du pancréas
dans les familles présentant des mutations de
CDKN2A, avec un risque estimé 22 fois plus élevé
chez les individus porteurs d’une mutation germi-
nale CDKN2A (12). Plusieurs autres groupes ont
rapporté la survenue d’un cancer du pancréas dans
les familles de mélanome mutées (13), et les patients
qui développent à la fois un mélanome et un cancer du
pancréas sont porteurs de mutations de CDKN2A (14).
Un risque accru de cancers du sein, de la prostate,
du côlon, de cancers du poumon et de carcinomes
épidermoïdes (SCC) a été suggéré, mais il n’est pas
établi avec certitude.
Facteurs modifiant la pénétrance des mutations
CDKN2A
Les études épidémiologiques suggèrent que la péné-
trance des mutations de CDKN2A est modifiée par
d’autres facteurs, génétiques ou environnementaux.
Elle a été estimée à 30 % avant l’âge de 50 ans et
à 67 % à l’âge de 80 ans. Cependant, il existe une
disparité géographique, avec un risque de méla-
nome à l’âge de 80 ans de 58 % dans les pays euro-

546 | La Lettre du Cancérologue ̐ Vol. XX - n° 9 - novembre 2011
DOSSIER THÉMATIQUE
Oncodermatologie Facteurs génétiques impliqués dans la prédisposition
et la progression du mélanome
péens, contre 91 % en Australie (15), soulignant une
inter action potentielle entre les rayons ultraviolets
(rayons UV) et les mutations de CDKN2A.
En outre, il a été démontré que la présence de
nævus dysplasiques cliniquement identifiés, le
nombre total de nævus et les antécédents de coups
de soleil augmentent considérablement le risque
de mélanome en Europe, en Amérique du Nord et
en Australie (16). Enfin, plus récemment, il a été
démontré que des variants fonctionnels du gène
MC1R augmentaient également la pénétrance des
mutations de CDKN2A.
◆CDK4
Dans le monde, environ 13 familles ont été signalées
comme porteuses de mutations du gène CDK4. Fait
intéressant, toutes les mutations se produisent dans
le codon 24, avec 2 familles porteuses d’un change-
ment R24C ou R24H (17). Le résidu R24 est critique
dans l’interaction p16INK4a-CDK4 et, lorsqu’il est
substitué, p16INK4a ne peut plus se lier ni inactiver
la protéine oncogénique CDK4, ce qui induit une
mutation “gain de fonction” (18).
◆BAP1
Très récemment, un nouveau gène de prédisposition
au mélanome, BAP1, a été identifié. Ce gène avait
tout d’abord été retrouvé muté dans un fort taux de
mélanomes oculaires (19). Des mutations germinales
de BAP1 ont ensuite été identifiées, principalement
dans des familles de mélanomes comprenant des
mélanomes oculaires (20). Ce gène prédispose
également à la survenue de mésothéliomes (21),
et peut-être d’autres cancers.
◆Indications et prescriptions du test génétique
Les indications du test génétique sont les suivantes :
➤
au moins 2 cas de mélanomes sur la même
branche parentale aux degrés 1 ou 2, dont l’un au
moins est invasif ;
➤
au moins 2 mélanomes invasifs chez la même
personne ;
➤
au moins 2 mélanomes chez la même personne,
l’un invasif, l’autre in situ, le premier avant 40 ans ;
➤
un cancer du pancréas peut remplacer un méla-
nome.
Le test génétique sera prescrit en consultation indi-
viduelle après information et signature d’un consen-
tement éclairé. Le résultat sera rendu lors d’une
deuxième consultation et, en cas d’identification
d’une mutation, un diagnostic présymptomatique
sera proposé aux apparentés. En cas de mutation,
une surveillance stricte des lésions pigmentées en
milieu hospitalier aura lieu tous les 3 à 6 mois, avec
exérèse de toute lésion suspecte.
◆Autres gènes de forte pénétrance
BRCA2
BRCA2 est un des 2 gènes majeurs de prédisposition
au cancer du sein. Globalement, il a été démontré
qu’il existe un surrisque de mélanome dans les
familles mutées BRCA2. BRCA2 a été peu étudié dans
les familles dont plusieurs membres sont atteints de
mélanomes, définition du mélanome familial ; des
mutations de BRCA2 ont été rapportées chez 2 %
des familles de mélanomes en Sardaigne.
Identification d’autres locus impliqués dans la
prédisposition génétique au mélanome
Un consortium international sur la prédisposition au
mélanome, GenoMEL, comprenant des groupes de
recherche majeurs d’Amérique du Nord, d’Europe,
d’Asie et d’Australie, a permis de collecter un grand
échantillon de familles de mélanomes en vue de
caractériser les mutations dans les gènes à haut
risque de susceptibilité au mélanome.
Plusieurs autres régions ont ainsi été identifiées :
9p21 et 1p22 pour le mélanome seul, et 9q21 pour
l’association d’un mélanome cutané et d’un méla-
nome oculaire.
Prédisposition multifactorielle
au mélanome
Au contraire de la prédisposition liée à des gènes
majeurs de forte pénétrance, la susceptibilité multi-
factorielle est liée à des polymorphismes ayant
chacun une faible pénétrance et qui interagissent avec
les facteurs environnementaux, principalement les
UV, et modulent le risque de mélanomes (figure 3).
Ces variants génétiques ont été identifiés soit grâce à
des études du type “gène candidat” (principalement
pour les gènes de pigmentation), soit grâce à des
études d’association dites “tout génome” (Genome-
Wide Association Studies [GWAS]), au cours desquelles
l’ensemble du génome est étudié sans a priori.
Les gènes les plus fréquemment impliqués sont ceux
impliqués dans la voie de la pigmentation (22, 23).
Le gène le mieux étudié est le gène codant pour le
récepteur de type 1 à la mélanocortine (MC1R) [24].
MC1R est le plus connu et le mieux étudié des locus
à faible pénétrance de susceptibilité au mélanome.
Le gène MC1R, localisé en 16q, code pour un récepteur
transmembranaire couplé à une protéine G (figure 4)

Figure 3. Récepteur de type 1 à la mélanocortine (MC1R). Ce récepteur possède 7 domaines
transmembranaires, et sa stimulation par l’α-MSH favorise la synthèse d’eumélanine
(marron, photoprotectrice) aux dépens de la phaéomélanine (rouge orangée, peu photo-
protectrice et mutagène). Le gène est très polymorphe dans la population caucasienne.
De nombreux variants sont représentés (différentes couleurs) dont certains (rouge) sont
associés aux cheveux roux et au risque de mélanome.
Mélanome
Cheveux/poils roux (humain,
cheval) ou pales (ours)
Sites liés au mélanome pour
les rock pocket mouse
Cheveux roux (humain)
Melanism in ?
Rock pocket mouse
Jaguarundi
Bananaquit
Récepteur de type 1
à la mélanocortine
(MC1R) Humain
Humain
Rock pocket mouse
Ours noir
Jaguar
NH2
Pig. sheep
A109W
A18C
95-102
101-105
Souris
Vache, cochon
Souris, poulet
Souris
Mouton
Cheval
L100P
L99P
E94K
S83F
871L M73K
A151C
A160W
Y298C
D294H
COOH
Q233H
D121N
C125R
Fox
Variants RHC = cheveux roux
Figure 4. Prédisposition au mélanome : gènes de forte pénétrance et prédisposition
multifactorielle.
Prédisposition au mélanome
Monogénique
CDKN2A, CDK4
Conseil génétique
Surveillance des sujets à risque Futurs biomarqueurs ?
Multifactorielle
Variants fréquents
MC1R
TYR
SLC45A2
ASIR
EDNRB...
Mélanome familial, multiple,
+ cancer pancréas
Variants rares
La Lettre du Cancérologue ̐ Vol. XX - n° 9 - novembre 2011 | 547
DOSSIER THÉMATIQUE
composé de 317 acides aminés, qui est exprimé dans
plusieurs types cellulaires, y compris les mélano-
cytes et les kératinocytes. La stimulation de MC1R
par l’hormone α-mélanocyte-stimulante (α-MSH)
active l’adénylcyclase et augmente la concentration
de l’adénosine monophosphate cyclique (AMPc),
induisant la synthèse du pigment noir photoprotec-
teur, l’eumélanine, plutôt que de la phaéomélanine,
pigment rouge orangé. MC1R est très polymorphe
dans les populations caucasiennes, et il existe de
nombreux variants de MC1R pouvant conduire à une
perte de fonction, en diminuant la production d’AMPc,
soit l’affinité de liaison de l’α-MSH (25).
Plusieurs allèles perte de fonction de MC1R (R142H,
R151C, R160W et D294H) ont été montrés comme
fortement associés avec les cheveux roux et le phéno-
type peau claire-difficulté à bronzer (variants dits
RHC, pour Red Hair Color). Ces variants RHC sont très
fréquents dans les populations d’origine celte, mais
moins fréquents dans les pays du sud de l’Europe
(France, Espagne, Italie, Grèce), dans lesquels d’autres
variants de MC1R ont aussi été associés au risque
de mélanome. Plusieurs études ont été réalisées à
travers le monde, montrant une nette augmenta-
tion du risque de mélanome (OR > 2) chez les indi-
vidus portant un variant fonctionnel de MC1R, et le
doublement du risque lorsque 2 allèles variants sont
présents (26-28). Fait important, l’effet de MC1R sur
la prédisposition au mélanome semble impliquer, au
moins en partie, des mécanismes indépendants de
son effet sur la pigmentation dans les populations
européennes (27, 28). Le risque de mélanome persiste
souvent après stratification sur les caractéristiques
pigmentaires (type ou couleur de peau, couleur des
yeux ou des cheveux, nombre de nævus).
◆Autres gènes de pigmentation
Un polymorphisme faux-sens (Leu374Phe) du gène
SLC45A2/MATP (22, 29-31) a été montré comme
protégeant assez fortement du risque de méla-
nome (OR = 0,35). Ce polymorphisme est à l’état
homozygote Leu/Leu dans les populations d’Afrique
noire, alors que l’allèle 374Phe est spécifique de la
population caucasienne. Dix à 20 % de la population
caucasienne est porteuse du variant 374Leu et est, de
ce fait, partiellement “protégée” du mélanome. De
manière intéressante, l’allèle 374Leu est associé à la
couleur foncée de la peau, des cheveux et des yeux,
mais l’association au mélanome est indépendante
du phénotype pigmentaire (et l’effet additif à celui
de MC1R). SLC45A2/MATP code pour une protéine
mélanosomale impliquée dans l’albinisme de type 4
(OCA4). On peut en rapprocher l’association de poly-
morphismes du gène codant pour une autre protéine
mélanosomale, OCA2 (32), dont les mutations sont
responsables de l’albinisme occulocutané de type 2.
Des variants du gène codant pour la protéine de
signalisation agouti (ASIP), l’antagonisme de MC1R,
ont aussi été associés au risque de mélanome (33).

Figure 5. Les différentes voies de signalisation impliquées dans l’oncogenèse du mélanome.
La voie des MAP kinases (avec l’oncogène BRAF, en bleu), le récepteur KIT et son ligand
(en violet), l’oncogène NRAS (en vert), la voie de la PI3 kinase (en vert), et MITF (en vert).
BRAF
NRAS PI(3)K
AKT3
mTOR
PTEN
NEDD9
Migration, invasion
Croissance cellulaireProlifération, survie
Transcription
*
*
*
*
*
*
*
*
SCF
MEK
ERK
MITF
K
I
T
Figure 6. Principaux facteurs génétiques impliqués dans la progression du mélanome. On
distingue des facteurs somatiques (propres à la tumeur) et les facteurs constitutionnels
(propres au malade).
Facteurs somatiques
BRAF
NRAS
CDKN2A
CKIT
PTEN
WNT5A
MMP8
GRM1
Polymorphismes
Gènes de réparation
Immunité
Récepteur de la vitamine D
Facteurs constitutionnels
Progression
Réponse au traitement
Classification tumorale
548 | La Lettre du Cancérologue ̐ Vol. XX - n° 9 - novembre 2011
DOSSIER THÉMATIQUE
Oncodermatologie Facteurs génétiques impliqués dans la prédisposition
et la progression du mélanome
Des polymorphismes de gènes codant pour des
enzymes impliqués directement dans la mélano-
genèse ont aussi été associés au risque de mélanome,
qu’il s’agisse du polymorphisme thermosensible
R402Q de l’enzyme tyrosinase, enzyme clé de la
mélanogenèse (TYR, gène de l’albinisme de type I),
ou de polymorphismes de la TYRP1 (Tyrosinase-
Related Protein 1) [33].
Récepteurs de l’endothéline B (EDNRB)
Des mutations d’un gène impliqué dans la différen-
ciation mélanocytaire et la maladie de Hir schrung
ont été identifiées dans la prédisposition au
mélanome familial (34). Les hypothèses physio-
pathologiques sont une moindre différenciation
mélanocytaire conduisant à une moins bonne
photoprotection ou à une transformation maligne
plus facile des mélanocytes.
Gènes associés au nombre de nævus
Des études d’association “tout génome” ont permis
d’identifier des variants associés au nombre de
nævus, dans les gènes MTAP (situé en 9p21) et
PLAG26 (en 22q13.1). Des variants de ces gènes
ont aussi été associés au risque de mélanome (35).
◆Autres gènes
Des polymorphismes d’autres gènes, non liés direc-
tement à la pigmentation, ont aussi été identifiés
récemment par des études d’association pan-géno-
mique (GWAS) à d’autres locus génétiques : tert-
CLPTM1 (codant pour la télomérase), CASP8, ATM,
MX2 et 1q21.3 (31, 36-39).
Facteurs génétiques
impliqués dans la progression
du mélanome (figure 5)
Classiquement, le développement du mélanome et
sa progression se déroulent en 6 étapes :
1. nævus mélanocytaire bénin acquis ;
2. nævus mélanocytaire avec hyperplasie mélano-
cytaire lentigineuse ;
3. nævus mélanocytaire avec atypies nucléaires,
c’est-à-dire une dysplasie mélanocytaire ;
4. mélanome au stade de croissance horizontale
(RGP) ;
5. mélanome en croissance verticale (VGP) ;
6. mélanome métastatique.
Il est maintenant prouvé que les facteurs génétiques
ont une importance cruciale dans la progression tumo-
rale et sur le pronostic. Parmi les facteurs génétiques
jouant un rôle dans la progression du mélanome, il
est possible de distinguer les facteurs somatiques,
présents dans les tumeurs, des facteurs constitution-
nels, présents dans l’ADN des patients eux-mêmes.
Facteurs génétiques somatiques
La caractérisation des facteurs génétiques soma-
tiques acquis a montré l’existence de différents
 6
6
 7
7
 8
8
1
/
8
100%