Les tissus musculaires Le tissu musculaire strié squelettique L

I) Le tissu musculaire strié squelettique
a. L’organisation
Page 2
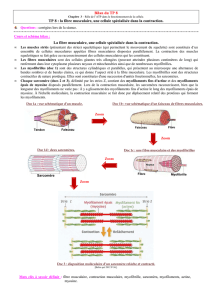
Tissu responsable des mouvements volontaires, tissu le plus abondant de l’organisme.
Sur le plan macroscopique, il y a un muscle avec une partie centrale et des extrémités, les
tendons qui viennent insérer le muscle de manière solide sur les pièces osseuses.
Si on effectue une coupe de la masse musculaire, schéma du dessous, on remarquera un
certain nombre de faisceau avec à l’intérieur des cellules musculaires striées squelettiques que
l’on appelle les rhabdomyocytes. Ces faisceaux sont séparés par des travées conjonctives, le
périmysium.
Le muscle lui-même est entouré par un tissu conjonctif collagénique (épimysium,
aponévrose).
Dans les travées conjonctives, on retrouve des vaisseaux, des artères, des veines, des nerfs
(tissu innervé).
Les rhabdomyocytes sont séparées par de fines travées conjonctifs, les endomysium dans
lesquelles on va trouver de nombreux capillaire qui vont vasculariser les rhabdomyocytes.
b. Le rhabdomyocyte
A l’échelle cellulaire, cytologie (MO), page 4.
Le rhabdomyocyte est l’unité fonctionnelle du tissu. C’et une cellule en forme de ruban, à
contour parallèle, ce sont des cellules de grande taille (variable selon leur localisation) jusqu’à
30 cm pour les muscles des membres inferieurs. Leur diamètre varie de 10 à 100 µm.
Coupe longitudinale, membrane plasmique doublée extérieurement par une membrane
basale, association membrane plasmique membrane basale = sarcolemme. Sous la
membrane plasmique, on a un certain nombre de noyaux qui occupent une localisation
sous sarco-plasmique, ce sont des cellules multinucléés (fonction de la taille
cellulaire). Le cytoplasme de ces cellules comporte deux compartiments, celui des
protéines contractiles formant des myofibrilles, l’ensemble de ces myofribrilles
constitue le myoplasme. En dehors de ce myoplasme, les autres éléments du
cytoplasme constituent le sarcoplasme. On voit sur le schéma qu’il existe une striation
transversale caractéristique de ce type cellulaire, elle est constituée par l’alternance de
bande sombres et de bandes claires (coupe longitudinale !). Cellules isolées .
Coupe transversale. 1
Coupe transversale 2

Coupe 3, le myoplasme est constitué de myofibrilles qui vont se regrouper en amas, ce
sont les champs de Conheim. Le sarcoplasme est le cytoplasme qui se trouve entre
les amas mais aussi entre les myofribrilles. MO
Ultrastructure MET.
Page 3.
Une myofibrille est constituée de protéines contractiles que l’on appelle les myofilaments.
Deux grands types de myofilaments, les myofilaments épais qui sont constitués par une seule
protéine qui est la myosine. Myofilaments fins constituées d’Actine, Troponine et
Tropomyosine. Il y a juxtaposition et interpénétration des myofilaments épais et fins. Ces
myofilaments vont constituer l’unité contractile du rhabdomyocyte que l’on appelle le
Sarcomère.
Sarcomère.
Espace compris entre deux stries Z, au centre, myofilaments épais de myosine.
Voir petit schéma manuscrit.
Si l’on considère les disques A, bande centrale plus claire que l’on appelle la bande H, c’est
la zone de la bande A où il n y a que des myofilaments épais. Au centre de la bande H, ligne
M, au centre du disque A et de la bande H.
Lorsque l’on additionne bout à bout des sarcomères, on obtient des myofribrilles qui vont
parcourir la cellule dans toute sa longueur. Les sarcomères sont orientées de façon
longitudinale selon le grand axe cellulaire.
Ce qui est responsable de la striation transversale que l’on voit en coupe longitudinale, c’est
l’arrangement particulier des sarcomères dans les myofibrilles. Le diamètre des myofibrilles
est de 1 à 2 µm.
Les myofilaments épais.
Constitués de molécules de myosine (schéma du milieu de la page 5). Ces molécules sont
volumineuses, on retrouve à l’intérieur 4 chaines polypeptidique légères et 2 lourdes.
Les 2 lourdes chaines polypeptidiques sont entourées en hélice alpha. A l’extrémité N
terminale, chacune des deux chaines présentent un enroulement en motte ce qui forme une
tête globuleuse au niveau de l’extrémité N terminale.
Quand aux chaines légères, une paire de chaine légère vient se localiser à chacune des têtes.
Ces molécules de myosine s’organisent entre elles pour former un myofilaments épais (300
molécules de myosines). Arrangement particulier car les molécules vont s’organiser tête
bèche, l’une d’un côté et l’autre de l’autre côté.
La ligne M est formée par une protéine que l’on appelle la myomésine qui permet de lier les
molécules de Myosine entre elles.
Deux remarques importantes : au niveau de chacune des têtes de myosine, il y a un site de
fixation pour l’actine et d’autre part une activité ATPase (capacité d’hydrolyse de l’ATP) qui
est actine-dépendante.
Les myofilaments fins.
Trois types de protéines.

L’actine, protéine de petite taille globulaire, les monomère de G actine ont une
propension à former de la F actine c'est-à-dire de l’actine fibrillaire. A l’intervalle
entre les molécules d’actines viennent se localiser la tropomyosine, protéine de deux
chaines enroulées en hélice alpha (schéma de page 11). A intervalle régulier, on
retrouve également de la troponine constituée de trois sous unités (TnC qui va fixer
les ions calciums, TnT qui rentre en contact avec la tropomyosine et TnI qui va inhiber
le contact entre l’actine et les têtes de myosine.
Dans le muscle l’actine doit avoir une longueur et une structure stable, cela est possible dans
les myofilaments fins grâce à deux protéines, la protéine Cap Z à une extrémité et la
tropomoduline à l’autre extrémité du myofilaments fin.
Les éléments du cytosquelette dans les rhabdomyocytes.
Ils vont maintenir l’architecture et l’organisation structurale des myofibrilles.
Cytosquelette endosarcomérique et Cytosquelette exosarcomérique
Endosarcomérique 3 éléments, une molécule que l’on appelle TITIN, grosse molécule
qui permet d’ancrer les myofilaments épais ; les stries Z constituées d’alpha actinine ; la
nébuline, deux chaines qui entourent les myofilaments fins.
Cytosquelette exosarcomérique :
- Filament intermédiaire, desmine qui permet de relier les stries Z entre elles
- Les complexes dystrophine-glycoprotéines associées. (page 8). Dystrophine avec
deux chaines enroulées, occupant une position sous sarcolémmique , (Dystrophine
présente dans toutes les cellules musculaires). L’une des extrémités va se lier à l’actine
des myofilaments fins les plus périphériques, l’autre extrémité se lie à un complexe
moléculaire à deux sous unités, la Syntrophine (liaison à sous unité alpha) , et à un
deuxième complexe le Dystroglycane qui lui aussi a deux sous unités , (Dystrophine
liée à la sous unité béta)
Ce complexe permet d’ancrer les myofibrilles les plus périphériques à la membrane
basale. Cette Dystrophine est codée par un gène qui lorsqu’il est déficient donne la
maladie de Duchenne.
- Protéines costamères, contact focaux, il y a un complexe moléculaire sous
sarcolémmique avec notamment de la Vinculine qui se lie à l’alpha actinine qui se lie
aux stries Z des myofibrilles les plus périphériques. La Vinculine est aussi liée à la
Taline qui est liée a une intégrine (alpha 5/béta 1) qui est liée à une fibronectine de la
membrane plasmique.
Page 6 :
La membrane plasmique contient à intervalle de nombreuses invaginations profondes, ce sont
les tubules T. Ils se projettent dans l’union Disque I/ Disque A.
Autre élément important de ces cellules, le REL qui est appelée ici le réticulum
sarcoplasmique. C’est un réservoir de ions calciums. Il va se constituer d’une part par les
citernes terminales transversales qui sont situées de part et d’autre des tubules T. Lorsqu’on
associe tubule et citerne TRIADE qui vient se projeter aux frontières Disque I et disque A.
Ces citernes sont reliées entre elles par des tubules L qui forment un vaste réseau anastomosé
Dépolarisation membranaire parcoure la membrane plasmique, les tubules T ouverture des
canaux calciums des citernes terminales transversales par un phénomène de couplage voltage-
dépendant. Ouverture des canaux calciques entraine un afflux brutal d’ions calciums dans le
cytosol.

Autres organites importants, les mitochondries en position sous sarcolemmique mais
également entre les myofibrilles source d’energie.
On a également un grand nombre de vacuoles lipidiques, des grains de glycogène [ ici aussi,
source d’énergie] et de la myoglobine qui est liée à l’oxygène qu’elle va céder aux
mitochondries pour la synthèse d’ATP.
c. Innervation des rhabdomyocytes.
R = Rhabdomyocytes
MN = motoneurone
Innervation motrice (jonction neuromusculaire)
Motoneurone alpha.
Dans la corne intérieur de la moelle, à partir des corps cellulaires née un axone qui va
gagner le nerf et se retrouver à la surface des rhabdomyocytes qui va former une plaque
motrice = synsapse neuromusculaire.
En règle générale, un R est innervé par un seul Motoneurone alpha, mais l’inverse n’est pas
vrai. Le nombre de R innervées par MN alpha dépend de la finesse du mouvement considéré,
si mouvement fin un MN alpha innerve peu de R. Pour innerver l’ensemble du muscle, il
faut innerver plus de R.
L’unité motrice est l’ensemble des R innervés par un seul MN alpha.
Lorsque l’on considère un neurone, plusieurs dendrites mais un seul axone, cette axone étant
unique, il peut se séparer à sa terminaison pour donner plusieurs petits rameaux.
La plaque motrice = synapse neuromusculaire.
Sorte de gouttière à la surface de R.
Page 9. Si l’on considère une synapse trois parties : partie prés synaptique, partie synaptique
et partie post synaptique.
Partie présynaptique l’une des terminaisons axonales, qui est ronflée et limitée en
périphérie par une membrane plasmique axonale, à l’interieur, on a certain nombre
d’organites et des vésicules synaptiques où l’on trouve un neuromédiateur qui est ici
l’AcétylCholine. La membrane présyaptique est assez épaisse.
Fente synaptique primaire, espace étroit d’environ 60 nm et à l’intérieur un matériel amorphe
qui est constituée par la fusion des MB entourant R et les terminaisons axonales.
Partie Postsynaptique : Membrane plasmique du R en regard de la plaque motrice, cette
membrane plasmique est constituée de plusieurs invaginations que l’on appelle les fentes
synaptiques secondaires et c’est au niveau de ces fentes que l’on trouve les récepteurs de
l’AcétylCholine.
Innervation sensitive du muscle. (fuseaux neuro-musclaire et organes neuro-
tendineux)

Organes neurosanguineux qui se situent dans les tendons des muscles qui vont renseigner les
centres nerveux sur l’étirement des muscles.
La deuxième structure fuseau neuro-musculaire, dans la partie centrale du corps
musculaire, constitués par des R particuliers intra –fusales (partie centrale).
R particuliers car noyaux en positions centrales et myofibrilles en position périphérie. Ils sont
entourés par une fibre nerveuse sensitive et le tout est entouré par un peu de tissu conjonctif.
Ce nerf sensitif rentre en liaison avec le motoneurone alpha qui est présent dans la moelle
épinière. Les fibres intra fusales sont innervées par des MN gamma qui vont entrainer un
certain état de tension et de contraction musculaire de base permanent mais à un faible niveau,
cette contraction n’excite pas la fibre nerveuse sensitive.
Lors de la contraction musculaire, les MN se déclenchent, le degrés de contraction des
cellules intrafusales dépasse un seuil qui va exciter les cellules nerveuses sensitives
intrafusales. Elles informent les MN alpha sur l’état de contraction musculaire des cellules
intrafusales ce qui permet à l’organisme de s’adapter.
d) Les bases de la contraction musculaire
Voyons maintenant les mécanismes de contraction musculaire.
Page 5.
Lors de la contraction, le muscle se raccourcit car chacun des R se raccourcit car les
myofibrilles se raccourcissent car les sarcomères se raccourcissent.
Importance de ce raccourcissement des sarcomères, 20 à 50% par glissement des
myofilaments fins le long des myofilaments épais. L’extrémité de chacun des
myofilaments fins va aller vers la ligne M, hausse de l’interpénétration des myofilaments
fins dans les myofilaments épais. La bande H se raccourcit aussi. Ce qui ne change pas,
c’est la longueur du disque A.
Le cerveau donne un ordre moelle épinière, excitation du NM alpha, dépolarisation
membranaire le long de l’axone de MN alpha.
Lorsque cette dépolarisation arrive à l’extrémité axonale ouverture des canaux calcique de
la MP de l’extrémité axonale. La conséquence est une brutale augmentation de la
concentration calcique dans le cytosol fusion des vésicules synaptiques avec la membrane
pré synaptique. , libération d’Acétylcholine dans la fente synaptique primaire.
La conséquence et que l’Acétylcholine va se fixer sur son récepteur spécifique qui est présent
dans la membrane des fentes synaptiques secondaires. Une fois qu’elle est fixée ouverture
des canaux sodiques de la membrane plasmique du R, des ions sodiums chargées + vont
rentrer dans la cellule, inversion du potentiel membranaire.
Cette dépolarisation va alors se propager le long de la Membrane du R. Signal électrique puis
chimique puis électrique.
On a ici un couplage ligand dépendant.
Notons qu’il y a une enzyme dans la fente synaptique qui est
l’ACETYLCHOLINESTERASE qui va rapidement cliver l’ACH en A et en Choline ce
qui interrompre le processus
La dépolarisation membranaire se prolonge donc dans la Membrane des R et aussi dan.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%