D`une manière générale, l`inhabituel jeune âge au diagnostic doit

Prédisposition au cancer du sein et de l’ovaire
Dr Olivier Caron
Gustave Roussy
Mars 2016
Objectifs :
- Savoir reconnaître les indications de consultation de génétique
- Connaître les modalités de prise en charge des personnes porteuses de
mutation BRCA1 ou 2, PALB2.
- Connaître l’impact d’une mutation constitutionnelle sur la prise en charge
thérapeutique
Le cancer résulte de la conjonction de 3 facteurs : l’environnement, le
patrimoine génétique, le hasard. Il est important de distinguer patrimoine génétique
constitutionnel d’une personne, présent dans toutes les cellules nucléées d’un
individu, et matériel génétique somatique, qui ne concerne que certaines cellules,
notamment tumorales. La mutation du patrimoine génétique constitutionnel entraîne
la survenue d’une prédisposition.
Plusieurs gènes peuvent, lorsqu’ils sont porteurs d’anomalies génétiques, être
responsables d’une augmentation majeure du risque de cancer du sein. Deux
éléments permettent de suspecter une anomalie constitutionnelle: le nombre
inhabituel de cancer du sein dans une famille, et l’âge précoce des cancers. Les
situations suivantes doivent mener à la réalisation d’une consultation de génétique et
constituent des indications d’analyse de BRCA1 et BRCA2 :
- au moins 3 cas de cancers du sein chez des apparentées proches
1

- au moins deux cas, dont un diagnostiqué avant l’âge de 45 ans ou un cas
masculin
- un seul cas de cancer du sein, diagnostiqué avant 35 ans
- l’association chez une même personne ou dans une même famille d’un cancer
du sein et d’un cancer de l’ovaire.
- Un seul cas de cancer de l’ovaire de haut grade (séreux+++), diagnostiqué
avant 70 ans
- Un seul cas de cancer du sein triple négatif (absence de récepteurs aux
estrogènes, absence de récepteurs à la progestérone, absence de
surexpression de Cerbb2), diagnostiqué avant 50 ans
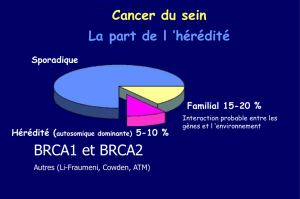
Figure 1: Situations évocatrices
de mutation BRCA1 ou
BRCA2
2

Les indications d’analyse de PALB2 sont identiques, sauf cas sporarique de cancer de
l’ovaire.
Pour les gènes BRCA1 et BRCA2, l’âge jeune et la présence de cancers de l’ovaire
dans la famille sont les deux facteurs les plus prédictifs. Dans les familles à cas
multiples de cancer du sein post-ménopausiques, la fréquence des mutations est très
basse.
La première étape consiste à identifier une anomalie dans une famille où elle est
suspectée. A ce niveau, une seule analyse est menée par famille, chez la personne
chez laquelle la probabilité de trouver l’anomalie si elle existe est la plus grande. Il
s’agit de la personne ayant développé le cancer à l’âge le plus jeune.
La consultation d’oncogénétique doit être une démarche volontaire de la part du
patient. Lors de cet entretien, l’oncogénéticien précise la structure familiale et les
3

antécédents. En fonction de tous ces éléments, il valide l’indication d’analyse
génétique.
Le résultat de cette analyse révèlera :
- soit une mutation délétère (en moyenne, dans 10-15% des situations ci-
dessus), authentifiant la prédisposition
- soit aucune anomalie particulière. Ceci ne permet pas d’exclure la
prédisposition et peut être expliqué par :
• Soit par les limites techniques laissant inexplorée une proportion non
négligeable du gène.
• Soit par l’implication d’un autre gène que ceux qui ont été étudiés.
• Soit par le simple fruit du hasard.
- soit un variant de signification inconnue : le lien entre la variation observée et
les risques de cancer ne peut être clairement établi.
Risques associés aux mutations constitutionnelles de BRCA1 ou BRCA2
Chez la femme, une mutation de BRCA1 confère un risque de cancer du sein
d’environ 50-60% et un risque de cancer de l’ovaire de 20 à 40%. Une mutation de
BRCA2 génère un risque équivalent de cancer du sein, mais un risque de cancer de
l’ovaire significativement inférieur, de l’ordre de 10 à 20%.
Les cancers du sein associés à BRCA1 sont préférentiellement « triple-négatifs »
(absence de récepteurs hormonaux, absence de surexpression de cerbB2), mais tous
4

les cancers triple-négatifs ne correspondent pas à une mutation constitutionnelle de
BRCA1.
Les cancers de l’ovaire sont préférentiellement une histologie séreuse. Il ne s’agit
pratiquement jamais de forme mucineuse. Les tumeurs germinales de l’ovaire ne font
pas partie du spectre BRCA, pas plus que les tumeurs borderline de l’ovaire.
Chez l’homme, un risque de cancer du sein existe notamment avec BRCA2 mais est
nettement plus faible (risque absolu de 2-4%). Un sur-risque de cancer de la
prostate de quelques pourcents est habituellement retenu.
Pour les deux sexes, un sur-risque de cancer du pancréas est également suspecté,
notamment pour une mutation de BRCA2.
Pour PALB2, seul le risque de cancer du sein a été estimé. Longtemps considéré
comme un gène de prédisposition modérée, suite à une analyse poolée, les risques
seraient assez proches de ceux de BRCA2, mais très influencé par l’histoire familiale.
Prise en charge des femmes porteuses de mutation BRCA1, BCRA2, PALB2
Prise en charge du risque de cancer du sein:
Il est recommandé de réaliser chez les personnes porteuses d’une mutation BRCA1
ou 2 :
- une surveillance clinique, dès l’âge de 25 ans, par palpation mammaire chez le
spécialiste 2 fois par an
- des examens d’imagerie : mammographie et échographie mammaire
annuelles dès l’âge de 30 ans. Les données récentes de la littérature
permettent d’ajouter la réalisation d’IRM mammaires systématiques. Il est
5
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%