Mortemousque_CI_2008..

CÔLON
Diagnostic des formes familiales
Isabelle MORTEMOUSQUE
Service de Génétique – TOURS
FFCD – 2/10/08 - ORLÉANS

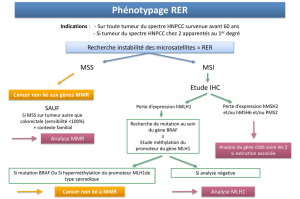
Syndrome de Lynch / HNPCC
Colon 82 ans
Colon 35 ans
Endomètre 47 ans Endomètre 38 ans
Colon 42 ans
Colon 31 ans

Présence de tous les critères Amsterdam II :
-
au moins 3 sujets atteints (spectre HNPCC)
- au moins 2 géné
rations successives
- au moins 1 cancer avant 50 ans
Syndrome de Lynch / HNPCC
Colon 82 ans
Colon 35 ans
Endomètre 47 ans
Colon 31 ans
Endomètre 38 ans
Colon 42 ans

Amsterdam II
VPP Sensibilité / détection
porteurs mutations MMR
60% 40%
CRITÈRES
- Pénétrance incomplète
Risque cumulé de cancer dans
les familles avec mutations
MMR identifiées.
Vasen J Med Genet, 2008
4-7 %Cancer intestin grêle 2 %Cancer voies biliaires 1-4 %Tumeur cérébrale 1-12 %Cancer tractus urinaire 2-13 %Cancer gastrique 3-13 %Cancer ovaire 27-71%Cancer endomètre 24-52 %CCR femme 28-75 %CCR homme

Amsterdam II
VPP Sensibilité / détection
porteurs mutations MMR
60% 40%
CRITÈRES
- Pénétrance incomplète
- Expressivité variable
Colon 82 ans
Colon 35 ans
Endomètre 47 ans Endomètre 38 ans
Colon 42 ans
!
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
1
/
27
100%