Semaines du 16 au 28 novembre

Semaines du 10 décembre au 21 décembre 2012
Programme des colles de chimie
- Spé PC
Semaine du 10 au 14 décembre
Révisions
Chapitres B.4, B.4 bis : Aldéhydes et cétones
- Réactivité en chimie organique : revoir dans le détail
−le chapitre sur la réactivité des organomagnésiens mixtes
−le chapitre sur la réactivité de la liaison C-O
−le chapitre sur la réactivité de la liaison C-N
−la réaction d'ozonolyse dans le chapitre sur la réactivité de la liaison C=C
Nouveautés
Fin du Chapitre B.4 bis : Réactivité liée à la mobilité de l’atome
d'hydrogène porté par l'atome de carbone en
α
du groupement C=O
• Généralisation : Obtention d’un carbanion en α d’un groupement Π-attracteur
- Savoir proposer des exemples de molécules comportant des atomes H acides sur un
atome C en α d’un groupement Π-attracteur, en plus des aldéhydes et cétones !
- Connaître l’acidité particulière des atomes H sur un atome C en α de deux groupements
Π-attracteurs (cas des β-dicétones, des β-diesters)
Chapitre B.4 ter : Réactivité des aldéhydes et cétones conjugués
• Connaître les termes de : aldéhydes et cétones conjugués ; composés carbonylés α, β
insaturés ; énones
• Connaître les caractéristiques spectroscopiques (IR) des aldéhydes et cétones
conjugués ; savoir citer des méthodes de préparation de ces composés
• Savoir donner une approche orbitalaire de la réactivité des énones (l’exemple de
l’acroléine a été vu en cours) ; connaître les termes d’addition 1,2 et addition 1,4
• Applications :
- connaître la différence de réactivité entre un organolithien, un organomagnésien mixte,
un organocuprate lithié
- connaître l’addition de Michael
1

Semaine du 17 au 21 décembre
Même programme que la semaine du 10 au 14 décembre (y compris
les révisions) +
Révisions de première année : Réactivité en chimie organique :
revoir dans le détail le chapitre sur la réactivité de la liaison C-X
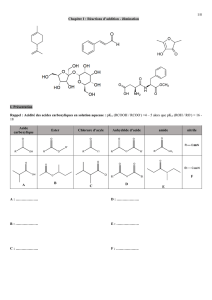
Nouveautés : Chapitre B.5 : Acides carboxyliques et dérivés
• Connaître la nomenclature des acides carboxyliques et de ses dérivés (chlorure
d’acyle, anhydride d’acide, amide, ester, nitrile)
• Connaître la réactivité relative des dérivés d’acide vis-à-vis d’un nucléophile
• Connaître le mécanisme d’addition-élimination ; savoir l’écrire dans le cadre des
réactions citées ci-dessous
• Savoir comment on synthétise un chlorure d’acyle (à partir d’un acide
carboxylique), un anhydride d’acide (à partir d’un chlorure d’acyle), un nitrile (à
partir d’un halogénalcane)
Liste des réactions à connaître (savoir écrire le bilan ; savoir les reconnaître dans
une séquence de réactions ; savoir écrire le mécanisme) :
• Synthèse d’un ester :
- à partir d’un acide carboxylique et d’un alcool
- à partir d’un chlorure d’acyle (ou d'un anhydride d'acide) et d’un alcool
- par transestérification
• Synthèse d’un amide à partir d’un chlorure d’acyle (ou d’un acide carboxylique)
• Hydrolyse d’un chlorure d’acyle (ou d’un anhydride d’acide) ; hydrolyse basique
d’un ester (saponification)
• Hydrolyse d’un amide et hydrolyse d’un nitrile [pour ces deux dernières
hydrolyses, le mécanisme est hors programme]
• Réduction d’un ester en alcool primaire par LiAlH4
• Synthèse malonique
Remarque : Révisions personnelles du programme de PCSI concernant les
dérivés d'acide : addition nucléophile d’un organomagnésien mixte sur un ester, un
chlorure d’acyle, un anhydride d’acide, un nitrile ; elles doivent être parfaitement
maîtrisées (le produit de la réaction doit pouvoir être trouvé sans refaire le
mécanisme).
2
1
/
2
100%