29/10/15 POUILLY Nakya L2 CR : Juliette Phélip TSSIB Pr F

TISSU SANGUIN ET SYSTEME IMMUNITAIRE - Le Complexe Majeur d'Histocompatibilité
29/10/15
POUILLY Nakya L2
CR : Juliette Phélip
TSSIB
Pr F.VELY
12 pages
Le Complexe Majeur d'Histocompatibilité (CMH)
(ouvrage de référence en immunologie : immunobilogy Janeway & Travers)
A.Généralités
I.Définitions
Le système immunitaire est un système complexe qui se doit de différencier le soi du non soi (et notamment le
non-soi dangereux comme les éléments pathogènes du non-soi commensale comme les bactéries intestinales).
Le complexe majeur d'histocompatibilité CMH est une dénomination valable pour toutes les espèces, il est
nommé plus spécifiquement HLA (Human Leukocyte Antigen) pour l'homme.
Nous ne sommes pas égaux face à la maladie, chaque personne réagira différemment et cela est régulé en
grande partie par un set de gènes (HLA) dont on va hériter de nos parents.
Cette inégalité est due au fait que le CMH se définit comme un ensemble de gènes très polymorphes qui
codent pour des molécules qui sont des marqueurs du soi : glycoprotéines (superfamille des
Immunoglobulines Ig, c'est à dire une molécule ancrée dans la membrane et qui présente des domaines
1/12
Plan :
A.Généralités
I. Définitions
II. Des ligands pour le TCR
III. Les molécules du CMH
B. Aspects génétiques
I. Quelques rappels de génétique
II. L'organisation génomique
III. Structure des CMH I et II
IV. Contrôle génétique et régulation de la réponse immunitaire
V. Expression des molécules du CMH
C. Mode d'action
I. Les cellules présentatrices de l'antigène (CPA)
II. La dynamique de la réponse immunitaire
III. La mise en place des ligands pour le TCR
D. La famille des molécules du CMH
E. Applications biomédicales

TISSU SANGUIN ET SYSTEME IMMUNITAIRE - Le Complexe Majeur d'Histocompatibilité
extracellulaires semblables à ceux des Ig) et alloantigènes.
Cette mosaïque antigénique constitue la carte d'identité de l'individu. La transmission est dite « mendélienne ».
Ce complexe a un rôle essentiel dans le rejet de greffe et les réponses immunitaires.
Attention : les glycoprotéines appartiennent à la superfamille des Ig mais ce ne sont pas des Ig !
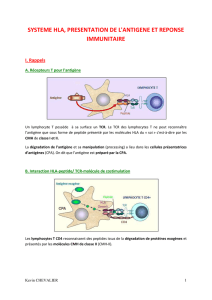
Un des rôle principal de ces molécules d'histocompatibilité va être de présenter des peptides aux lymphocytes T
(Qui ont des fonctions soit cytotoxiques lorsqu'ils sont sous forme CD8 soit auxiliaire sous forme CD4 qui vont
participer à la réponse immunitaire par la sécrétion de cytokine) .
II. Des ligands pour le TCR
Les LT ne sont capables de reconnaître l’antigène (AG) qu'en association avec
les molécules du CMH , on parle de « restriction par le CMH ».
Il existe donc une co-reconnaissance « CMH + AG » par les LT. On aboutit
alors à un complexe tri-moléculaire « CMH-AG-Récepteur T ».
Sans la présence d'un CMH, la réponse immunitaire adaptative est inefficace.
III. Les molécules du CMH
Les molécules du CMH se divisent en 3 classes :
•Les molécules du CMH de classe I sont exprimées sur toutes les cellules nucléées ce sont donc
des marqueurs du soi. Ces molécules vont êtres importantes pour contrôler le rejet de greffe
(dissociation entre informations du soi/non soi et danger/non danger). Les cellules de classe I
seront capables de présenter des peptides aux lymphocytes cytotoxiques (CD8) .
•Les molécules du CMH de classe II sont restreintes aux cellules présentatrices d'antigènes
(cellules dendritiques, LT et macrophages ; ces cellules vont être capable de prendre en charge
un antigène, de le présenter sous dorme de peptides aux LT CD4 ) et elles participent aux
coopérations cellulaires.
•Les molécules du CMH de classe III existent sous forme soluble dans le plasma, ce sont des
protéines du complément.
B.Aspects génétiques
I.Rappels de génétique
Le premier degré de diversité est un système multigénique. L'ensemble des gènes codant pour les CMH se
trouvent sur le bras court du chromosome 6. Chaque classe est codée par plusieurs gènes.
Ainsi on va s'intéresser à :
- 3 gènes HLA de classe I : HLA-A, HLA-B, HLA-C
- 3 gènes HLA de classe II : DP, DQ, DR
2/12

TISSU SANGUIN ET SYSTEME IMMUNITAIRE - Le Complexe Majeur d'Histocompatibilité
HLA classe I au niveau du chromosome 6 ne possède qu'une chaine tandis que HLA classe II en possède deux,
une alpha et une bêta (c'est pourquoi on observe deux segments géniques).
Quelques rappels de génétiques :
Locus : Position géographique sur un chromosome où se trouve un gène ou un groupe de gènes. Par exemple
ici le locus HLA classe I est localisé sur le bras court du chromosome 6
Allèle : Gène occupant un même locus avec une différence de quelques nucléotides et ayant des effets
différents sur un même caractère.
Haplotype : combinaison de gènes différents sur un même chromosome. On possède donc un haplotype
maternel et un haplotype paternel.
II.L'organisation génomique
Polymorphisme génétique multi-allélique
Pour chaque locus il existe de nombreux allèles (parfois plusieurs centaines) ayant des effets différents sur un
même caractère. Chaque individu est hétérozygote pour la plupart de ses gènes HLA de classe I et de classe II.
Cette caractéristique rend chaque individu quasiment unique.
Polymorphisme de la protéine correspondante (allotype HLA)
Chaque allèle code pour une protéine caractérisée par un ou plusieurs acides aminés variants comparée aux
protéines codées par d'autres allèles. Ces quelques acides aminés qui diffèrent vont conférer des propriétés
différentes à chaque personne en terme de défense immunitaire.
Codominance et transmission en bloc
-Codominance : phénotype = génotype (c'est à dire que si un individu possède un gène il possédera également
la protéine correspondante)
-Transmission en bloc : Comme les gènes sont localisés très près géographiquement, c'est tout le bloc qui est
transmis. Il y a donc très peu de crossing-over.
3/12

TISSU SANGUIN ET SYSTEME IMMUNITAIRE - Le Complexe Majeur d'Histocompatibilité
Le nombre d'allèles décrit chez l'homme à ce jour pour chacun des locus HLA classe I (728 allèles décrites à ce
jour pour HLA-B, 210 allèles HLA-C et 414 allèles HLA-A) est extrêmement important.
Il y a deux segment géniques pour les molécules DP, DQ et DR, La diversité pour HLA II est essentiellement
portée par la chaine bêta qui a beaucoup plus de polymorphisme que la chaine alpha.
Le polymorphisme est beaucoup plus important pour les classes I que pour les classes II.
Nomenclature des molécules HLA (pas à savoir) : Il y a le nom du gène HLA-A, suivi des numéros de la
famille allélique 02 et de l'allèle dans cette famille.
Ainsi l'organisation génomique se base sur deux systèmes :
– système multigénique
– système multi-allélique lié au grand nombre d'haplotypes
Pour chaque locus il existe 10 à 100 gènes ayant des effets différents sur un même caractère. Pour chaque locus,
il existe entre 3 et 72 allèles différents. Et chaque allèle aura des propriétés différentes de celles de son voisin.
Chaque individu est hétérozygote sur chaque locus HLA, par exemple si je suis HLA-A2 sur mon chromosome
paternel j'ai peu de chance d'être HLA-A2 sur mon chromosome maternel.
Il va être excessivement difficile de retrouver dans la population une personne qui va présenter sur tous les loci
exactement les mêmes allèles HLA que soi. Un grand nombre d'individus sont hétérozygotes pour les HLA de
classe I et II ce qui enrichit la réponse immunitaire. Cette caractéristique rend donc chaque individu quasiment
unique car il est quasiment impossible de trouver les 6 mêmes allèles pour HLA chez 2 individus différents sauf
dans une même famille.
4/12

TISSU SANGUIN ET SYSTEME IMMUNITAIRE - Le Complexe Majeur d'Histocompatibilité
Le polymorphisme HLA :
Un enfant est né d’un père dont les deux haplotypes HLA de classe I sont: A2/B27/Cw3 et A2/B54/Cw3 et
d’une mère dont les deux haplotypes HLA de classe I sont: A2/B13/Cw3 et A3/B27/Cw4.
1.Quel est le nombre maximal de molécules HLA classe I différentes que l’on peut trouver à la surface
de cellules nucléées d’un individu?
Quels sont les haplotypes possibles pour cet enfant ?
J'ai deux chromosomes et sur chaque chromosome j'ai 3 loci HLA classe I (A, B et C). Si tous les allèles sont
différents j'ai 6 molécules HLA classe I différentes à la surface des cellules nucléées. Il est possible d'en avoir
moins si le sujet est homozygote pour certains locus (c'est le cas ici pour le père qui a 2 A2 et 2 Cw3).
L'enfant peut avoir 4 haplotype différents.
2.Chez quel membre de la famille ai-je le plus de chance de trouver un donneur HLA identique pour cet
enfant?
Si je choisis le père ou la mère, ils ne pourront donner qu'un des deux haplotypes identiques puisque j’hérite
d'un chromosome paternel et d'un chromosome maternel.
Le plus compatible ne peut être qu'un frère ou une soeur si celui-ci a pris le même haplotype du père avec le
même haplotype de la mère. Plus il y a de frères et soeurs plus j'ai de chances de trouver un donneur.
5/12
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%