Voyage dans le monde des cellules souches…

25/11/2013
2013-11-19-Cellules-souches.doc 1 / 8
Voyage dans le monde des cellules souches…
Voyage dans le monde des cellules souches…Voyage dans le monde des cellules souches…
Voyage dans le monde des cellules souches…
INSERM 972 – Villejuif France.
« Les cellules souches, de leurs niches à leurs applications thérapeutiques »
par Madame Marie-Caroline Le Bousse-Kerdilès,
Directeur de recherche à l’INSERM
1
Sommaire
Voyage dans le monde des cellules souches…........................................................................................................................... 1
I. Définition des cellules souches :....................................................................................................................................... 1
A. D’où vient le terme « cellule souche » ?:................................................................................................................ 1
B. Définition d’une cellule :........................................................................................................................................ 1
C. Qu’entend t-on aujourd’hui par cellules souches ?:................................................................................................ 2
II. Différents types de cellules souches : ..........................................................................................................................2
III. Des cellules souches tout au long de la vie :................................................................................................................ 2
IV. Les cellules souches embryonnaires :.......................................................................................................................... 2
A. Comment peut-on les obtenir ?:.............................................................................................................................. 3
B. Transfert nucléaire (clonage) :................................................................................................................................ 3
C. Lignées utilisées en France :................................................................................................................................... 4
D. Intérêt en recherche et pharmacologie : .................................................................................................................. 4
E. Les cellules souches, avantages / inconvénients :........................................................................................................5
V. Les cellules souches adultes : ...................................................................................................................................... 6
VI. Les cellules souches induites, des cellules embryonnaires à façon, obtenues à partir de cellules souches adultes :.... 7
La décennie qui vient de s’écouler est connue comme une révolution tellement les dernières
découvertes dans l’étude des cellules souches, ont été déterminantes. En effet, l’importance des
cellules souches (CS) pour la régénération tissulaire et leur mise en évidence récente dans les
mécanismes de cancérogenèse/leucémogenèse sont à la base de leur intérêt croissant en recherche
fondamentale et en thérapie cellulaire pour la médecine régénérative.
I. Définition des cellules souches :
A.
A.A.
A.
D’où vient le terme «
D’où vient le terme «D’où vient le terme «
D’où vient le terme «
cellule souche
cellule souchecellule souche
cellule souche
»
»»
»
?:
?:?:
?:
1868 : Terme utilisé par le biologiste allemand Ernest Hæckel pour définir
l’ancêtre unicellulaire des organismes multicellulaires, et pour nommer l’œuf
fertilisé à l’origine de toutes les cellules de l’organisme.
1885 : Ultérieurement emprunté par le zoologiste Auguste Weismann, pour
identifier une cellule de l’embryon capable de donner naissance à des cellules
plus spécialisées.
1905 : Utilisé par l’hématologiste Arthur Pappenheim pour nommer la cellule à l’origine des cellules
du sang. La notion de cellule souche hématopoïétique (CSH) était née…
B.
B.B.
B.
Définition d’une cellule
Définition d’une celluleDéfinition d’une cellule
Définition d’une cellule
:
::
:
Le mot cellule vient de « cellula », qui signifie « petite chambre »
en latin. C’est l’unité de base des êtres vivants ; sa taille est de quelques
centièmes de millimètres et il y a environ 10
14
(100 billions) de cellules
dans un individu. Elle est composée d’un noyau qui renferme la majorité de
l’information génétique. Ce noyau est entouré d’un cytoplasme dans lequel
se déroulent la plupart des réactions chimiques nécessaires à la vie.
1
Institut national de la santé et de la recherche médicale - 101, rue de Tolbiac - 75654 Paris Cedex 13

25/11/2013
2013-11-19-Cellules-souches.doc 2 / 8
C.
C.C.
C.
Qu’entend t
Qu’entend tQu’entend t
Qu’entend t-
--
-on aujourd’hui par cellules souches
on aujourd’hui par cellules soucheson aujourd’hui par cellules souches
on aujourd’hui par cellules souches
?:
?:?:
?:
Les cellules souches sont des cellules indifférenciées qui assurent le renouvellement des
cellules d’un individu tout au long de sa vie. Elles ont la capacité de s’auto-renouveler, c'est-à-dire de
donner naissance à des cellules filles quasiment identiques à elles-mêmes, mais aussi de produire des
cellules différenciées (dites spécialisées), par divisions successives.
Chez un individu, les tissus peuvent être endommagés par les incidents de la vie. De plus, les
cellules de l’organisme vieillissent ; elles ont donc besoin d’être renouvelées pour que l’individu garde
intact l’intégrité de son organisme tout au long de sa vie. C’est le rôle des cellules souches.
II. Différents types de cellules souches :
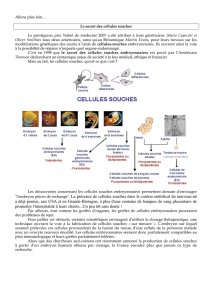
On distingue quatre types de cellules souches :
- Les cellules souches Totipotentes : elles donnent naissance à toutes les
cellules à l’origine d’un individu ainsi qu’aux cellules extra-embryonnaires
(ex : l’œuf fécondé).
- Les cellules souches Pluripotentes : elles donnent naissance aux cellules de
tous les types de tissus mais ne sont plus capables de donner naissance aux
cellules extra-embryonnaires (ex : cellules souches embryonnaires).
- Les cellules souches Multipotentes : elles donnent naissance à différents types
de cellules différenciées/spécialisées (ex : les cellules souches hématopoïétiques
2
).
- Les cellules souches Unipotentes : elles donnent naissance à un seul type
cellulaire tout en conservant leur capacité d’autorenouvellement
(ex : kératinocytes
3
).
III. Des cellules souches tout au long de la vie :
On peut distinguer
deux grands types de
cellules souches :
Les cellules
souches embryonnaires qui
vont constituer l’embryon et
les cellules souches adultes
qui vont assurer le
développement de l’individu
jusqu’à l’age adulte et le
maintien de l’intégrité de
l’organisme.
IV. Les cellules souches embryonnaires :
On les trouve dans l’œuf fécondé. Jusqu’au 4
ème
jour après la fécondation, chacune de ces
cellules pourrait donner naissance à un embryon car elles sont totipotentes.
À partir du cinquième jour, il se forme dans le blastocyste un bourgeonnement cellulaire
contenant des cellules souches pluripotentes qui, quand elles sont isolées de ce blastocyste, ne peuvent
plus donner naissance à un embryon ; en effet, elles ne peuvent pas former les annexes extra-
embryonnaires.
2
Hématopoïétique : qui concerne la formation des cellules du sang. Celles-ci sont principalement formées dans
la moelle osseuse chez l’homme adulte.
3
Kératinocytes : cellules constituant 90% de la couche superficielle de la peau, et des cheveux, ongles, etc.

25/11/2013
2013-11-19-Cellules-souches.doc 3 / 8
C’est à partir de ces cellules que sont obtenues les cellules souches embryonnaires.
Les cellules souches
embryonnaires, isolées de la masse
interne du blastocyste, sont pluripotentes,
c’est à dire qu’elles sont capables de
générer tous les tissus de l’embryon:
Mésoderme (muscle, sang…),
Endoderme (tube digestif, poumons…),
Ectoderme (peau, tissu nerveux…).
A.
A.A.
A.
Comment peut
Comment peutComment peut
Comment peut-
--
-on les obtenir
on les obteniron les obtenir
on les obtenir
?:
?:?:
?:
Pour que la recherche progresse, il faut que les chercheurs puissent travailler sur des embryons
et sur les cellules embryonnaires. Tout ceci est très encadré par la loi
et par des comités d’éthique.
On peut obtenir des cellules embryonnaires de différentes
façons, lors d’une fécondation in vitro (FIV), d’un diagnostic
préimplantatoire (DPI) ou par clonage.
Lors d’un projet parental par fécondation in vitro (FIV), tous
les embryons ne sont pas utilisés. On en congèle certains pour qu’ils
puissent éventuellement être réutilisés en cas d’échec de la FIV.
Lorsque le projet a abouti, il reste parfois des embryons surnuméraires qui pourront être utilisés pour
la recherche si les parents le souhaitent et en donnent l’autorisation.
Toujours lors d’un projet parental, si, dans le cadre d’un DPI
pour recherche d’une anomalie génique (par exemple une mutation)
portée par les parents, l’œuf fécondé présente cette anomalie, le projet
de maternité est arrêté. L’embryon porteur de l’anomalie est soit
détruit, soit donné à la recherche pour étudier le rôle de la mutation
dans la pathogenèse de la maladie qu’elle engendre.
B.
B.B.
B.
Transfert nucléaire (clonage)
Transfert nucléaire (clonage)Transfert nucléaire (clonage)
Transfert nucléaire (clonage)
:
::
:
Le clonage reproductif humain est interdit en France.
On peut cependant pratiquer ce que l’on appelle un clonage thérapeutique ou à visées
thérapeutiques par transfert nucléaire.
Principe : on enlève le noyau d’un ovocyte (ovule
non fécondé); il reste alors le cytoplasme. Si, par exemple,
on prend le noyau d’une cellule différenciée de peau que l’on
place dans le cytoplasme de l’ovocyte énucléée, on obtient
un clone de cellules souches contenant le patrimoine
génétique de l’individu qui a fourni le fibroblaste de peau.
Entre clonage thérapeutique et clonage reproductif, seule la finalité change. Cependant le
procédé soulève de nombreuses questions :
Source des ovocytes ?
Création d’un embryon sans projet
parental ?
Statut moral d’un tel embryon ?
Mesure de l’intérêt médical ?
cytoplasme
Bourgeonnement

25/11/2013
2013-11-19-Cellules-souches.doc 4 / 8
Le clonage reproductif humain est interdit en France, mais le clonage thérapeutique est
possible dans et avec certaines conditions. Les cellules souches pluripotentes isolées du blastocyste
obtenu par clonage
thérapeutique ne
peuvent pas donner
naissance à un
embryon viable, mais
peuvent produire des
cellules des différents
tissus humains,
conformément à la loi.
C.
C.C.
C.
Lignées utilisées en France
Lignées utilisées en FranceLignées utilisées en France
Lignées utilisées en France
:
::
:
Initialement, les chercheurs français
travaillaient sur des lignées de cellules souches
embryonnaires (dites cellules ES pour la
terminologie anglaise « Embryonic Stem cells »)
obtenues à l’étranger. Peu à peu, la loi a autorisé
les laboratoires français à dériver des lignées de
cellules ES. Compte tenu du régime d’interdiction
de travailler sur l’embryon et les cellules
embryonnaires, il fallait monter de lourds dossiers
de demande d’autorisation pour pouvoir le faire.
Maintenant (depuis le mois d’août 2013), la législation s’est assouplie puisque nous sommes
passés à un régime d’autorisation encadrée. Il faut cependant toujours exposer l’objectif de la
recherche, dire de quelle façon on compte y arriver et expliquer qu’on ne dispose d’aucune autre
solution alternative pour atteindre cet objectif.
Cadre juridique français :
- Lois de bioéthique de 2004 et 2011 : la recherche sur l’embryon est interdite en France, mais
des dérogations sont autorisées.
- Loi de bioéthique du 6 août 2013 tend à modifier la loi du 7 juillet 2011 en autorisant sous
certaines conditions la recherche sur l’embryon et les cellules souches embryonnaires.
Passage d’un régime d’interdiction de la recherche sur l’embryon et des cellules
souches embryonnaires avec dérogations, à un régime d’autorisation encadrée.
Énumération des quatre conditions cumulatives nécessaires à l’octroi d’une
autorisation de recherche : la pertinence scientifique, la finalité médicale de la
recherche, l’absence de techniques alternatives, et le respect des principes éthiques par
le protocole.
Ce qui est formellement interdit :
o Créer des embryons spécifiquement pour la recherche
o Créer des embryons par transfert nucléaire
o Modifier le génome des embryons donnés à la recherche
o Implanter dans un utérus des embryons donnés à la recherche
Tous les pays n’ont pas la même réglementation, en particulier les pays du nord de l’Europe,
l’Inde et la Chine sont plus libéraux.
En France, on a certes pris du retard sur ces pays, mais les limitations et les contrôles imposés
par la législation française sont essentiels au bon développement des recherches sur les cellules
embryonnaires.
D.
D.D.
D.
Intérêt en recherche et pharmacologie
Intérêt en recherche et pharmacologieIntérêt en recherche et pharmacologie
Intérêt en recherche et pharmacologie
:
::
:
Compréhension du vivant :
o Étude des gènes du développement et de leurs fonctions

25/11/2013
2013-11-19-Cellules-souches.doc 5 / 8
o Compréhension des mécanismes de prolifération et de différenciation
o Comment une cellule donne naissance à un tissu
Recherche préclinique et pharmaceutique :
o Test de l’efficacité de nouveaux médicaments sur des cellules humaines qui
peuvent être multipliées facilement (modèles plus proches de la situation in vivo,
limitation de l’utilisation des animaux …)
Utilité en médecine régénératrice :
Grâce aux cellules embryonnaires, on peut obtenir « tous » les types cellulaires en nombre
illimité afin de les utiliser pour la greffe.
Plus de 100 autorisations ont déjà été accordées en France
pour travailler sur les cellules souches embryonnaires humaines et
plusieurs protocoles utilisent ces cellules embryonnaires dans des
modèles animaux (accidents vasculaires cérébraux, maladie
génétique conduisant à la destruction des neurones de certaines
régions du cerveau…).
Cependant, la recherche sur les cellules embryonnaires
humaines n’est qu’au début de ses découvertes ; on ne sait pas
encore tout faire… Certaines avancées thérapeutiques ont déjà été
observées chez la souris et plusieurs essais cliniques sont en cours chez l’homme, en particulier dans
le domaine des greffes de cellules neurales pour réparer des cellules nerveuses lésées mais également
de la rétine pour lutter contre les dystrophies maculaires liées à l’âge.
E.
E.E.
E.
Les cel
Les celLes cel
Les cellules souches, avantages / inconvénients
lules souches, avantages / inconvénientslules souches, avantages / inconvénients
lules souches, avantages / inconvénients
:
::
:
Des avantages majeurs :
On peut obtenir un nombre illimité de cellules embryonnaires (auto-renouvellement). Ce sont
des cellules embryonnaires, donc « neuves ».
Ces cellules sont pluripotentes, elles peuvent se différencier en de multiples cellules
spécialisées différentes que l’on pourra sélectionner selon le tissu à réparer. Il se constitue
actuellement des banques internationales de cellules souches.
Mais tout cela ne va pas sans poser des problèmes et soulever des questions :
- Tumorigénicité : il faut contrôler les cellules créées et vérifier qu’elles ne dégénèrent pas en
tumeurs, qu’elles restent saines après culture.
- Instabilité génétique dans la culture in vitro.
- Immunogénicité : il y a un risque de rejet de greffe ; il faut résoudre les problèmes liés à
l’incompatibilité immunologique.
- Éthique : accès aux embryons, statut de l’embryon, destruction d’embryon.
 6
6
 7
7
 8
8
1
/
8
100%