16_1S_1A_dst2

http://lewebpedagogique.com/bouchaud 16_1S_1A_dst2.docx
1
DST Thème 1A « Génotype, phénotype, mutations… » 2
1. Questions de cours.
Durée conseillée : 5 minutes.
3 points.
Définir génotype, protéine, mutation.
2. L’origine de la phénylcétonurie.
D’après SVT 1S Belin 2001, modifié 2016
Durée conseillée : 20 minutes.
8 points.
La phénylcétonurie est une maladie affectant un nouveau né sur 17 000 en France, et responsable d’une
altération mentale progressive importante en l’absence de traitement approprié. Certains sujets atteints sont
caractérisés par la pâleur de leur visage et la couleur claire de leurs yeux et de leurs cheveux.
Document1. Les voies de la transformation de la phénylalanine.
La phénylalanine est un acide aminé d’origine alimentaire (l’organisme est incapable de le synthétiser
seul), présent en grande quantité dans les protéines animales. Dans les cellules du foie, il est le point de départ
des réactions suivantes
La mélanine est un pigment noir, présent en plus ou moins grande quantité dans les cellules de la peau,
de l’iris de l’œil et de la base du cheveu et du poil.
L’accumulation de phénylalanine et d’acide phénylpyruvique dans le sang est très toxique dans les
neurones non matures du cortex cérébral avant 6 ans.
Si on trempe les racines des cheveux d’un individu atteint de phénylcétonurie dans de la tyrosine, les
cheveux se colorent en brun.
Doc. 2. Dosage de la phénylalanine et de ses dérivés dans le plasma et l’urine de différents individus.
Plasma
Urine
Substances
Individu normal
Individu atteint
Individu normal
Individu atteint
Phénylalanine (mg pour 100 mL)
1 à 2
15 à 63
30
300 à 1000
Acide phénylpyruvique (mg pour 100 mL)
0
0,3 à 1,8
0
300 à 2000
Doc.3. Les causes de la phénylcétonurie.
Les progrès de la biologie moléculaire ont permis de découvrir les causes de la phénylcétonurie. Dans
63% des familles touchées, cette anomalie correspond à une différence dans une protéine appelée PAH,
comportant 452 acides aminés, dont la synthèse est contrôlée par un gène, pouvant présenter différents allèles.
La protéine PAH est une enzyme : elle permet donc une réaction chimique.
Doc. 4. Extraits des séquences des allèles sain et morbide du gène concerné ; le reste est identique.
Allèle d’individu sain : ACAATACCTCGGCCC Allèle d’un individu malade : ACAATACCTTGGCCC
TGTTATGGAGCCGGG TGTTATGGAACCGGG
Questions.
1. Réaliser un schéma de synthèse complet reconstituant les étapes qui, du gène, conduisent aux différentes
échelles des phénotypes phénylcétonurique et sain. Y inclure la présence éventuelle d’un facteur
environnemental.
2. Proposer un traitement envisageable pour cette maladie.
Note : aucune utilisation du code génétique en annexe n’est demandée.
PAH

http://lewebpedagogique.com/bouchaud 16_1S_1A_dst2.docx
2
3. L’élaboration des protéines du lait.
D’après SVT 1S Hatier 2001, modifié 2016
Durée conseillée : 30 minutes.
9 points.
Le lait est sécrété au niveau des glandes mammaires par des cellules spécialisées regroupées en acinus
autour d’un canal, le canal galactophore, qui permettra par la suite l’évacuation du lait. On veut ici étudier
quelques aspects de la formation du lait.
Document 1. Coupe schématique d’un acinus.
Document 2. Séquence d’une partie du gène codant la caséine du lait chez la brebis et la vache.
Les caséines, les protéines les plus abondantes du lait, sont codées par des gènes dont on connaît la
séquence de nucléotides chez la brebis et chez la vache.
Séquence de nucléotides d’une portion du gène
Brebis (brin codant = brin non transcrit)
GCC
CTT
GTT
CTT
AAC
TTA
CAA
CAT
CCA
Vache (brin codant = brin non transcrit)
TCC
CTC
AAT
CTT
AAT
TTG
GGA
CAG
CCT
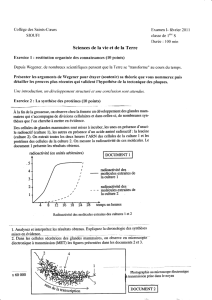
Document 3. Evolution de la radioactivité dans une cellule de l’acinus, et la lumière de l’acinus.
Afin de comprendre comment les caséines sont
élaborées, des fragments de tissus de glandes mammaires
de brebis sont placés pendant trois minutes sur un milieu
de culture contenant un acide aminé radioactif (donc
repérable) entrant dans la composition de la caséine, la
leucine, puis sur un milieu non radioactif.
L’acide aminé radioactif est capable d’entrer
dans le milieu intracellulaire.
Des fragments de tissus sont prélevés 3, 15, 25,
45 et 60 minutes après que les cellules aient été placées
sur le milieu non radioactif. Le graphique traduit
l’évolution de la radioactivité dans une des cellules.
Questions.
1. En utilisant le tableau du code génétique (en annexe), écrire la séquence des acides aminés de la caséine du
lait chez la Brebis et chez la Vache.
Comparer les deux séquences d’acides aminés et montrer la propriété du code génétique mise en évidence.
2. Analyser l’évolution de la radioactivité dans une cellule de glande mammaire après qu’elle ait été cultivée
dans un milieu contenant de la leucine radioactive.
3. A l’aide de vos connaissances, construire un schéma fonctionnel expliquant les phénomènes observés dans le
document 3. Doivent y figurer les termes clé de : transcription – traduction – exportation.
Annexe. Le code génétique (acides aminés et abréviations conventionnelles).

http://lewebpedagogique.com/bouchaud 16_1S_1A_dst2.docx
3
Correction
1. Questions de cours.
Durée conseillée : 5 minutes.
3 points.
Génotype : ensemble des allèles portés par un individu
Protéine : molécule constituée d’une séquence d’AA (synthétisée à partir de gène(s).
Mutation : modification dans la séquence de NT de l’ADN.
2. L’origine de la phénylcétonurie.
Durée conseillée : 20 minutes.
8 points.
Sain
Malade
Génotype
0,5 allèle / local° mutation
0,5 « substitution »
Au moins un allèle
« sain »
Couple GC en position 10
Au moins un allèle « dysfonctionnel »
Couple TA en position 10
Substitution
[Moléculaire]
0,5 modif° séq AA
0,5 F° / dysf°
Séquence normale 452 AA
de PAH (enzyme
fonctionnelle)
Séquence ??? PAH déficiente (1AA ?).
PAH inactive
[Cellulaire]
2
- Synthèse de tyrosine à
partir de la phénylalanine
dans les hépatocytes
- Synthèse de mélanine.
- Pas d’accumulation
d’acide phénylpyruvique
- Pas de synthèse de tyrosine à partir de la
phénylalanine dans les hépatocytes.
- Pas de synthèse de mélanine.
- Accumulation d’acide phénylpyruvique toxique,
évacué dans le plasma et l’urine.
[Macroscopique]
2
- Pas de symptôme
- altération mentale progressive (accumulation).
- Pâleur du visage (mélanine).
- Couleur claire des yeux et des cheveux (mélanine).
Titre : 0,5
Précision sur le facteur environnemental : phénylalanine d’origine alimentaire (protéines animales) 0,5
Question 2. Il faut un régime sans phénylalanine pour éviter les symptômes (1).
3. L’élaboration des protéines du lait.
Durée conseillée : 30 minutes.
9 points.
1. En utilisant le tableau du code génétique (en annexe), écrire la séquence des acides aminés de la
caséine du lait chez la Brebis et chez la Vache.
Brebis (brin codant = brin non transcrit)
GCC
CTT
GTT
CTT
AAC
TTA
CAA
CAT
CCA
Séquence peptidique
Ala
Leu
Val
Leu
Asn
Leu
Gln
His
Pro
Vache (brin codant = brin non transcrit)
TCC
CTC
AAT
CTT
AAT
TTG
GGA
CAG
CCT
Séquence peptidique
Ser
Leu
Asn
Leu
Asn
Leu
Gly
Gln
Pro
2 points (-0,5 par erreur)
Comparer les deux séquences d’acides aminés et montrer la propriété du code génétique mise en évidence.
Sur les deux séquences comportant chacune 9AA, on constate 4 AA différents alors que 8 codons sont touchés
par au moins une mutation. Cela démontre la redondance du code génétique (code génétique dégénéré) : pour un
même AA, très souvent plusieurs codons sont possibles. (2)
Décrire l’évolution de la radioactivité dans une cellule de glande mammaire après qu’elle ait été cultivée dans
un milieu contenant de la leucine radioactive (document 3).
- Jamais de radioactivité dans le noyau : la leucine (AA) n’entre pas dans le noyau. (1)
- Radioactivité dans le cytoplasme, avec un pic à 25 min. La leucine est incorporée dans la caséine en cours de
synthèse dans le cytoplasme. C’est la traduction qui est visible ici. (1)
- La radioactivité augmente par la suite dans la lumière de l’acinus (milieu extracellulaire) avec un pic à 45 min.
La caséine est exportée en dehors de la cellule (milieu extracellulaire). (1)
A l’aide de vos connaissances, construire un schéma fonctionnel.
Voir la qualité du schéma, si c’est complet, et si c’est légendé et titré. 2 points.

http://lewebpedagogique.com/bouchaud 16_1S_1A_dst2.docx
4
1
/
4
100%