Hypertrophie ventriculaire gauche atypique révélatrice d`une cause

Quel est votre diagnostic ? Me
´decine et Sante
´Tropicales 2013 ; 23 : 390-393
Hypertrophie ventriculaire
gauche atypique révélatrice
d'une cause rare d'insuffisance
cardiaque chez un Comorien
Atypical left ventricular hypertrophy
revealing a rare cause of heart failure
in a man from the Comoros Islands
Cautela J.
1
, Massoure P.-L.
1
, Roche N.-C.
1
, Taix S.
2
,
Gil J.-M.
1
, Fourcade L.
1
1
Ho
ˆpital des arme
´es A.-Laveran, service de cardiologie, boulevard
Laveran, 13384 Marseille ce
´dex 13
2
Service d’anatomopathologie, boulevard Laveran, 13384 Marseille
L’apparition d’une insuffisance cardiaque aigue
¨chez un
patient hypertendu d’origine africaine est une situation
fre
´quente. Dans ce contexte, l’existence d’une hypertrophie
ventriculaire gauche (HVG) te
´moignant d’une cardiopathie
hypertensive est classique, d’autant que l’absence de de
´pistage
et donc de traitement pre
´coce est habituelle en Afrique [1].
Cependant,l’hypertensionarte
´rielle(HTA)n’estpas laseulecause
d’HVG. D’autres pathologies plus rares doivent e
ˆtre e
´voque
´es
devant des e
´le
´ments cliniques et paracliniques atypiques.
Observation
Un Comorien de 73 ans, n’ayant jamais quitte
´les Comores
auparavant, est hospitalise
´en urgence pour une premie
`re
pousse
´e d’insuffisance cardiaque globale se
´ve
`re, sans douleur
thoracique. Ses facteurs de risque cardiovasculaire e
´taient
limite
´sa
`l’a
ˆge, une HTA ne
´glige
´e et un diabe
`te de type II
insulinoreque
´rant. Il de
´crivait une dyspne
´e au moindre effort
d’aggravation progressive depuis deux mois, sans fie
`vre ni
contexte infectieux. L’examen retrouvait une pression arte
´rielle
a
`160/80 mmHg syme
´trique aux deux bras, des œde
`mes
bilate
´raux des membres infe
´rieurs de
´clives et prenant le godet,
remontant jusqu’a
`la racine des membres, et une turgescence
jugulaire spontane
´e avec reflux he
´patojugulaire. Il n’y avait pas
de souffle cardiaque. Il n’y avait pas d’anomalie a
`l’examen
pulmonaire, neurologique et oste
´oarticulaire, ni d’anomalie
cutane
´e ou muqueuse.
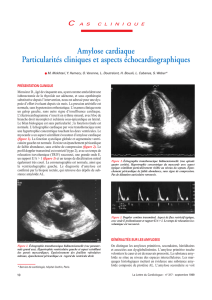
L’ECG mettait en e
´vidence un rythme sinusal sans trouble de
la conduction, sans onde Q pathologique ni trouble de la
repolarisation, mais avec un microvoltage dans les de
´rivations I,
II, III, vR, vL et vF (figure 1). La radiographie pulmonaire
montrait une surcharge alve
´olo-interstitielle bilate
´rale et une
cardiome
´galie. Sur le plan biologique, on notait une ane
´mie
normocytaire are
´ge
´ne
´rative a
`9,3 g/dL sans atteinte des autres
ligne
´es sanguines, une insuffisance re
´nale se
´ve
`re (clairance de
la cre
´atinine a
`30 mL/min), une prote
´inurie minime (0,21 g/
24 h), un taux d’he
´moglobine glyque
´ea
`6.9 % et une e
´le
´vation
du NT-pro-brain natriuretic peptide (NT-proB-NP) a
`3 989 ng/L
(N <300 ngL). La troponine-T et le bilan he
´patique e
´taient
normaux. La se
´rologie du virus de l’immunode
´ficience humaine
(VIH) e
´tait ne
´gative. L’e
´chocardiographie (figure 2A) retrouvait
une fonction systolique ventriculaire gauche normale (fraction
d’e
´jection : 65 %) avec une dilatation mode
´re
´e du massif atrial
et une HVG (masse ventriculaire gauche : 145 g/m
2
) pre
´domi-
nant sur le septum interventriculaire (SIV) mesure
´a
`15 mm en
te
´le
´diastole. On notait un aspect inhabituellement hypere
´cho-
ge
`ne, he
´te
´roge
`ne et « granite
´» du SIV (figure 2B). Le septum
interatrial e
´tait e
´paissi (8 mm d’e
´paisseur maximale [normale
<4 mm]). La fonction diastolique e
´tait anormale avec un profil
transmitral de type « pseudo-normal » (E/A = 1,2, E/E’ = 15) en
faveur d’une e
´le
´vation des pressions te
´le
´diastoliques du
ventricule gauche estime
´es a
`20 mmHg. Il y avait une e
´le
´vation
de la pression arte
´rielle pulmonaire systolique estime
´ea
`
55 mmHg a
`partir d’un flux d’insuffisance tricuspide (apre
`s
correction a
`partir de la pression atriale droite estime
´ea
`
10 mmHg). Il n’y avait pas d’anomalie des valves cardiaques ou
d’aspect e
´vocateur de fibrose endomyocardique. Enfin, il y avait
un e
´panchement pe
´ricardique de faible abondance (5 a
`7 mm)
en regard de la paroi poste
´rieure et de l’oreillette droite.
Figure 1. ECG mettant en e
´vidence un microvoltage dans les de
´rivations I, II, III, vR, vL, vF
Figure 1. ECG showing microvoltage in the I, II, III, vR, vL, and vF leads.
doi: 10.1684/mst.2013.0267
390 Pour citer cet article : Cautela J, Massoure PL, Roche NC, Taix S, Gil JM, Fourcade L. Hypertrophie ventriculaire gauche atypique re
´ve
´latrice d’une cause rare d’insuffisance
cardiaque chez un Comorien. Med Sante Trop 2013 ; 23 : 390-393. doi : 10.1684/mst.2013.0267
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Quel est votre diagnostic ? Re
´ponse page
suivante.
VG
OG
ABC
OD
VG
OG OG
OD
VG
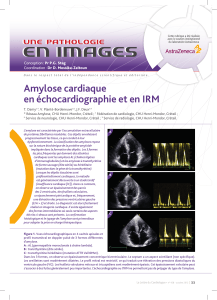
Figure 2. A,B) E
´chocardiographie A) Hypertrophie des parois du ventricule gauche (VG) en incidence parasternale grand axe B) Aspect scintillant (grande fle
`che) du
septum interventriculaire (SIV), dilatation des oreillettes droite (OD) et gauche (OG), e
´panchement pe
´ricardique minime en arrie
`re de l’OD (petite fle
`che) en incidence
apicale quatre cavite
´sC) IRM myocardique 10 minutes apre
`s injection de gadolinium rehaussement tardif pre
´dominant au niveau du SIV (grande fle
`che) et de l’apex du
VG (petite fle
`che)
Figure 2. A,B) Echocardiography A) Left ventricular wall hypertrophu (LV), parasternal long-axis plane B) Scintillating appearance (large arrow) of the interventricular
septum (IVS), dilatation of the right atrium (RA) and left atrium (LA), minimal pericardial effusion behind the RA (small arrow) on an apical four-chamber view C)
Myocardial MRI 10 minutes after injection of gadolinium delayed enhancement predominantly at level of the IVS (large arrow) and the LV apex (small arrow).
Ibis caroncule
´s, espe
`ce ende
´mique (monts Simiens, 3 900 m, E
´thiopie) #F Augey
Me
´decine et Sante
´Tropicales, Vol. 23, N84 - octobre-novembre-de
´cembre 2013 391
Une cause rare d’insuffisance cardiaque
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

L’amylose AL : cause rare
d’insuffisance cardiaque re
´ve
´le
´e
par une hypertrophie ventriculaire
gauche
Devant un tableau atypique n’e
´voquant pas une simple
cardiopathie hypertensive avec l’association d’une insuffisance
cardiaque diastolique se
´ve
`re, d’une HVG atypique pouvant
faire e
´voquer une cardiomyopathie restrictive, d’un e
´panche-
ment pe
´ricardique et d’un microvoltage a
`l’ECG, d’une
insuffisance re
´nale et d’une ane
´mie, l’hypothe
`se d’une maladie
de surcharge e
´tait souleve
´e. Une he
´mochromatose e
´tait e
´limine
´e
devant la normalite
´du bilan ferrique, une maladie de Wilson e
´tait
e
´carte
´e du fait la normalite
´de la cupre
´mie et de la cuprurie, et une
maladie de Fabry e
´tait exclue en raison de la normalite
´de
l’activite
´alphagalactosidase A. Une amylose cardiaque e
´tait
e
´voque
´e d’autant que des chaı
ˆnes le
´ge
`res d’immunoglobulines
lambda monoclonales e
´taient retrouve
´es a
`l’e
´lectrophore
`se des
prote
´ines se
´riques et urinaires. La pre
´sence de 18 % de
plasmocytes dysmorphiques au mye
´logramme confirmait l’exi-
stence d’un mye
´lome. La calce
´mie e
´tait normale et il n’y avait pas
de le
´sion osseuse. La biopsie des glandes salivaires s’est ave
´re
´e
normale. Le diagnostic d’amylose AL a finalement e
´te
´confirme
´
par une biopsie de la graisse sous-cutane
´e abdominale montrant
la pre
´sence d’une substance amyloı
¨de prenant la coloration par le
rouge Congo (figure 3).
Me
ˆme si l’aspect e
´chocardiographique e
´tait fortement
e
´vocateur, l’atteinte myocardique de type amyloı
¨de a e
´te
´
indirectement confirme
´e en imagerie par re
´sonance magne
´-
tique (IRM) cardiaque, retrouvant des plages de rehausse-
ment tardif (hypersignal myocardique 10 mn apre
`s injection de
gadolinium) au niveau des zones hypertrophiques, en
particulier au niveau du SIV (figure 2C). Il n’a pas e
´te
´re
´alise
´
de biopsie endomyocardique dans ce contexte.
Le diagnostic final est celui d’un mye
´lome a
`chaı
ˆnes le
´ge
`res
lambda complique
´d’une amylose syste
´mique AL lambda
re
´ve
´le
´e par une insuffisance cardiaque par cardiopathie
restrictive (amylose cardiaque). Un traitement par furose
´mide
ae
´te
´de
´bute
´, permettant la re
´gression des signes congestifs et la
stabilisation initiale du patient en l’absence de re
´hospitalisation
pour insuffisance cardiaque aigue
¨a
`trois mois. Paralle
`lement, une
chimiothe
´rapie associant melphalan et borte
´zomib a e
´te
´de
´bute
´e.
Discussion
L’amylose cardiaque est probablement largement sous-estime
´e
en Afrique, et son e
´pide
´miologie y reste mal connue [2].A
`notre
connaissance, ce cas de cardiopathie amyloı
¨de avec amylose AL
est le premier a
`e
ˆtre rapporte
´chez un patient originaire des
Comores. En Afrique, l’HTA, dont la pre
´valence peut atteindre
50 a
`60 % dans certaines re
´gions chez les sujets de plus de
65 ans, est une des causes les plus fre
´quentes d’insuffisance
cardiaque [1]. Une cardiopathie hypertensive est retrouve
´e dans
pre
`s de 50 % des cas d’insuffisance cardiaque en Afrique
subsaharienne [3]. Comme dans notre observation, la de
´cou-
verte d’une HVG dans un contexte d’insuffisance cardiaque a
`
fonction systolique pre
´serve
´e chez un Africain hypertendu est
attendue. De me
ˆme, l’association d’une insuffisance re
´nale dans
le cadre d’une ne
´phropathie hypertensive et/ou diabe
´tique est
e
´galement habituelle. Chez ce Comorien, la discordance entre
les donne
´es cliniques (HTA) et les donne
´es de l’ECG (micro-
voltage, la
`ou
`un aspect plus compatible avec l’HVG e
´tait
attendu), l’association d’un SIV hypere
´choge
`ne et d’un e
´pan-
chement pe
´ricardique, ainsi que l’existence d’une insuffisance
re
´nale ont motive
´la recherche d’une cardiopathie restrictive par
maladie de surcharge au-dela
`du diagnostic de simple cardiopa-
thie hypertensive initialement e
´voque
´. Une fibrose endomyo-
cardique, cause la plus fre
´quente de cardiomyopathie restrictive
en Afrique, a e
´te
´e
´carte
´e d’emble
´e par les examens d’imagerie.
Les maladies de surcharge sont une cause non exceptionnelle
d’insuffisance cardiaque avec des formes particulie
`res d’HVG,
associe
´es a
`des atteintes polyvisce
´rales. L’amylose est une des
causes les plus fre
´quentes de cardiopathie de surcharge avec
l’he
´mochromatose et la maladie de Fabry. Dans l’amylose, les
complications visce
´rales sont lie
´es au de
´po
ˆt insoluble de
prote
´ines fibrillaires (ou substance amyloı
¨de) au niveau du
rein, du cœur, du foie, du syste
`me nerveux pe
´riphe
´rique et des
vaisseaux. Si la biopsie des glandes salivaires et/ou celle de la
graisse cutane
´e abdominale sont facilement re
´alisables au lit du
patient, l’analyse histologique – qui seule permet le diagnostic
positif – n’est pas toujours disponible en Afrique. La biopsie
endomyocardique n’est pas indispensable pour porter le
diagnostic d’amylose cardiaque lorsque l’amylose a e
´te
´
prouve
´e histologiquement a
`partird’unautresitedepre
´-
le
`vement et que les donne
´es d’imagerie, incluant aujourd’hui
l’IRM cardiaque, sont concordantes [4].
AB
Figure 3. Biopsie de la graisse cutane
´e abdominale confirmant le diagnostic d’amylose. A) En coloration standard (HES), mise en e
´vidence d’une substance e
´osinophile,
extracellulaire et amorphe (fle
`che). B) Ce de
´po
ˆt colorable par le rouge Congo (fle
`che) correspond a
`de la substance amyloı
¨de.
Figure 3. Biopsy of abdominal cutaneous fat confirming the diagnosis of amyloidosis. A) Standard staining (HES), demonstration of an eosinophilic, extracellular,
amorphous substance (arrow). B) This Congo red-stainable deposit (arrow) corresponds to the amyloid substance.
392 Me
´decine et Sante
´Tropicales, Vol. 23, N84 - octobre-novembre-de
´cembre 2013
J. CAUTELA, ET AL.
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Il existe plusieurs types d’amylose, en fonction de la
prote
´ine pre
´curseur (vingt-huit prote
´ines amyloı
¨des sont
identifie
´es a
`ce jour). Les plus fre
´quentes sont :
–l’amylose AL, associe
´ea
`des chaı
ˆnes le
´ge
`res monoclonales,
–l’amylose AA, qui est la plus fre
´quente en Afrique (42 a
`66 %
des amyloses), associe
´ea
`une maladie inflammatoire, ne
´o-
plasique ou infectieuse chronique en particulier tuberculeuse
en Afrique,
–l’amylose he
´re
´ditaire a
`transthyre
´tine mute
´e,
–l’amylose se
´nile e
´galement associe
´ea
`un de
´po
ˆtde
transthyre
´tine non mute
´e[2].
Devant une gammapathie monoclonale a
`chaı
ˆnes le
´ge
`res, la
recherche d’une atteinte d’organe est syste
´matique. L’atteinte
cardiaque est retrouve
´e dans environ 60 % des amyloses AL [5].La
cardiopathie amyloı
¨de s’exprime le plus souvent par une HVG
associe
´a
`une dysfonction diastolique, e
´voluant vers une cardi-
opathie restrictive, des troubles du rythme atriaux et ventricu-
laires, et des anomalies de la conduction. Si la dysfonction
diastolique est constante et s’aggrave progressivement, une
dysfonction systolique ventriculaire gauche est absente dans
75 % des cas mais peut e
ˆtre pre
´sente dans les formes les plus
e
´volue
´es. Par ordre de fre
´quence de
´croissante, les anomalies
e
´chocardiographiques les plus e
´vocatrices sont : une hyper-
trophie du SIV, un aspect granite
´et scintillant du myocarde, une
hypertrophie de la paroi libre du ventricule droit, un e
´pan-
chement pe
´ricardique, une oreillette gauche dilate
´e ou une
dilatation biauriculaire, une hypertrophie du septum interauri-
culaire (anomalie peu fre
´quente mais tre
`s spe
´cifique), un
e
´paississement des feuillets valvulaires et l’existence de thrombus
intracardiaque [5]. Plusieurs de ces aspects e
´taient re
´unis chez
notre patient.
La me
´diane de survie des patients avec une amylose AL est
infe
´rieure a
`quatre ans, avec un tiers de mortalite
´a
`un an, 75 %
des de
´ce
`se
´tant lie
´sa
`l’atteinte cardiaque incluant 25 % de
morts subites [6]. Un traitement pre
´coce permet la disparition
des chaı
ˆnes le
´ge
`resdanslese
´rum et parfois une lente
re
´gression des signes cliniques, avec une re
´gression partielle
de l’atteinte cardiaque et ame
´lioration de la qualite
´de vie [7].
Le traitement symptomatique de l’insuffisance cardiaque
est souvent difficile et repose essentiellement sur les
diure
´tiques de l’anse, parfois a
`forte posologie. Les be
ˆta-
bloquants peuvent avoir un effet he
´modynamique de
´le
´te
`re
dans ce contexte et doivent e
ˆtre utilise
´s avec beaucoup de
prudence ; ils sont principalement re
´serve
´s aux patients en
fibrillation atriale rapide [8].
Conclusion
Une insuffisance cardiaque a
`fonction systolique pre
´serve
´e chez
un Africain hypertendu avec une HVG n’est pas syste
´matique-
ment ou exclusivement lie
´ea
`l’HTA. La connaissance des
aspects atypiques de certaines HVG permet de s’orienter vers
des causes rares d’insuffisance cardiaque peu ou pas de
´crites a
`
ce jour en Afrique mais ne
´anmoins classiques comme l’amylose
cardiaque. L’amylose cardiaque, en particulier de type AL,
s’inte
`gre dans un tableau syste
´mique e
´vocateur. Son pronostic
est se
´ve
`re a
`court terme.
Conflits d’inte
´re
ˆt:aucun.
Re
´fe
´rences
1. Opie L, Seedat YK. Hypertension in sub-saharian African populations.
Circulation 2005 ; 112 : 3562-8.
2. Lekpa FK, Ndongo S, Pouve A, et al. Les amyloses en Afrique
subsaharienne. Med Sante Trop 2012 ; 22 : 275-8.
3. Damasceno A, Mayosi BM, Sani M, et al. The Causes, Treatment, and
Outcome of Acute Heart Failure in 1006 Africans From 9 Countries : Results
of the Sub-Saharan Africa Survey of Heart Failure. Arch Intern Med 2012 ;
3 : 1-9.
4. Maceira AM, Joshi J, Prasad SK, et al. Cardiovascular magnetic resonance
in cardiac amyloidosis. Circulation 2005 ; 111 : 186-93.
5. Seldin DC, Berk JL, Sam F, Sanchorawala V. Amyloidotic cardiomyopa-
thy : multidisciplinary approach to diagnosis and treatment. Heart Fail Clin
2011 ; 7 : 385-93.
6. Merlin G, Seldin DC, Gertz MA. Amyloidosis : pathogenesis and new
therapeutic options. J Clin Oncol 2011 ; 29 : 1924-33.
7. Desport E, Bridoux F, Sirac C, et al. AL Amyloidosis. Orphanet J Rare Dis
2012 ; 7 : 54.
8. Falk RH. Diagnosis and management of the cardiac amyloidoses.
Circulation 2005 ; 112 : 2047-60.
Re
´sume
´.En Afrique, l’hypertension arte
´rielle est
un proble
`me majeur de sante
´publique, et la
cardiopathie hypertensive est une cause fre
´quente
d’insuffisance cardiaque. L’hypertrophie ventricu-
laire gauche (HVG) est l’une des manifestations
cardinales de la cardiopathie hypertensive. Cepen-
dant, certaines HVG peuvent re
´ve
´ler des patholo-
gies rares comme l’amylose cardiaque, pathologie
exceptionnellement de
´crite en Afrique. L’enque
ˆte
e
´tiologique d’une HVG atypique chez un Comorien
de 73 ans hospitalise
´pour insuffisance cardiaque a
permis de diagnostiquer une amylose cardiaque,
pathologie jamais rapporte
´e jusqu’alors aux
Comores et dont le pronostic demeure sombre.
Mots cle
´s:amylose cardiaque, hypertrophie ven-
triculaire gauche, insuffisance cardiaque, Comores.
Correspondance : P.-L. Massoure <plmassoure@aol.com>
Abstract. In Africa, hypertension is a major public
health problem, and hypertensive heart disease is a
leading cause of heart failure. Left ventricular
hypertrophy is a common consequence of hyper-
tension. We present a case illustrating an unusual
cause of such hypertrophy in a 73-year-old patient
with heart failure living in the Comoros Islands, in
whom we diagnosed cardiac amyloidosis. This
disease has not previously been reported in the
Comoros Islands and remains associated with a
poor prognosis.
Key words: cardiac amyloidosis, left ventricular
hypertrophy, heart failure, Comoros.
Me
´decine et Sante
´Tropicales, Vol. 23, N84 - octobre-novembre-de
´cembre 2013 393
Une cause rare d’insuffisance cardiaque
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
1
/
4
100%