Cancer neuroendocrine de la prostate. A propos de 6 cas

Le cancer neuroendocrine de la prostate représente une pathologie
rare, dont l’origine est discutée [2, 16]. Son diagnostic est histolo-
gique. Des cellules endocrines, à l’état normal, ont été mises en évi-
dence au sein de la prostate et du tractus urinaire par plusieurs
auteurs [2, 14]. Ces cellules ont été décrites au sein de près de 100%
des adénocarcinomes prostatiques [2] mais le plus souvent avec un
contingent minime.
La fréquence des cancers neuroendocrines est probablement sous esti-
mée en raison de l’absence d’étude immuno-histochimique systéma-
tique du tissu prostatique ainsi qu’un diagnostic souvent tardif, sans
relecture des lames d’anatomo-pathologie ni de nouvelle biopsie au
stade d’hormonorésistance. On en distingue principalement 2 formes,
une dite “pure” constituée exclusivement de petites cellules neuro-
endocrines, la plus rare, dont la fréquence se situe entre 0,2 et 1% [5]
et une forme mixte dans laquelle on retrouve au sein d’un adénocarci-
nome prostatique standard, souvent peu différencié, des cellules neuro-
endocrines en contingent variable, et dont la fréquence est inférieure à
10% (sans distinction de pourcentage de contingent) [5, 20].
Nous avons évalué les cas de cancers neuroendocrines diagnosti-
qués dans le service entre septembre 1998 et mai 2002.
MATERIELS ET METHODES
Nous avons effectué une étude rétrospective sur 6 cas de cancer
neuroendocrine de la prostate diagnostiqués entre septembre 1998
et mai 2002 dans le service. Le diagnostic était orienté par des élé-
ments cliniques et paracliniques (Tableau I) et posé par l’étude
immuno-histochimique du tissu prostatique. Les marqueurs
sériques (NSE, Chromogranine A) ont été dosés chez 3 patients. Ce
diagnostic était basé sur la mise en évidence d’un fort contingent
neuroendocrine (>50%) : recherche d’un marquage par les anti-
corps anti-Chromogranine A (Figure 1) et anti-Neuron Specific
Enolase (anti-NSE) (Figure 2), dont la positivité était retrouvée
respectivement dans 6 cas sur 6 et 5 cas sur 6, avec absence de mar-
quage par les anticorps anti-PSA dans tous les cas. Dans 5 des 6 cas
les fragments provenaient de biopsies endorectales et dans un cas
de résection trans-urétrale de prostate.
RESULTATS
Le cancer neuroendocrine représentait 2.1% des cancers de la pro-
state diagnostiqués dans le service sur la même période. L’âge
médian au moment du diagnostic était de 69.5 ans (61-89) (Tableau
II).
◆
ARTICLE ORIGINAL Progrès en Urologie (2003), 13, 1340-1344
Cancer neuroendocrine de la prostate. A propos de 6 cas
Xavier BRETON (1), Caroline PLAZANET (2), François Joseph MURAT (1), Serge MILINKEVITCH (2), Jacques IRANI (1),
Pierre LEVILLAIN (2), Bertrand DORÉ (1)
(1) Service d’Urologie, (2) Service d’Anatomo-pathologie, CHU La Milétrie, Poitiers, France
RESUME
Introduction : Le cancer neuroendocrine de la prostate (CNEP) représente une entité rare. Son dépistage, qui
n’est pas fait de manière systématique, a pourtant des implications thérapeutiques. Nous avons évalué rétrospec-
tivement 6 cas de CNEP observés dans le service entre septembre 1998 et mai 2002.
Matériel et Méthodes : Le diagnostic était basé sur l’analyse immuno-histochimique des fragments biopsiques
avec présence d’une différentiation neuroendocrine forte (minimum 50%). Une positivité pour les anticorps anti-
Neuron-Specific Enolase (NSE) et anti-Chromogranine A était notée dans 5 et 6 cas respectivement alors que le
marquage par anticorps anti-PSA était toujours négatif.
Résultats : Les CNEP représentaient 2,1% des cancers de la prostate diagnostiqués dans le service sur la même
période. Le toucher rectal était anormal dans tous les cas avec un PSA médian de 9,75 ng/ml (0.25-19.6). Trois
patients étaient métastatiques d’emblée. Quatre des 6 patients ont été hospitalisés en urgence pour une sympto-
matologie aiguë. Des douleurs abdominales paroxystiques sont apparues au cours de l’évolution dans tous les cas
avec une médiane de 52 jours (22-198) et étaient initialement présentes dans 2 cas. Une chimiothérapie a pu être
réalisée dans 3 cas et un traitement palliatif dans les autres cas. Une différence de survie a été notée chez les
patients ayant pu bénéficier d’une chimiothérapie (13 mois contre 4,7). La médiane de survie était de 9 mois et
14 jours, le décès survenant au décours d’une altération rapide de l’état général et de la fonction rénale.
Conclusion : Les CNEP ont un pronostique sombre. Des éléments cliniques et paracliniques orientent le dia-
gnostic qui sera confirmé par l’analyse immuno-histochimique. Ceci permettra une prise en charge précoce
basée sur la chimiothérapie.
Mots clés : Cancer prostatique, cancer à petites cellules, tumeurs neuroendocrine, traitement.
1340
Manuscrit reçu : avril 2003, accepté :septembre 2003
Adresse pour correspondance : Dr. X. Breton, Service d’Urologie, CHU La Milétrie, 3,
rue de la Milétrie, 86021 Poitiers Cedex.
e-mail : [email protected]
Ref : BRETON X., PLAZANET C., MURAT F.J., MILINKEBITCH S., IRANI J.,
LEVILLAIN P.DORE B., Prog. Urol., 2003, 13, 1340-1344

Circonstances diagnostiques
Dans 4 cas les patients ont été hospitalisés en urgence : 2 cas pour
rétention aiguë d’urine, un cas pour hématurie macroscopique et le
dernier pour douleur lombaire droite évoquant une colique néphré-
tique. La médiane du PSA était de 9,75 ng/ml (0.25-19.6) et seulement
2 cas ont été diagnostiqués en raison de l’élévation du PSA. Le tou-
cher rectal était anormal au moment du diagnostic, avec une prostate
dure et irrégulière pour l’ensemble des patients. Des douleurs abdo-
minales paroxystiques sont apparues au cours de l’évolution dans tous
les cas avec une médiane de 52 jours (22-198) et étaient initialement
présentes dans 2 cas. Une altération initiale de l’état général avec
amaigrissement était notée chez 3 des 6 patients. Un seul patient pré-
sentait des signes fonctionnels urinaires depuis plus de 2 ans. Dans un
cas le diagnostic a été suggéré par l’existence d’un syndrome para-
néoplasique sur le bilan biologique standard (Syndrome de Sécrétion
Inappropriée de l’Anti-Diurétique Hormone - SIADH).
Des métastases ont été découvertes chez 3 patients au cours du bilan
d’extension initial : hépatiques et osseuses dans 2 cas, pulmonaire
dans 1 cas.
Caractéristiques anatomopathologiques
Le caractère neuroendocrine du cancer de prostate a été recherché
d’emblée par l’analyse immuno-histochimique adéquate dans 3 cas
alors que dans les 3 autres cas, le diagnostic a été effectué dans un
second temps :
- dans 1 cas par relecture des lames de biopsie de prostate devant la
rapidité d’évolution de la maladie
- dans 2 cas lors d’un nouveau prélèvement (1 résection trans-uré-
thrale de prostate pour rétention aiguë d’urine et 1 ponction biopsie
hépatique).
Traitement
Seuls 3 patients ont pu bénéficier d’une chimiothérapie, les autres
étant contre-indiqués en raison de l’importance de l’asthénie et de
la rapidité d’évolution de la maladie. Deux des 3 patients traités par
chimiothérapie avaient eu le diagnostic de tumeur neuroendocrine
posé d’emblée.
Les chimiothérapies comprenaient toujours des sels de platine
(paraplatine, carboplatine, cis-platine) associé à du vépéside dans
un cas. Deux patients ont pu bénéficier de 3 cycles et le troisième
n’a eu qu’un cycle.
Evolution
Pour les 2 patients ayant eu plus d’un cycle de chimiothérapie, une
amélioration nette de l’état général associée à une normalisation du
taux de NSE et de Chromogranine A ont été observées avec une sur-
vie de 8 et 9 mois respectivement, supérieure aux autres cas
(Tableau II). Une différence de survie a été notée pour les 3 patients
ayant bénéficié d’une chimiothérapie (médiane 13 mois) par rap-
port au traitement hormonal simple (médiane 4,7 mois).
Une altération de l’état général et une insuffisance rénale obstructi-
ve sont apparues au cours de l’évolution de façon systématique,
responsable de troubles hydro électrolytiques à l’origine du décès.
DISCUSSION
Les cancers neuroendocrines de la prostate sont rares et de pronos-
tic sombre. Concernant la fréquence de ces cancers, il faut noter que
la définition même de cancer neuroendocrine reste encore obscure
à l’heure actuelle : Outre les cancers neuroendocrines à petites cel-
lules, dont le diagnostic anatomo-pathologique est plus aisé, un pro-
blème se pose pour les adénocarcinomes avec différentiation neuro-
X. Breton et coll., Progrès en Urologie (2003), 13, 1340-1344
1341
Tableau I. Critères devant faire évoquer un cancer neuroendocrine.
Clinique Paraclinique Anatomopathologique
• Altération récente et rapide de l’état général • PSA faiblement élevé avec TR anormal • Présence de cellules faiblement différentiées
• Douleurs abdominales paroxystiques +/- présence de métastases • Présence de granules denses
• Apparition et évolution rapide de signes fonctionnels • Existence d’un syndrome paranéoplasique intra-cytoplasmiques
urinaires obstructifs biologique • (gleason élevé)
• Existence d’un syndrome paranéoplasique clinique
• Absence d’amélioration sous traitement hormonal -->dosage NSE et Chromogranine A --> étude immuno-histochimique
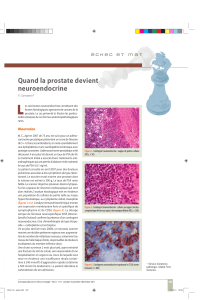
Figure 1. Immunomarquage positif par anticorps anti-Chromograni-
ne A, Objectif 20. Figure 2. Immunomarquage positif par anticorps anti-NSE, Objectif
20.

endocrine. En effet, la présence de cellules neuroendocrines a été
décrite au sein de près de 100% des adénocarcinomes prostatiques
[2] mais il n’y a pas à l’heure actuelle de consensus sur le pourcen-
tage de cellules neuroendocrines à partir duquel un adénocarcinome
prostatique est considéré comme neuroendocrine tant sur le plan
diagnostique, pronostique que thérapeutique. Nous avons inclus
dans notre étude les cas d’adénocarcinome prostatique comportant
au moins 50% de différentiation neuroendocrine lors de l’examen
anatomo-pathologique. Cela représentait les cas pour lesquels un
autre traitement était proposé au sein des réunions de concertation
pluridisciplinaire avec nos oncologues.
Notre étude a confirmé le mauvais pronostic de ce type de tumeurs.
La médiane entre le diagnostic et le décès étant de seulement 267
jours, comparable avec les données de la littérature [17]. Un dia-
gnostic précoce semble néanmoins être important dans leur prise en
charge en raison de leur rapidité d’évolution et de leur hormonoré-
sistance [9, 23]. Devant un cancer de prostate, plusieurs éléments
doivent faire évoquer un cancer neuroendocrine tant sur le plan cli-
nique, paraclinique qu’anatomopathologique (Tableau I). Parmi les
éléments cliniques, l’existence d’une altération de l’état général
d’installation et d’évolution rapide ainsi que la présence de dou-
leurs abdominales paroxystiques sont fortement évocatrices d’une
forme neuroendocrine. Dans notre étude, ces 2 symptômes étaient
présents respectivement dans 50 et 30% des cas au moment du dia-
gnostique et 100% au cours de l’évolution. Si l’existence d’une
altération de l’état général est souvent rapportée [5], la présence de
douleurs abdominales paroxystiques ne nous semble pas avoir été
décrite dans la littérature. Sur le plan biologique, un faible taux de
PSA discordant avec le toucher rectal et/ou le stade clinique (M+)
doit également attirer l’attention [18]. Parmi les 6 cas présentés, 3
étaient métastatiques d’emblée avec un taux de PSA inférieur à 20
ng/ml ce qui témoigne du caractère peu différencié de la tumeur et
doit faire rechercher un contingent neuroendocrine [22]. De même,
des perturbations du bilan biologique standard peuvent être en rap-
port avec un syndrome paranéoplasique secondaire à un carcinome
neuroendocrine. Dans la littérature, quelques articles rapportent des
syndromes paranéoplasiques, avec souvent des implications neuro-
logiques [7]. Dans notre étude, un patient présentait une hyponatré-
mie en rapport avec une sécrétion inappropriée d’hormone anti-diu-
rétique (SIADH).
Dans la littérature, nombre d’articles soulignent l’intérêt du dosage
plasmatique de la Chromogranine Aet du NSE dans le dépistage et
le suivi des cancers neuroendocrines avec une supériorité de la
Chromogranine A par rapport au NSE [8, 11, 16, 22]. ISSHIKI [22]
ainsi que DEFTOS [13] suggèrent même que le taux de Chromogra-
nine A est corrélé non seulement avec le pourcentage de cellules
neuroendocrines au sein de la tumeur mais aussi avec l’extension
métastatique. Au cours du suivi des adénocarcinomes prostatiques,
plusieurs auteurs [8, 15, 16] ont montré qu’une élévation de ces 2
marqueurs représentait un facteur de mauvais pronostic, indépen-
dant du PSA. Ceci reste néanmoins très discuté [3, 10, 28]. Par
ailleurs, dans le cadre de carcinomes neuroendocrines diagnosti-
qués d’emblée (comme c’était le plus souvent le cas dans notre
étude), leur intérêt est diagnostique et de suivi. Ils ne doivent pas
être réalisés à titre systématique devant tout cancer de la prostate,
en raison de leur coût élevé et du faible pourcentage représenté par
les cancers neuroendocrines. Néanmoins, lorsque plusieurs élé-
ments orientent vers une forme neuroendocrine (Tableau I), le dosa-
ge de ces 2 marqueurs représente un argument supplémentaire avant
une étude immuno-histochimique (nouvelle biopsie, relecture des
lames) qui confirmera le diagnostic.
Le caractère hormonorésistant des cellules neuroendocrines a été
prouvé par de nombreux auteurs [9, 23]. Une hormonothérapie est
cependant souvent instaurée initialement en raison de la méconnais-
sance du caractère neuroendocrine, de l’impossibilité de réaliser une
chimiothérapie ou basée sur le fait qu’il ne s’agit que d’un contin-
gent neuroendocrine et que ce traitement reste efficace sur le reste
de la prostate [19]. Le traitement chirurgical est rarement possible en
raison de la rapidité d’évolution de la maladie et de la découverte à
un stade tardif dans la majorité des cas. Dans notre étude, le toucher
rectal était anormal dans tous les cas au moment du diagnostic et un
geste chirurgical n’a pu être proposé à aucun patient. Néanmoins,
M
ACKEY
[25] a mis en évidence une augmentation de la survie dans
les cancers neuroendocrines prostatiques traités par prostatectomie
radicale. De même l’intérêt de la radiothérapie est décrit également
dans la littérature, souvent en association avec une chimiothérapie et
lorsque le stade clinique est localisé [6, 12].
Basée sur les similitudes avec les cellules neuroendocrines pulmo-
naires, une polychimiothérapie à base de platine a été proposée par
de nombreux auteurs [18, 27, 29] avec une rémission complète de
courte durée (quelques mois) dans certains cas [4, 26]. Dans notre
étude, une chimiothérapie a pu être réalisée dans 3 cas avec 3 cycles
dans seulement 2 cas. Un bénéfice thérapeutique a pu être rapide-
ment apprécié pour les 2 patients ayant eu plus d’un cycle, avec une
diminution de la symptomatologie urinaire, la disparition clinique
et radiologique des métastases et également une normalisation des
taux de NSE et de Chr A. Malheureusement la rechute est survenue
en quelques mois dans les 2 cas. Ce traitement doit être instauré le
1342
Tableau II. Récapitulatif des données
Patient Age PSA CREAT D. ABDO Délai TNM Gleason Traitement Survie Evolution
initial initiale PAROX d’apparition initial Score (jours)
initiales/ des D.ABDO
secondaires
N°1 71 11.4 76 NON/OUI 22 T2c Non fait Hormonothérapie 89 Aeg/IR décès
N°2 68 4.6 80 NON/OUI 53 T2a 8 (4+4) Hormonothérapie 120 Aeg/IR décès
N°3 64 8.18 77 NON/OUI 51 T3aM+ 7 (4+3) Chimiothérapie 353 Aeg/IR décès
N°4 89 14.5 78 NON/OUI 198 T2cM+ 9 (4+5) Hormonothérapie 215 Aeg/IR décès
N°5 63 19.6 40 OUI/OUI 0 T3b 7 (3+4) Hormonothérapie 434 Aeg/IR décès
puis
Chimiothérapie
N°6 61 0.25 62 OUI/OUI 0 T2cM+ 9 (4+5) Chimiothérapie 393 Aeg/IR décès
MEDIANE 69.5 9.755 68.8 52 8 267 100% décès
* D ABDO PAROX = Douleurs Abdominales Paroxystiques ; * Aeg = Altération de l’état général ; ** IR = Insuffisance Rénale.
X. Breton et coll., Progrès en Urologie (2003), 13, 1340-1344

plus précocement possible afin d’augmenter la survie comme l’ont
souligné AMATO [4] et MOORE [26]. Il est important de noter par
ailleurs la différence, dans notre étude, de survie entre les patients
ayant pu bénéficier d’une chimiothérapie (13 mois) et ceux traités
par hormonothérapie seule (4,7 mois).
Concernant les perspectives thérapeutiques, l’utilisation d’hormo-
nes neuroendocrines, dont les analogues de la somatostatine, la
bombésine et la sérotonine, semble intéressante [1, 21]. Certaines
sont déjà employées dans les cancers pulmonaires neuroendocrines
à petites cellules.
CONCLUSION
Les cancers neuroendocrines de la prostate ont un pronostique som-
bre. Plusieurs éléments cliniques et paracliniques doivent orienter
vers le diagnostic qui sera confirmé par l’analyse immuno-histochi-
mique et conduire à une prise en charge précoce basée sur la chi-
miothérapie.
REFERENCES
1. ABRAHAMSSON P.A. : Neuroendocrine differentiation in prostatic carci-
noma. Prostate, 1999 ; 39 : 135-148.
2. ABRAHAMSSON P.A., FALKME S., GRIMELIUS L. : The course of
neuroendocrine differentiation in prostatic carcinomas. An immunohisto-
chemical study testing Chromogranin A as an “endocrine marker”. Pathol.
Res. Pact., 1989 ; 185 : 373-380.
3. ALLEN F.J., VAN VELDEN D.J.J., HEYNS C.F. : Are neuroendocrine cells
of practical value as an independent prognostic parameter in prostate can-
cer? Br. J. Urol., 1995 ; 75 : 751-754.
4. AMATO R.J., LOGOTHETIS C.J., HALLINAN R., RO J.Y., SELLA A.,
DEXEUS F.H. : Chemotherapy for small cell carcinoma of prostatic origin.
J. Urol., 1992 ; 147 : 935-937.
5. ATHER M.H., ABBAS F. : Prognostic significance of neuroendocrine diffe-
rentiation in prostate cancer. Eur. Urol. 2000 ; 38 : 535-542.
6. AYGUN C. : Small cell carcinoma of the prostate : a case report and review
of the literature. Md Med. J., 1997 ; 46 : 353-356.
7. BAIRD A.D., CORNFORD P.A., HELLIWELL T., WOOLFENDEN K.A. :
Small cell prostate cancer with anti-Hu positive peripheral neuropathy. J.
Urol. 2002 ; 168 : 192-200.
8. BERRUTI A., DOGLIOTTI L., MOSCA A., BELLINA M., MARI M.,
TORTA M., TARABUZZI R., BOLLITO E., FONTANA D., ANGELI A. :
Circulating neuroendocrine markers in patients with prostate carcinoma.
Cancer 2000 ; 88 : 2590-2597.
9. BONKHOFF H. : Neuroendocrine cells in benign and malignant prostate tis-
sue : morphogenesis, proliferation and androgen receptor status. Prostate,
1998; 18-22.
10. COHEN M.K., ARBER D.A., COFFIELD K.S., KEEGAN G.T., MCCLIN-
TOCK J., SPEIGHTS V.O. : Neuroendocrine differentiation in prostatic ade-
nocarcinoma and its relationship to tumour progression. Cancer, 1994 ; 74 :
1899-1903.
11. CUSSENOT O., VILLETTE J.M., VALERI A., CARIOU G., DESGRAND-
CHAMPS F., CORTESSE A., MERIA P., TEILLAC P., FIET J., LE DUC
A.: Plasma neuroendocrine markers in patients with benign prostatic hyper-
plasia and prostatic carcinoma. J. Urol., 1996 ; 155 : 1340-1343.
12. DEBRAS B., CHAUTARD D., DELVA R., PABOT DU CHATELARD P.,
GUYETANT S., SORET J.Y. : Small cell carcinoma of the prostate. Com-
plete remission after chemotherapy : a propos of a case. Prog. Urol., 1994 ;
4 : 569-571.
13. DEFTOS L.J., NAKADA S., BURTON D.W., DI SANT’AGNESE P.A.,
COCKETT A.T.K., ABRAHAMSSON P.A. : Immunoassay and immuno-
histology studies of Chromogranin Aas a neuroendocrine marker in patients
with carcinoma of the prostate. Urology, 1996 ; 48 : 58-62.
14. DI SANT’AGNESE P.A. : Neuroendocrine differentiation and prostatic car-
cinoma. The concept ‘’comes of ages’’. Arch. Pathol. Lab. Med., 1988 ; 112:
1097-1099.
15. DI SANT’AGNESE P.A. : Neuroendocrine cells of the prostate and neuro-
endocrine differentiation in prostatic carcinoma : a review of morphologic
aspects Urology. 1998 ; 51 : 121-124.
16. FERRERO-POUS M., HERSANT A.M., PECKING A., BRESARD-
LEROY M., PICHON M.F. : Serum Chromogranin-A in advanced prostate
cancer. BJU Int., 2001 ; 88 : 790-796.
17. HELPAP B. : Morphology and therapeutics strategies for neuroendocrine
tumors of the genitourinary tract. Cancer, 2002 ; 95 : 1415-1420.
18. HELPAP B., KLOPPEL G. : Neuroendocrine carcinomas of the prostate and
urinary bladder : a diagnostic and therapeutic challenge. Virchows Arch.,
2002 ; 440 : 241-248.
19. HELPAP B., KOLLERMANN J. : Undifferentiated carcinoma of the prosta-
te with small cell features. Virchows Arch., 2001 ; 438 : 86-91.
20. HELPAP B., KOLLERMANN J. : Undifferentiated carcinoma of the prosta-
te with small cell features. Immunohistochemical subtyping and reflections
on histogenesis. Virchows Arch., 1999 ; 434 : 385-391.
21. HOOSEIN N.M., LOGOTHETIS C.J., CHUNG L.W. : Differential effects
of peptide hormones bombesin, vasoactive intestinal polypeptide and soma-
tostatin analog RC-160 on the invasive capacity of the human prostatic cells.
J. Urol., 1993 ; 149 : 1209-1213.
22. ISSHIKI S., AKAKURA K., KOMIYA A., SUZUKI H., KAMIYA N., ITO
H. : Chromogranin A concentration as a serum marker to predict prognosis
after endocrine therapy for prostate cancer. J. Urol., 2002 ; 167 : 512-515.
23. KRIJNEN J.L., JANSSEN P.J., RUIZEVELD DE WINTER J.A., VAN
KRIMPEN H., SCHRODER F.H., VAN DER KWAST T.H. : Do neuro-
endocrine cells in human prostate cancer express androgen receptor ? Histo-
chemistry, 1993 ; 100 : 393-398.
24. LEPINARD V., DAUGE-GEFFROY M.C., DELMAS V., BERTRAND G.,
FONDIMARE A., FETISSOF F. : Neuroendocrine cancers of the prostate.
Prog. Urol., 1993 ; 3 : 86-94.
25. MACKEY J.R., AU H.J., HUGH J. : Genito urinary small cell carcinoma :
determination of clinical and therapeutic factors associated with survival. J.
Urol., 1998 ;159 : 1624-1629.
26. MOORE S.R., REINBERG Y., ZHANG G. : Small cell carcinoma of pro-
state : effectiveness of hormonal versus chemotherapy. Urology, 1992 ; 39 :
411-416.
27. ROBENSTEIN J.H., KATIN M.J., MANGAMOM M. : Small cell anaplas-
tic carcinoma of the prostate : seven new cases : review of the litterature and
discussion of therapeutic strategy. Am. J. Clin. Oncol., 1997 ; 20 : 376-380.
28. SEGAWA N., MORI I., UTSUNOMIYA H., NAKAMURA M., NAKAMU-
RA Y., SHAN L., KAKUDO K., KATSUOKA Y. : Prognostic significance
of neuroendocrine differentiation, proliferation activity and androgen recep-
tor expression in prostate cancer. Pathol. Int., 2001 ; 51 : 452-459.
29. SELLAA., KONICHETZKY M., FLEX D. : Low PSA metastatic androgen-
independent prostatic cancer. Eur. Urol., 2000 ; 38 : 250-254.
____________________
SUMMARY
Neuroendocrine cancer of the prostate. A series of 6 cases.
Introduction: Neuroendocrine cancer of the prostate (NECP) is a rare enti-
ty. Screening for this tumour, although not systematic, may have therapeu-
tic implications. The authors retrospectively evaluated 6 cases of NECP
observed in the department between September 1998 and May 2002.
Material and Methods: The diagnosis was based on immunohistoche-
mical analysis of biopsy fragments with the presence of marked neuro-
endocrine differentiation (minimum 50%). Positive staining for anti-
Neuron-Specific Enolase (NSE) and anti-Chromogranin A antibodies
was observed in 5 and 6 cases, respectively, while anti-PSA antibody
labelling was always negative
1343
X. Breton et coll., Progrès en Urologie (2003), 13, 1340-1344

Results: NECP represented 2.1% of all prostate cancers diagnosed in
the department over the same period. Digital rectal examination was
abnormal in every case with a median PSA of 9.75 ng/ml (range: 0.25-
19.6). Three patients presented metastatic disease at the time of the dia-
gnosis. Four of the 6 patients were urgently admitted to hospital becau-
se of acute clinical features. Paroxysmal abdominal pain occurred
during the course of the disease in every case with a median of 52 days
(range: 22-198) and was initially present in 2 cases. Chemotherapy
was performed in 3 cases and palliative therapy was administered in
the other cases. A survival difference was observed for patients treated
by chemotherapy (13 months versus 4.7). The median survival was 9
months and 14 days. Death occurred in a context of rapid alteration of
the general state and renal function.
Conclusion: NECP has a poor prognosis. Clinical and complementary
features guide the diagnosis, which can be confirmed by immunohisto-
chemical analysis, allowing early management based on chemothera-
py.
Key-Words: prostate cancer, small cell carcinoma, neuroendocrine
tumours, therapy
1344
X. Breton et coll., Progrès en Urologie (2003), 13, 1340-1344
1
/
5
100%