Traitement des MICI chez l`enfant et l`adolescent

Mini-revue
Traitement des MICI
chez l’enfant et l’adolescent
Thierry Lamireau
1
, Dominique Turck
2
1
Unité de gastroentérologie et nutrition pédiatriques, Hôpital des Enfants, place Amélie-
Raba-Léon, 33076 Bordeaux Cedex
<thierry[email protected]>
2
Unité de gastroentérologie, hépatologie et nutrition, Clinique de pédiatrie, Hôpital
Jeanne-de-Flandre et Faculté de Médecine, 2, avenue Oscar-Lambret, 59037 Lille Cedex
Les maladies inflammatoires chroniques de l’intestin (MICI) débu-
tent dans l’enfance ou l’adolescence dans environ 10 % des cas,
avec une incidence de respectivement 2,3 cas de maladie de
Crohn (MC) et de 0,8 cas de rectocolite hémorragique (RCH) pour
100 000 enfants de moins de 17 ans. Les buts du traitement sont
d’induire et de maintenir la rémission, et d’assurer une qualité de
vie, en particulier une scolarité, satisfaisante. Le retentissement sur
la croissance et la puberté constitue la particularité essentielle des
MICI chez l’enfant, surtout dans la MC. La plupart des traitements
utilisés chez l’adulte sont validés chez l’enfant. Les techniques
nutritionnelles sont en revanche beaucoup plus utilisées dans cette
population. En effet, les causes de malnutrition sont nombreuses et
les carences en certains nutriments sont fréquentes. Le retentisse-
ment sur la croissance explique l’utilisation plus importante chez
l’enfant de l’alimentation artificielle, notamment avant 5 ans et en
période péripubertaire où la croissance est rapide. L’azathioprine
garde les mêmes indications que chez l’adulte. Au cours de la MC,
son utilisation précoce dès la première poussée afin de modifier
l’évolution de la maladie à long terme est actuellement débattue,
mais est préconisée par certains auteurs, notamment en cas
d’atteinte extensive d’emblée, en particulier pancolique. L’introduc-
tion des anticorps anti-TNFadans l’arsenal thérapeutique a trans-
formé la prise en charge de la MC puis, à un moindre degré, de la
RCH. Les données pédiatriques concernent essentiellement l’inflixi-
mab (Rémicade
®
), l’utilisation étant limitée pour les autres produits.
Mots clés : traitement, maladie inflammatoire chronique de l’intestin, enfant,
adolescent
Les maladies inflammatoires chroniques de l’intestin (MICI) débutent
dans l’enfance ou l’adolescence dans environ 10 % des cas, avec
une incidence de respectivement 2,3 cas de maladie de Crohn
(MC) et de 0,8 cas de rectocolite hémorragique (RCH) pour
100 000 enfants de moins de 17 ans dans le nord-ouest de la France [1].
Par rapport à l’adulte, la localisation au diagnostic de la MC chez l’enfant
est plus fréquemment iléocolique alors que la localisation de la RCH est
plus fréquemment pancolique. Les MICI débutant à l’âge pédiatrique sont
volontiers plus actives que chez l’adulte.
Hépato-Gastro, vol. 15, numéro spécial, juin 2008 5
doi: 10.1684/hpg.2008.0220
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Les buts du traitement sont d’induire et de maintenir la
rémission, et d’assurer une qualité de vie, en particulier
une scolarité, satisfaisante. Le retentissement sur la
croissance et la puberté constitue la particularité essen-
tielle des MICI chez l’enfant, surtout dans la MC, où un
retard staturo-pondéral est présent chez environ la
moitié des patients, souvent observé bien avant l’appa-
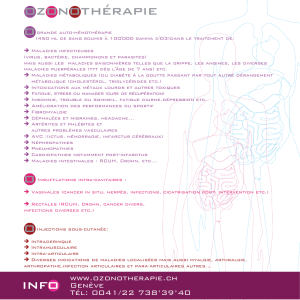
rition des signes digestifs (figure 1). Par ailleurs, la
corticothérapie peut aggraver le retard de croissance
si elle est utilisée à forte dose de façon prolongée.
Chez l’adolescent, un retard pubertaire est présent
dans un quart des cas. La prise en charge devra donc
adapter la stratégie thérapeutique, en particulier en
utilisant les supports nutritionnels, pour maintenir une
croissance satisfaisante et permettre une taille finale
proche de la taille cible. Le recours aux indices d’acti-
vité permet une appréciation objective de l’évolution
de la MC et de l’efficacité des traitements. On utilise
surtout le Pediatric Crohn’s Disease Activity Index
(PCDAI) [2], qui tient compte de la croissance staturale
(tableau 1).
Les thérapeutiques utilisées chez
l’enfant
Les données pharmacologiques manquent chez
l’enfant, et les essais thérapeutiques randomisés sont
très peu nombreux en pédiatrie, ce qui explique que les
attitudes se fondent souvent sur les données obtenues
chez l’adulte.
Médicaments
Les anti-inflammatoires non stéroïdiens sont représentés
essentiellement par la salazopyrine, dont l’utilisation
est très limitée chez l’enfant en raison de ses effets
secondaires, et surtout par les 5-amino-salicylés
(5-ASA) qui sont beaucoup mieux tolérés.
Dans la MC, quelques études contrôlées ont montré
que les 5-ASA ont une efficacité satisfaisante dans les
atteintes iléo-coliques modérées [3]. Ils peuvent égale-
ment être utilisés pour diminuer le risque de rechute
après chirurgie.
Dans la RCH, très peu d’études sont disponibles chez
l’enfant, et les indications sont calquées sur les données
établies chez l’adulte. Les 5-ASA sont actifs par voie
orale dans les poussées d’intensité faible à modérée et
peuvent être utilisés par voie rectale (suppositoires,
lavements) dans les formes recto-sigmoïdiennes. Ils sont
insuffisants pour traiter les formes graves mais peuvent
être aussi utilisés pour faciliter le maintien en rémission.
Les corticoïdes systémiques constituent depuis de nom-
breuses années le traitement de référence des poussées
d’intensité moyenne à sévère de MC et de RCH chez
l’adulte et l’enfant. Leur efficacité est reconnue, mais ils
peuvent entraîner de nombreux effets secondaires.
Environ la moitié des malades en deviennent dépen-
dants au cours de la MC, d’où la réticence à les utiliser
Tableau 1.Score d’activité de la maladie de Crohn utilisé chez
l’enfant. (Pediatric Crohn’s Disease Acitivity Index) [2].
Selles/jour
aucune 0
<5+sang 5
≥5 et sang abondant 10
Douleurs abdominales
absentes 0
modérées 5
sévères 10
Etat général
bon 0
moyen (activité limitée) 5
mauvais (arrêt de scolarité ou alitement) 10
Poids
gain normal 0
stagnation 5
perte de poids ≥10 % 10
Taille/vitesse de croissance
≥-1DS 0
<-1DSet>-2DS 5
≤- 2 DS 10
Masse abdominale
absente 0
douteuse 5
certaine 10
Lésions anales
absentes 0
fissures 5
fistules / abcès 10
Manifestations extra-intestinales,
articulaires, cutanées, fièvre > 38 °C, uvéite
absentes 0
une 5
plusieurs 10
Hématocrite (%)
≥34 0
29-33 5
<29 10
Vitesse de sédimentation
(mmàla1
re
heure)
<20 0
20-50 5
>50 10
Albumine (g/L)
≥35 0
31-34 5
≤30 10
Total :
Rémission : < 20
Atteinte moyenne : 30-50
Poussée sévère : > 50
Mini-revue
Hépato-Gastro, vol. 15, numéro spécial, juin 2008
6
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

de façon prolongée et le recours de plus en plus
précoce, en pédiatrie, aux immunomodulateurs.
Dans la MC, l’efficacité des corticoïdes à la dose de
1 mg/kg/j (sans dépasser 40 mg/j) est similaire à la
nutrition entérale avec un taux de rémission d’environ
85 % dans les MC nouvellement diagnostiquées [4]. Ils
sont utilisés à cette dose pendant une période de 2 à
4 semaines, suivie d’une baisse progressive de la dose
quotidienne par pallier de l’ordre de 5 mg par
semaine. Le maintien d’une faible dose de corticoïdes
n’est pas efficace dans la prévention des rechutes au
long cours et expose aux effets délétères sur la minéra-
lisation osseuse et la croissance. Les corticoïdes ont un
effet suppressif rapide et important sur la croissance
staturale, à partir d’une dose quotidienne de 0,2-
0,3 mg/kg/j, se cumulant avec les effets de l’inflam-
mation chronique pour entraîner dans la MC un ralen-
tissement, voire un arrêt complet, de la croissance en
taille. Quel que soit le sexe, la vitesse de croissance
staturale doit être d’au moins 4-5 cm/an de l’âge de
3-4 ans jusqu’au début de la puberté. Bien que l’admi-
nistration des corticoïdes un jour sur deux permette en
théorie de limiter l’effet délétère sur la croissance, le
recours possible aux immunomodulateurs ou à l’ali-
mentation entérale rend la corticothérapie prolongée
totalement injustifiée dans le traitement de la MC. Il est
bien sûr recommandé d’associer systématiquement une
supplémentation en calcium et en vitamine D pendant
la corticothérapie.
Dans les poussées de RCH, la prednisone à la dose de
1 mg/kg/j (sans dépasser 40 mg/j) est plus efficace
que la mésalazine [5]. Les corticoïdes peuvent être
utilisés par voie locale (suppositoires, lavements) dans
les formes distales. Ils n’ont aucun effet préventif sur la
survenue de rechutes.
Le budésonide est un corticoïde dont la faible diffusion
systémique explique la moindre fréquence des effets
indésirables par rapport aux corticoïdes systémiques.
Les données pharmacologiques chez l’enfant sont simi-
laires à celles chez l’adulte.
Des études contrôlées dans la MC iléale ou iléocolique
droite de l’enfant ont montré que l’efficacité du budéso-
nide est peu différente de celle de la prednisone (50-
71 % de rémission), un peu plus lente, mais avec moins
d’effets secondaires [6]
. Il n’y a pas de données dispo-
nibles sur l’efficacité et la tolérance du budésonide en
traitement d’entretien en pédiatrie. Les effets délétères
sur la taille sont moins importants qu’avec les corticoï-
des systémiques, mais un ralentissement de la crois-
sance est possible en cas d’administration prolongée.
Les antibiotiques sont utilisés en raison du rôle proba-
ble de la flore bactérienne du tube digestif dans la
physiopathologie de la MC.
Bien qu’aucune étude contrôlée ne soit disponible chez
l’enfant, le métronidazole est volontiers prescrit dans
les atteintes anopérinéales de la MC. Son utilisation
prolongée, au-delà d’une durée d’un mois, expose au
risque de neuropathies, qui ont souvent une expression
plus électrique que clinique, et régressent habituelle-
ment à l’arrêt du traitement. Aucune étude n’a évalué
l’intérêt des fluoroquinolones, contre-indiquées avant
10 ans.
Les probiotiques sont potentiellement intéressants dans
les MICI par leur effet modulateur de la microflore
intestinale et des réponses immunes locales. Les résul-
tats sont insuffisants, chez l’enfant comme chez
l’adulte, pour recommander leur utilisation en pratique
clinique.
L’azathioprine (AZA) est débutée de plus en plus pré-
cocement chez l’enfant et l’adolescent dans les formes
de MICI actives avec rechutes fréquentes ou dans les
formes cortico-dépendantes, en raison de son délai
d’action prolongé (3 à 4 mois en moyenne) et de la
contre-indication formelle à utiliser les corticoïdes de
façon prolongée. L’AZA est utilisé initialement à la
posologie de 2,5 mg/kg/j. Un sevrage de la cortico-
thérapie est obtenu dans 70 à 75 % des cas chez
l’enfant.
P1
A0 11 ans
A0 13 ans
NEDC
NP
I
Figure 1.Retard de croissance dans la maladie de Crohn.
Hépato-Gastro, vol. 15, numéro spécial, juin 2008 7
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Au cours de la MC, son utilisation précoce dès la
première poussée afin de modifier l’évolution de la
maladie à long terme est actuellement débattue, mais
est préconisée par certains auteurs, notamment en cas
d’atteinte extensive d’emblée, en particulier pancoli-
que [7].
Dans la RCH, l’AZA permet une épargne des corticoï-
des ou de prendre le relais d’un traitement par ciclos-
porine dans les formes cortico-résistantes.
L’administration prolongée de l’AZA pose le problème
des effets secondaires, qui semblent toutefois assez
rares chez l’enfant. La survenue de pathologie mali-
gne, notamment de lymphome, est considérée comme
faible et acceptable en regard du bénéfice quant à la
qualité de vie [8]. Le dosage de l’activité de la TPMT et
la surveillance du taux de 6-thioguanine pour prédire
la toxicité et ajuster la posologie restent débattus, en
pédiatrie comme chez l’adulte.
Le méthotrexate (MTX) à faible dose est utilisé en cas de
cortico-dépendance, ou d’échec de l’AZA, ou encore
de complications [9]. Il permet un sevrage des corticoï-
des dans environ 1 cas sur 2 chez l’enfant et l’adoles-
cent. On note souvent un épuisement de l’effet théra-
peutique avec survenue de rechutes dans 50 % des cas
à 3 ans. La dose recommandée de MTX est de l’ordre
de 15 mg/m
2
en une injection sous-cutanée hebdoma-
daire. Les effets secondaires et la surveillance sont
analogues à ce qui est décrit chez l’adulte. Le MTX est
parfois utilisé au cours de la RCH, mais aucune donnée
n’est disponible chez l’enfant.
La ciclosporine est proposée à la dose de 2 mg/kg/j
dans le traitement des poussées sévères, cortico-
résistantes de RCH pour éviter la colectomie en
urgence, sur une courte période en raison de sa
toxicité, notamment rénale, impliquant la nécessité
d’un relais par les immunomodulateurs « classiques »
(MTX, AZA), et la chirurgie reste souvent nécessaire à
moyen terme. L’expérience est limitée en pédiatrie, et
son utilisation repose sur les données publiées chez
l’adulte. La ciclosporine n’est habituellement pas effi-
cace dans le traitement de la MC, sauf parfois en cas
de colite aiguë grave.
L’introduction des anticorps anti-TNF
␣
dans l’arsenal
thérapeutique a transformé la prise en charge de la
MC puis, à un moindre degré, de la RCH. Les données
pédiatriques concernent essentiellement l’infliximab
(Rémicade
®
), l’utilisation étant limitée pour les autres
produits.
Dans la MC de l’enfant, le traitement d’induction par
3 perfusions d’infliximab (IFX) à la dose de 5 mg/kg
aux semaines S0, S2 et S6 entraîne une amélioration
dans 52 à 100 % des cas, et une rémission dans 21 à
90 % des cas [10, 11] dans les formes intraluminales
réfractaires et les formes fistulisantes. Un traitement
concomitant par immunomodulateurs (AZA surtout)
limite la formation d’anticorps anti-infliximab, et sem-
ble diminuer les réactions indésirables. Cependant, la
description de cas de lymphome hépato-splénique T
chez plus d’une dizaine d’enfants adolescents et de
jeunes adultes, tous traités par AZA et IFX [12], a fait
renoncer à cette association thérapeutique. La majorité
des patients rechutant après l’arrêt du traitement, l’IFX
au long cours est proposé, tout comme chez l’adulte.
L’étude REACH a montré que 55 % des enfants ayant
répondu au traitement initial sont maintenus en rémis-
sion par des perfusions d’IFX à la dose de 5 mg/kg
toutes les 8 semaines contre 23 % en cas de perfusion
toutes les 12 semaines [13]. L’efficacité sur la maladie
digestive s’accompagne d’une reprise de la croissance
[14]. En cas d’échappement, on peut au cas par cas
augmenter la posologie jusqu’à 10 mg/kg ou raccour-
cir à 6 semaines le délai entre les perfusions. En cas de
réaction lors de la perfusion ou d’hypersensibilité retar-
dée, le traitement peut être poursuivi sous couvert d’une
corticothérapie ou bien changé pour un anticorps
anti-TNFahumanisé (Humira
®
).
Dans la RCH, l’IFX est efficace pour induire une rémis-
sion clinique et une cicatrisation des lésions endosco-
piques dans les formes sévères cortico-résistantes. Seu-
les quelques études rétrospectives, avec de faibles
effectifs, ont été conduites chez l’enfant. Le traitement
par IFX à la dose de 5 mg/kg entraîne une réponse à
court terme, définie par l’absence de reprise de corti-
cothérapie ou de recours à la chirurgie, dans 64 à
83 % des cas [15].
Techniques nutritionnelles
Les causes de malnutrition sont nombreuses (tableau 2)
et les carences en certains nutriments sont fréquentes
(tableau 3). Le retentissement sur la croissance [16]
explique l’utilisation plus importante chez l’enfant de
l’alimentation artificielle (tableau 4), notamment avant
5 ans et en période péripubertaire où la croissance est
rapide.
L’alimentation orale doit couvrir les besoins énergéti-
ques des patients en estimant qu’ils sont a priori supé-
rieurs de 20 à 50 % aux apports recommandés pour
l’âge. Un régime pauvre en lactose et en fibres est
conseillé uniquement lors des poussées. Certains
auteurs ont rapporté l’efficacité dans la MC d’un pro-
duit polymérique à base de caséine enrichi en TGFb
donné de façon exclusive par voie orale pendant
8 semaines [17]. Le taux de rémission obtenu avec ce
produit était comparable à celui classiquement
observé après corticothérapie orale. Néanmoins,
aucune étude contrôlée n’a été réalisée en pédiatrie.
La nutrition entérale à débit continu est aussi efficace
que la corticothérapie dans la MC avec une rémission
obtenue dans 85 % des cas [4]. Elle semble en revan-
che plus efficace lors d’une première poussée (86 %)
Mini-revue
Hépato-Gastro, vol. 15, numéro spécial, juin 2008
8
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

qu’en cas de rechute (50 %). Il n’y a pas d’avantage à
utiliser un soluté élémentaire ou semi-élémentaire par
rapport à un produit polymérique. Les effets cosméti-
ques indésirables et le retentissement sur la croissance
des corticoïdes militent en faveur de l’alimentation
entérale en cas de retard staturo-pondéral et/ou puber-
taire important. Administrée sur 10 à 12 heures la nuit,
l’alimentation entérale est compatible avec une réinser-
tion familiale et scolaire. Néanmoins, elle n’est pas
toujours bien acceptée sur le plan psychologique par
les adolescents en raison de l’arrêt de l’alimentation
orale et de la présence de la sonde naso-gastrique.
À côté de son effet dans les poussées de MC, l’alimen-
tation entérale a également un intérêt pour le traitement
du retard staturo-pondéral et/ou pubertaire. Elle doit
être débutée précocement, avant que le développe-
ment pubertaire n’atteigne le stade III de Tanner. Elle
peut être utilisée au long cours de façon intermittente,
1 mois tous les 4 mois, associée à une alimentation
orale diurne, permettant alors de doubler ou de tripler
la vitesse de croissance [18] et de maintenir la rémis-
sion clinique [19]. Lorsqu’une alimentation entérale est
prévue pour une durée prolongée, la pose d’une gas-
trostomie endoscopique peut être discutée si la sonde
naso-gastrique est mal tolérée, et en l’absence de
localisation gastrique de la MC. L’utilisation de plus en
plus fréquente et précoce des immunomodulateurs en
pédiatrie va réduire dans l’avenir les indications de
l’alimentation entérale.
L’alimentation parentérale a également un effet bénéfi-
que sur l’état nutritionnel et la croissance dans les MICI
de l’enfant. Du fait de ses risques, notamment infectieux
et thromboemboliques, ses indications sont extrême-
ment limitées : poussée sévère résistante au traitement
médicamenteux ou à l’alimentation entérale, et inac-
cessible à la chirurgie ; forme occlusive ou fistulisée ;
prise en charge nutritionnelle périopératoire ; résection
intestinale étendue (tableau 3).
Chirurgie
Il n’existe pas de consensus sur le traitement chirurgical
des MICI en pédiatrie, et certaines équipes recourent
plus volontiers au traitement chirurgical que d’autres.
Dans la MC, la chirurgie est habituellement réservée
comme chez l’adulte aux complications (fistules, sténo-
ses, perforations, abcès) en limitant au maximum
l’étendue des segments réséqués. Une indication bien
posée de résection intestinale limitée en cas de sténose
iléale permet parfois une amélioration de la crois-
Tableau 2.Causes de malnutrition au cours de la maladie de
Crohn chez l’enfant [16].
Diminution des apports
- dues à la maladie : douleurs abdominales, diarrhée induite par
l’alimentation, effet anorexigène des cytokines pro-
inflammatoires, altérations du goût, troubles psychologiques
- iatrogène
Malabsorption intestinale
- diminution de la surface d’absorption intestinale (fistule, résec-
tion intestinale étendue)
- pullulation microbienne intraluminale (sténose du grêle)
- déficit en sels biliaires (iléite, résection iléale)
Augmentation des pertes intestinales
- entéropathie exsudative
- diarrhée, fistule (électrolytes, minéraux, oligoéléments)
- saignement digestif chronique
Interactions médicamenteuses
- corticoïdes (métabolisme calcique et protéique)
- sulfasalazine, méthotrexate (métabolisme des folates)
- cholestyramine (malabsorption des lipides et des vitamines lipo-
solubles)
Augmentation des dépenses énergétiques
- hypercatabolisme protéique (cytokines pro-inflammatoires, corti-
cothérapie)
- fièvre, infection, inflammation
- renouvellement cellulaire intestinal (altération des muqueuses,
fistule)
- croissance normale ou de rattrapage
Tableau 3.Carences nutritionnelles au cours de la maladie de
Crohn chez l’enfant et l’adolescent [16].
Déficit Prévalence (%)
Fer 70
Calcium 10 – 20
Magnésium 20
Zinc 20
Cuivre rare
Acide folique 50
Vitamine B12 (test de Shilling
anormal) 40–50
Vitamine D 60 – 70
Vitamine A 5 – 10
Vitamine K rare
Vitamine E rare
Vitamine C rare
Tableau 4.Indications des techniques d’alimentation
artificielle au cours de la maladie de Crohn de l’enfant [16].
Alimentation entérale
- Poussée aiguë avec dénutrition
- Retard staturo-pondéral et/ou dénutrition
- Forme cortico-dépendante ou -résistante
Alimentation parentérale
- Forme suraiguë, résistante au traitement médicamenteux
et à l’alimentation entérale, et inaccessible à la chirurgie
- Forme occlusive
- Fistule résistante au traitement médicamenteux et à l’alimenta-
tion entérale
- Prise en charge nutritionnelle péri-opératoire
- Résection intestinale étendue
Hépato-Gastro, vol. 15, numéro spécial, juin 2008 9
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
 7
7
 8
8
1
/
8
100%