ASPECTS MICROBIOLOGIQUES de la - IFR-133-IBCT

1
Infection Chronique et Inflammation chez le Patient
Atteint de Mucoviscidose
Patrick Plésiat/Gérard Couetdic
EA3186, IFR133
UFR SMP Besançon

2
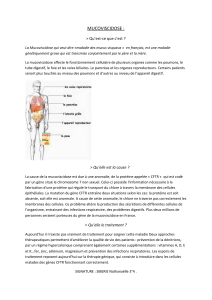
Rappel: la mucoviscidose
Mucoviscidose ou fibrose kystique
–Maladie génétique autosomique récessive grave et fréquente (1:2500 naissances dans
la population européenne; 1:12000 au Moyen-Orient)
–Hétérozygotes sains (?) 1:25 individus
Déficit
–Défaut de la perméabilité aux ions Cl-des cellules épithéliales des glandes exocrines
et des voies respiratoires
–Absence ou altération des canaux ioniques CFTR (cystic fibrosis transmembrane
conductance) qui normalement permettent la sortie des Cl-après activation par une
protéine kinase AMPc-dépendante
–Production de secrétions visqueuses obstruant les voies respiratoires, le pancréas
et/ou les glandes séminales.

3
Expression clinique de la maladie
Maladie très polymorphe
–Formes sévères avec affections pulmonaires graves et insuffisance pancréatique;
issue fatale rapide
–Formes atténuées aux conséquences pulmonaires variées et suffisance
pancréatique; issue fatale à ± long terme (25 - 30 ans)
–Formes asymptomatiques avec absorption normale des aliments et des graisses
Génotype et phénotype
– 2 allèles “sévères” entraînent plus souvent une insuffisance pancréatique que 2
allèles “atténués”
–D’autres facteurs peuvent moduler la sévérité et la progression de la maladie:
»contexte génétique de l ’individu: gènes modulateurs
»environnement: qualité des soins, conditions de vie, précocité du diagnostic..

4
Les défauts du CFTR
Gène et protéine
–Gène sur le bras long du chromosome 7
–Protéine dimérique de 1480 aa / sous-unité, 6 segments transmb, sites de
phosphorylation (domaine R), site de liaison aux nucléotides triPO4 (NBF), même
famille de transporteurs que glycoprotéines-P
–Plus de 600 mutations décrites: substitutions d ’aa, délétions, protéines tronquées…
la mutation DF508 représente 50 à 80% des mutations
Les dégâts causés par les mutations
–DF508 empêche la maturation correcte de la protéine, sa glycosylation et sa
migration jusqu’ à la membrane cellulaire
–Autres mutations: perturbent la synthèse de la protéine, sa migration ou son
insertion correcte dans la mb, diminuent la conductance du canal...
–Conséquences indirectes (?): augmentation de l ’absorption du Na+, de la
sulfatation des protéines et diminution de la sialylation des glycoprotéines

5
Mutations du gène cftr
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
1
/
15
100%