Structure de l'atome : Ionisation, électronégativité et taille

Rappel: Structure de l’atome

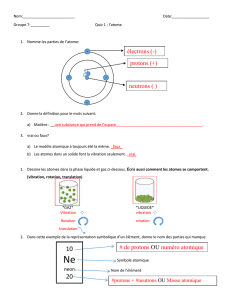
L'atome
= [neutrons(n) + protons(+)] + Cortège électronique(-)
NOYAU
Hydrogène, 1 proton, numéro atomique = 1
Fer, 26 protons, numéro atomique = 26
Nbre Protons = Nbre électrons = numéro atomique (Z)
Nbre Protons + Nbre neutrons = nombre de masse (N)
Atome = NAZ

Les Isotopes

Niveaux d’énergie et orbitales
Orbitales: densité de probabilité de présence des électrons autour du noyau
n: nombre quantique principal : rayon de l’atome
l: nombre quantique de moment angulaire (forme)
ml: nombre quantique magnétique
ms: nombre quantique de spin

Les orbitales
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
1
/
26
100%