les atomes et éléments

SCIENCES 9E ANNÉE
MODULE 3 : LES ATOMES ET LES ÉLÉMENTS
TEST SOMMATIF
Nom :__________________________________________________
Date : _____________
Connaissances visées :
utiliser des modèles pour décrire la structure et les composants des atomes et des molécules.
donner des exemples montrant le regroupement des éléments dans le tableau périodique.
donner des exemples des éléments communs et comparer leurs caractéristiques et leur structure
atomique.
identifier et écrire le symbole chimique ou la formule moléculaire d’éléments ou composés
communs.
Consigne :
Lis attentivement chaque question.
Réfléchis avant de donner une réponse.
Réponds aux questions en suivant tes réflexions.
Fais un retour sur tes réponses
Approfondie tes réponses si possible
Fais une vérification de ton examen avant de remettre l’examen à ton enseignant
Note : Vérifie que tu as utilisé les bons termes en français et en sciences 9e année.
Temps alloué : 50minutes
BON SUCCES!!!

SCIENCES 9E ANNÉE
MODULE 2 : LES ATOMES ET LES ÉLÉMENTS
TEST SOMMATIF
Partie 1 : L’atome et ses particules (10 points)
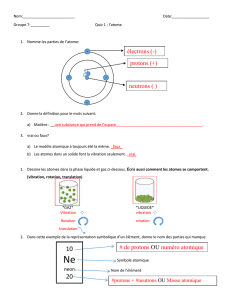
A. Nomme les parties de l’atome indiquées par une ligne (5 points)
A. Complète les questions suivantes en utilisant les renseignements de l’atome ci-haut (5
points)
nombre d’électrons :
nombre de protons :
nombre de neutrons :
numéro atomique de
l’élément :
nom et symbole de
l’élément :

Partie 2 : Révision (10 points)
1. Combien de protons, d’électrons et de neutrons aura un atome de magnésium, de numéro
atomique 12 et masse atomique 24,305? (3 points)
2. Les isotopes naturels de rubidium et de strontium ont le même nombre de masse 87.
Explique comment cela est possible. (Rb no 37 et Sr no 38) (2 points)
3. Pourquoi les métaux alcalins (I) et les halogènes (XVII) sont-ils si réactifs? (2,5 points)
4. Qu’est-ce qu’une liaison covalente (moléculaire)? Quels types d’atomes se combinent dans
des liaisons covalentes? (2,5 points)

Partie 3 : Les modèles atomiques (15 points)
A. Dessine le modèle de Dalton pour l’Argon
B. Dessine le modèle de Rutherford pour le Magnésium
C. Dessine le modèle de Bohr-Rutherford pour le Silicium
Partie 4 : Les liaisons chimiques (15 points)
A. À partir de tes connaissances du tableau période et des familles, quelles formules sont
erronées? Corrige-les:
a. LiCl2 _____________________
b. KS _____________________
c. MgF2 _____________________
d. AlO3 _____________________

B. Dessine le modèle de formation de la liaison et indique s’il s’agit d’un composé ou d’une
molécule:
1. de l’oxyde de magnésium MgO (2 points)
2. du bromure de potassium KBr (2 points)
3. de l’azote gazeux N2 (2 points)
4. l’alcool C2H5OH (4 points)
1
/
5
100%