Uvéite Vogt Koyanagui Harada

CAS CLINIQUE
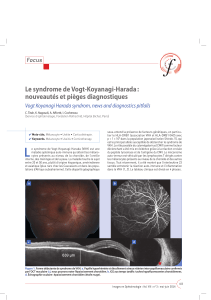
▲ Figure 1. Fond d’œil avec plis choroïdiens bilatéraux et aspect de
pâleur choroïdienne à gauche.
68 | La Lettre du Neurologue • Vol. XIX - no 3 - mars 2015
Mots-clés
Baisse d’acuité visuelle – Uvéite – Sclérose en plaques
Keywords
Decreased visual acuity – Uveitis – Multiple sclerosis
Quand la vue sème le trouble…
When the view sow disorder…
A. Fromont*, P. Koehrer**, T. Moreau*
* Service de neurologie 2, pathologies infl ammatoires et neurologie générale,
CHU de Dijon.
** Service d’ophtalmologie, CHU de Dijon.
Observation
Mme RS, âgée de 37 ans, sans antécédent médical personnel
mais dont la mère est suivie pour un trouble ophtalmologique
nécessitant une corticothérapie au long cours, présente entre
mars 2012 et septembre 2013 6 épisodes neurologiques, de
quelques semaines, d’instabilité ou de faiblesse du membre
inférieur droit ou d’impériosités mictionnelles.
Elle ne consulte qu’en décembre 2013, alors qu’elle a une
marche avec embardées et une paraparésie avec pares-
thésies de la main droite. Le bilan biologique ne montre pas
de syndrome infl ammatoire. La ponction lombaire (PL) est
normale. La recherche de synthèse intrathécale d’immuno-
globulines G (IgG) et de bandes oligoclonales n’est alors pas
réalisée. L’IRM encéphalique révèle plusieurs hypersignaux
T2 FLAIR périventriculaires et un hypersignal du pédoncule
cérébelleux moyen gauche non rehaussés après injection de
gadolinium. L’IRM médullaire est considérée comme normale.
La patiente est traitée par bolus de méthylprednisolone, puis
un traitement immunomodulateur (interféron β-1a [IFNβ-1a]
en sous-cutané [s.c.]) est commencé pour une sclérose en
plaques (SEP) rémittente.
En août 2014, la patiente consulte au CHU de Dijon. Depuis
3 semaines, elle a constaté l’apparition d’un scotome devant
l’œil gauche sans douleur à la mobilisation du globe oculaire.
L’acuité visuelle est de 1/10 P2 à gauche. Le fond d’œil révèle
des plis choroïdiens bilatéraux avec un certain degré de
dépigmentation choroïdienne sans infl ammation du segment
antérieur ou postérieur, ni papillite ou vascularite (fi gure 1). La
tomographie par cohérence optique (OCT) confi rme des plis
choroïdiens et montre de larges décollements séreux rétiniens
(DSR) cloisonnés (fi gure 2). L’angiographie à la fl uorescéine
montre, du côté gauche, une discrète diffusion de fl uorescéine
papillaire et, aux temps tardifs, des points de fuite (pin-points)
avec remplissage des DSR (fi gure 3).
L’angiographie au vert d’indocyanine montre un remplissage choroïdien
hétérogène avec aspect de vascularite choroïdienne et des hypocya-
nescences ponctiformes bilatérales aux temps tardifs, en faveur d’un

CAS CLINIQUE
◀ Figure 4.
Angiographie à la fl uorescéine
(à gauche) montrant
des points de fuite (pin-points)
et un pooling du colorant
dans les poches de DSR
aux temps tardifs.
Angiographie au vert
d’indocyanine (à droite)
montrant des hypocyanescences
tardives.
▲ Figure 2. Cliché infrarouge du pôle postérieur (à gauche) corrélé au SD-OCT
maculaire (plan de coupe : la ligne verte, à droite) de l’œil gauche : aspect de
plis choroïdiens et larges DSR multicloisonnés.
▲ Figure 3. Angiographie au vert d’indocyanine aux temps précoces objectivant
un remplissage choroïdien hétérogène et un aspect de vascularite choroïdienne.
La Lettre du Neurologue • Vol. XIX - no 3 - mars 2015 | 69
processus infl ammatoire choroïden (fi gure 4). Les ophtalmo-
logistes concluent à une maladie de Vogt-Koyanagi-Harada
(VKH). L’examen neurologique retrouve un périmètre de
marche limité à 1 km avec une marche cérébellospastique. La
marche du funambule est impossible. La patiente n’a aucun
défi cit moteur, les réfl exes ostéotendineux sont très vifs et
symétriques avec un signe de Babinski bilatéral. La sensibilité
au tact et au froid est préservée avec une hypopallesthésie
des hallux. L’examen retrouve un syndrome cérébelleux
cinétique du membre supérieur droit et des membres
inférieurs. L’extrémité céphalique est normale en dehors de
la baisse de l’acuité visuelle à gauche. La patiente rapporte
des impériosités mictionnelles. Elle n’a ni poliose, ni livedo,
ni alopécie. La consultation ORL est normale. Son typage
HLA est HLA DRB1*04-05. Après enquête auprès des ophtal-
mologistes, sa mère souffrait d’un VKH.
La patiente est hospitalisée. Le bilan biologique standard est
normal sans syndrome infl ammatoire ; le bilan auto-immun
est sans particularité. La PL retrouve 46 globules blancs/mm3,
dont 97 % de cellules mononucléées, des globules rouges,
une protéinorachie et une glycorachie normales. Elle révèle la
présence d’une synthèse intrathécale d’IgG avec index de Link
à 0,78 et présence de bandes oligoclonales. L’IRM cérébrale
est stable (figure 5, p. 70). L’IRM médullaire révèle un
hypersignal T2 à la hauteur de C4 latéralisé à gauche et
un C5 latéralisé à droite, non rehaussés par le gadolinium
(figure 6, p. 70). Un traitement par bolus de méthyl-
prednisolone pendant 3 jours, relayé par une corticothé-
rapie per os à 1 mg/kg/j est instauré avec arrêt de l’IFNβ-1a.
Au bout de 2 mois, l’acuité visuelle à gauche est norma-
lisée avec disparition des DSR en OCT (figure 7, p. 71).
Un traitement par diméthyl-fumarate est commencé.

CAS CLINIQUE
▲ Figure 5. IRM encéphalique séquence T2 FLAIR : hypersignaux périventriculaires et du pédoncule cérébelleux moyen gauche.
◀ Figure 6.
IRM médullaire : séquence T2
sagittale et T2 axiale.
Hypersignal T2 à la hauteur
de C4 latéralisé à gauche
et un C5 latéralisé à droite.
70 | La Lettre du Neurologue • Vol. XIX - no 3 - mars 2015

CAS CLINIQUE
▲ Figure 7. Disparition des DSR en OCT.
Discussion
Le VKH est une méningo-encéphalo-uvéite qui répond à des critères
diagnostiques précis (encadré) [1]. La physiopathologie du VKH serait
liée à l’activation de lymphocytes T par des peptides dérivés des
mélanocytes présentés par des cellules présentatrices d’antigènes. Les
lymphocytes T activés seraient dirigés contre les tissus contenant des
mélanocytes (méninges, uvée, peau, oreilles)
[2]. F.M. Damico et al. (3)
ont montré que les lymphocytes T des patients HLA DRB1*04-05 et
VKH reconnaissent un répertoire de peptides dérivés des mélanocytes
plus large que ceux HLA DRB1*04-05 négatifs.
Le VKH comporte 4 phases (3). Les prodromes de la première phase
se manifestent par un syndrome pseudogrippal (fi èvre, nausées, etc.),
des signes et des symptômes neurologiques (céphalées, méningo-
encéphalite aseptique, atteinte des nerfs crâniens, syndrome
cérébelleux, hémiparésie, aphasie, dysarthrie, troubles vésico-
sphinctériens, atteintes périphériques à type de polyradiculonévrite
aiguë). À ce stade, le liquide cérébrospinal révèle une pléiocytose
dans 80 % des cas dans la semaine qui suit le début. Les prodromes
peuvent être suivis en quelques jours par une phase d’uvéite aiguë,
bilatérale, rarement symétrique, diffuse avec hyperhémie et DSR.
L’infl ammation peut s’étendre au segment antérieur de l’œil. Après
plusieurs semaines, une phase de convalescence survient pendant
laquelle peuvent apparaître des dépigmentations des téguments et
de la choroïde. Chez les deux tiers des patients, une phase récurrente
ou chronique apparaît caractérisée par des épisodes récidivants
d’uvéites antérieures. Les récurrences d’uvéites postérieures sont
plus rarement observées au fond d’œil.
Notre observation soulève une question : s’agit-il d’un VKH seul
ou d’un VKH associé à une SEP ? Plusieurs arguments plaident en
faveur de la deuxième hypothèse : l’histoire clinique de la patiente,
la présence de bandes oligoclonales et l’existence d’une atteinte
médullaire. Si cette dernière est rapportée dans quelques cas de
VKH (4), elle s’explique mal puisqu’il n’y a pas de mélanocytes dans
la moelle. De plus, 1 cas de VKH associé à une SEP est rapporté
dans la littérature (5). Le rôle de l’IFNβ dans la survenue du VKH
se pose. Des cas de VKH ont été rapportés sous IFNα utilisé pour
le traitement de l’hépatite B, mais pas sous IFNβ (6, 7).
Le traitement du VKH repose sur une corticothérapie au long cours
avec diminution progressive sur 6 mois afi n d’éviter les récurrences
et pour un meilleur pronostic visuel. En cas de récidive malgré un
traitement adéquat par corticoïdes, des traitements immunosup-
presseurs peuvent être nécessaires (ciclosporine, azathioprine,
mycophénolate mofétil, anti-TNF α) [8]. ■
Les auteurs n’ont pas précisé leurs éventuels liens d’intérêts.
1. Absence d’antécédent de traumatisme oculaire ou de chirurgie avant
le début de l’uvéite
2. Absence d’autres pathologies oculaires
3. Atteinte oculaire bilatérale
4. Présence de symptômes neurologiques/auditifs
5. Présence de signes cutanés ne précédant pas le début de la maladie
ophtalmologique ou les manifestations neurologiques
➜ VKH complet si présence des 5 critères ; incomplet si présence des critères
1 à 3 et l’un des quatrième ou cinquième critères, probable si présence
uniquement des critères 1 à 3
Encadré. Critères diagnostiques du VKH.
1. Read RW, Holland GN, Rao NA et al. Revised diagnostic criteria for Vogt-Koya-
nagi-Harada disease: report of an international committee on nomenclature. Am J
Ophthalmol 2001;131(5):647-52.
2. Sakata VM, da Silva FT, Hirata CE et al. Diagnosis and classifi cation of Vogt-Koya-
nagi-Harada disease. Autoimmun Rev 2014;13(4-5):550-5.
3. Damico FM, Cunha-Neto E, Goldberg AC et al. T-cell recognition and cytokine profi le
induced by melanocyte epitopes in patients with HLA-DRB1*0405-positive and nega-
tive Vogt-Koyanagi-Harada uveitis. Invest Ophthalmol Vis Sci 2005;46(7):2465-71.
4. Gu S, Liu Y, Song Z et al. Acute myelitis in a patient with Vogt-Koyanagi-Harada
disease: case report and review of the literature. J Clin Neurol 2013;9(1):61-4.
5. Montero JA, Sanchis ME, Fernandez-Munoz M. Vogt-Koyanagi-Harada syndrome
in a case of multiple sclerosis. J Neuroophthalmol 2007;27(1):36-40.
6. Al-Muammar AM, Al-Mudhaiyan TM, Al Otaibi M et al. Vogt-Koyanagi-Harada
disease occurring during interferon-alpha and ribavirin therapy for chronic hepatitis
C virus infection. Int Ophthalmol 2010;30(5):611-3.
7. Lim JH, Lee YN, Kim YS et al. Vogt-Koyanagi-Harada disease occurring during
pegylated interferon-α2b and ribavirin combination therapy for chronic hepatitis
C. Korean J Hepatol 2011;17(1):61-5.
8. Greco A, Fusconi M, Gallo A et al. Vogt-Koyanagi-Harada syndrome. Autoimmun
Rev 2013;12(11):1033-8.
Références bibliographiques
1
/
4
100%