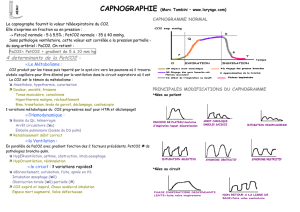
HCO3 - Free

Equilibre Acido-Basique du
sang artériel - Davenport
UE3 PACES - 2011-2012
Pr Bruno CHENUEL

L’équilibre acide-base du sang artériel
Diagramme de Davenport
1) La respiration – échanges gazeux pulmonaires
2) L’équation d’Henderson-Hasselbalch
3) Représentation graphique : le diagramme de Davenport
4) Les troubles de l’état acide-base et leurs compensations

La Respiration :
Définition : Ensemble des phénomènes qui concourent à
assurer les échanges gazeux entre le milieu ambiant et
la cellule vivante.
Permet :
1) de puiser dans le milieu ambiant l’oxygène exigé par
le métabolisme et de le fournir à chaque cellule,
2) d’enlever de chaque cellule le CO2 produit par le
métabolisme et de le rejeter dans le milieu ambiant.
- La « respiration » ne se limite pas à la seule ventilation pulmonaire.
- Elle comprend tous les mécanismes de transfert des gaz (O2 et CO2) et
leur transport sanguin vers et depuis les cellules;
- les mécanismes cellulaires d’utilisation de l’oxygène et de production du
CO2 et des H+ (respiration cellulaire)

Gaz Alvéolaire
Mbne alvéolo-capillaire
Capillaire pulmonaire
CO2!O2!
Sang veineux
mêlé (v)
Sang capillaire
terminal (c’)
Diffusion

Relation liant la ventilation alvéolaire et la pression partielle alvéolaire
de CO2 :
Tout le CO2 rejeté provient de la ventilation alvéolaire
PACO2 = K . VCO2
.
VA
.
Dans la mesure où la production de CO2 est constante, toute augmentation de la
ventilation alvéolaire diminue PACO2 et inversement.
Production métabolique de CO2
(ml.min-1)
Ventilation Alvéolaire
(ml.min-1)
K=863 si V en ml.min-1
.
~ PaCO2 (sang artériel)
Hypocapnie (PaCO2 < Nle)
Hypercapnie (PaCO2 > Nle)
Hyperventilation
Hypoventilation
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
1
/
28
100%