Troubles du rythme et cardiopathies congénitales

22 | La Lettre du Cardiologue • n° 454-455 - avril-mai 2012
DOSSIER THÉMATIQUE
Prise en charge
descardiopathies congénitales
de l’enfant devenu adulte
* Unité de cardiologie congénitale de
l’adulte, hôpital européen Georges-
Pompidou, Paris.
Troubles du rythme
et cardiopathies congénitales
Arrhythmias in adults with congenital heart diseases
E. Barre*, L. Iserin*
L
es troubles du rythme chez les patients atteints
de cardiopathies congénitales sont, par leur
incidence et par leur gravité, des problèmes
majeurs de la prise en charge à l’âge adulte.
En effet, les cicatrices chirurgicales, les surcharges
volumétriques et barométriques sont de nombreux
substrats arythmogènes. C’est la cause la plus
fréquente d’hospitalisation : l’incidence des aryth-
mies auriculaires est de 7 % à l’âge de 20 ans et elle
atteint 38 % à l'âge de 55 ans (1).
Les arythmies auriculaires ont une morbimortalité
élevée (insuffisance cardiaque [IC], détérioration
définitive de la fonction ventriculaire, augmentation
des accidents vasculaires cérébraux [AVC], décès) et
doivent donc être prises en charge de façon agressive.
Troubles du rythme
supraventriculaires
Épidémiologie
La prévalence des troubles du rythme auriculaires
(TDRA) dans cette population est particulièrement
fréquente et augmente avec l’âge et le type de cardio-
pathie. En moyenne, l’incidence est de 10 % dans la
population des patients congénitaux adultes, avec
une incidence de 5 % à 2 ans et de 13,7 % à 5 ans (2).
Pour un âge moyen de 42 ans, J. Bouchardy et al.
rapportent une incidence de 12 % pour les tétralogies
de Fallot (TOF), de 33 % pour les Ebstein, de 18,9 %
pour les communications interauriculaires (CIA), de
28 % pour les transpositions complexes des gros vais-
seaux et de 24,2 % pour les ventricules uniques (1).
Si l’on compare la population des patients congé-
nitaux à la population générale, un adulte âgé de
20 ans présenterait un risque d’arythmie équivalent
à celui d’une femme âgée de 55 ans (3).
Dans 94 % des cas, la tachycardie atriale paroxys-
tique est symptomatique (4), ce qui permet un
dépistage rapide. La morbimortalité des patients
concernés est très élevée : elle augmente de 50 %
la mortalité, l’incidence des AVC et l’insuffisance
cardiaque, et elle triple le risque de chirurgie
cardiaque (1). Le risque de mort subite (MS) sur des
arythmies rapides par défaillance hémo dynamique
ou par complications thromboemboliques concerne
principalement les TOF et les ventricules uniques
palliés par des dérivations cavopulmonaires de type
Fontan.
Physiopathologie
Les substrats arythmogènes sont nombreux chez
les patients congénitaux. Certains sont communs
à ceux de la population générale, mais ils sont
souvent spécifiques et parfois associés, comme dans
la cardiopathie d’Ebstein avec le syndrome de Wolff-
Parkinson-White. Les facteurs favorisants les plus
fréquents sont l’hypertrophie, la fibrose secondaire
à la cyanose chronique, la surcharge volumétrique
ou barométrique chronique, auxquelles s’ajoutent
les cicatrices chirurgicales.
Les arythmies les plus décrites sont le flutter, la fibril-
lation auriculaire (FA) et la tachyardie atriale. Toutes
peuvent s’associer à des dysfonctions sinusales ou
à des blocs de degré variable, ce qui complique les
possibilités de traitement.
Les patients opérés pour une transposition des
gros vaisseaux (TGV) et ayant eu une palliation
par switch atrial (procédure de Senning et Mustard)
développent dans 35 à 50 % des cas, à 15 ans de
suivi, une arythmie atriale due aux nombreuses
cicatrices intra-auriculaires (création de chenaux
pour dériver les veines pulmonaires [VP] dans
E. Barre

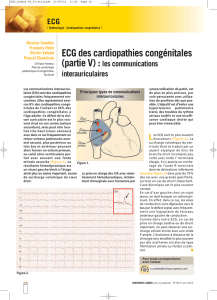
Figure 1. Bloc de
branche droit typique
d’une tétralogie de
Fallot.
La Lettre du Cardiologue • n° 454-455 - avril-mai 2012 | 23
Points forts
Highlights
»
Arrhythmias are common,
particularly supra ventricular
arrhythmia (SVA), symptomatic
and increased the morbid-
mortality.
»
SVA usually complicated TGA
(transposition of great arteries)
with atrial switch, repaired
TOF, Fontan palliation, Ebstein
anomaly and VT (ventricular
tachycardia): repaired TOF and
TGA with atrial switch.
»
Early reduction of arrhythmia
is the basis of the treatment
as well as betabloquers and
sometimes a new surgical inter-
vention. There is no guidelines
about the indication of implant-
able cardiac defibrillator in
primary prevention. On the
contrary of TGA, TOF seems
to have benefits despite the
number of complications and
the young age.
Keywords
Supra-ventricular arrhythmia
Ventricular arrhythmia
Congenital heart disease
Risk factors
Treatment
Mots-clés
Troubles du rythme
supraventriculaires
Troubles du rythme
ventriculaires
Cardiopathies
congénitales
Facteurs de risque
Traitement
»Les troubles du rythme sont graves et fréquents, principalement les troubles supraventriculaires (TSV)
qui sont souvent symptomatiques et augmentent la morbi-mortalité.
»Les TSV compliquent l’évolution des transpositions des gros vaisseaux (TGV) palliées à l’étage auricu-
laire, des tétralogies de Fallot (TOF), des interventions de Fontan, des maladies d’Ebstein. Les troubles
ventriculaires prédominent dans les TOF et les TGV. Le traitement s’appuie sur la réduction précoce, sur les
bêtabloquants, et parfois sur une nouvelle chirurgie. Les indications du défibrillateur automatique implanté
en prévention primaire ne sont pas définies. Contrairement aux TGV, les TOF semblent en bénéficier malgré
les nombreuses complications et leur jeune âge.
l’oreillette droite [OD] et les veines caves dans
l’oreillette gauche [OG]). Les arythmies se majorent
par l’augmentation de la pression intra-auriculaire.
De plus, ce type de chirurgie expose au risque de
dysfonction sinusale (jusqu’à 95 à 98 % des cas à
10 ans postopératoires) [2].
Dans les transpositions anatomiquement corri-
gées des gros vaisseaux, les TDRA alternent avec
les troubles de conduction et sont parfois difficiles
à mettre en évidence. La dilatation de l’OG et la
fuite tricuspide par dilatation du ventricule droit
(VD) systémique ou par anomalie valvulaire sont
les principaux substrats arythmogènes.
Chez les patients opérés d’une TOF, la fuite pulmo-
naire fréquente en postopératoire augmente la
pression télédiastolique ventriculaire droite et, par
conséquent, la pression intra-auriculaire droite.
L’incidence des TDRA est très variable selon les
séries (10 à 30 %). Le diagnostic différentiel avec
une arythmie ventriculaire est parfois difficile en
raison du bloc de branche droit (figure 1).
Dans la cardiopathie d’Ebstein, la surcharge volumé-
trique par la fuite tricuspide, par la dilatation majeure
de l’OD et par le syndrome de Wolff-Parkinson-
White associé chez 5 à 25 % des patients, explique
une incidence des TDRA qui atteint 25 à 40 %.
Dans le canal atrioventriculaire (CAV), les patchs de
fermeture des communications interauriculaires, la
plastie valvulaire et enfin la surcharge volumétrique
créée par l’insuffisance mitrale (préopératoire, voire
postopératoire résiduelle) sont autant de substrats
arythmogènes.
Parmi les cardiopathies congénitales complexes, les
ventricules uniques sont plus sujets aux arythmies
atriales. Pour ces ventricules uniques, les anciens
montages de type Fontan (atriopulmonaires) sont
plus arythmogènes que les nouvelles techniques par
dérivations cavopulmonaires totales (anastomose de
la veine cave supérieure et de la veine cave inférieure
directement sur l’artère pulmonaire) en raison de la
dilatation massive de l’OD.
Quelle que soit la cardiopathie sous-jacente, la
cyanose et l’hypoxie chronique entraînent une
fibrose qui semble jouer un rôle important dans
les arythmies d’origine auriculaire ou ventriculaire.
Facteurs de risque
Les facteurs de risque des tachycardies par réentrée
intra-atriale (flutter) sont les cicatrices chirurgicales
auriculaires, les interventions à un âge tardif et la
durée du suivi.

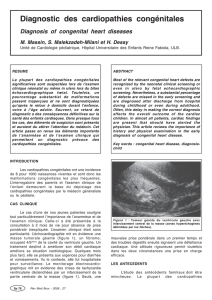
Figure 2. Cartographie d’une arythmie sur un ventri-
cule unique pallié par un Fontan.
24 | La Lettre du Cardiologue • n° 454-455 - avril-mai 2012
Troubles du rythme etcardiopathies congénitales
DOSSIER THÉMATIQUE
Prise en charge
descardiopathies congénitales
de l’enfant devenu adulte
Les cardiopathies les plus à risque sont : les cardio-
pathies ayant eu une intervention de type Fontan ;
les TGV corrigées à l’étage auriculaire, associées
à un haut risque de dysfonction sinusale ; les TOF
opérées en cure complète.
Ces troubles du rythme rapides sont responsables
de MS (jusqu’à 10 % des cas à 6,5 ans de suivi post-
opératoire) [5]. Les principaux facteurs de risque
de MS sur ces tachycardies sont : la cardiopathie
sous-jacente (ventricules uniques, hypertension
artérielle pulmonaire, lésions valvulaires significa-
tives), la classe fonctionnelle NYHA supérieure ou
égale à 3 (4) et les tachycardies mal contrôlées (5).
La FA et les tachycardies atriales sont retrouvées
chez 25 à 30 % des adultes congénitaux. La FA se
manifeste plus souvent en cas de lésion obstructive
résiduelle du cœur gauche, dans les cardiopathies
non réparées et dans les dysfonctions ventriculaires
gauches (4).
Chez les patients congénitaux, le rythme sinusal
doit être privilégié en raison d’un risque de défail-
lance hémodynamique rapide par perte de la
systole auriculaire, en particulier sur les cardio-
pathies du cœur droit et sur les ventricules droits
systémiques (double discordance, TGV palliée
à l’étage auriculaire). Ainsi le schéma habituel
de réduction du TDRA après 3 semaines d’anti-
coagulation ne doit en général pas s’appliquer aux
patients congénitaux dont l'état peut se détériorer
très rapidement pendant cette période, et de façon
irréversible.
La mortalité des TDRA est donc complexe et
multifactorielle : insuffisance cardiaque, MS par
conduction rapide auriculoventriculaire 1 :1 ou
thromboembolique. Réciproquement, l’arythmie
peut survenir à la suite d'une dégradation anato-
mique ou hémo dynamique (surcharge volumé-
trique/barométrique) et précipiter vers l’IC et les
troubles du rythme ventri culaires.
Traitement
◆Le traitement médical
Les réentrées intra-atriales étant particulièrement
difficiles à traiter, certains suggèrent l’emploi des
classes 1C sous réserve de leur potentiel aryth-
mogène et de leur effet dépresseur sur la fonction
ventriculaire et sur la fonction sinusale. Les médi-
caments le plus souvent utilisés sont donc les
bêtabloquants et les antiarythmiques de classe 3
(amiodarone surtout, malgré ses nombreux effets
indésirables chez des patients jeunes).
◆La place du pacemaker
L’implantation d’un pacemaker peut être utile
lorsque la dysfonction sinusale limite le traite-
ment médicamenteux. Elle peut entraîner plusieurs
problèmes :
➤
l’accessibilité au cœur (en cas de dérivation
cavopulmonaire, pas de voie endocavitaire possible,
sténose ou occlusion du chenal cave dans les Senning
et Mustard). La pose de sondes par voie épicardique
doit alors être envisagée ;
➤
la perméabilité des voies d’abord chez des
patients opérés à plusieurs reprises ;
➤
la difficulté, parfois, à obtenir des seuils satisfai-
sants, conséquences de la fibrose étendue ;
➤
et enfin, la multiplication des sondes et des
changements de boîtiers (implantation à un jeune
âge), qui accroît les risques infectieux et throm-
botiques.
Certains pacemakers de nouvelle génération
proposent une fonction "défibrillation atriale qui
pourrait être particulièrement intéressante chez
ces patients".
◆L’ablation
Les succès d’ablation des réentrées intra-atriales
par radiofréquence varient de 50 à 90 % selon les
séries. En général, les ablations ciblent des circuits
isolés de macroréentrées. Chez les patients avec
une valve auriculoventriculaire droite, l’isthme est
souvent le siège de la réentrée de façon similaire à
un flutter commun. Ainsi, les interventions de type
Mustard et Senning, les réparations de TOF et autres
réparations biventriculaires peuvent théoriquement
bénéficier de cette technique. Toutefois, les circuits

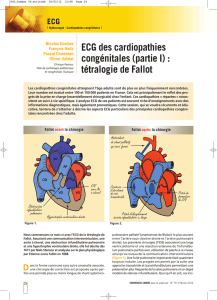
Figure 3. ECG de double discordance : bloc auriculoventriculaire complet et activation
septale droite.
La Lettre du Cardiologue • n° 454-455 - avril-mai 2012 | 25
DOSSIER THÉMATIQUE
sont souvent multiples, difficiles à cartographier,
et nécessitent des procédures longues et risquées
(zones d’ablation larges et confluentes) [figure 2].
Leur suivi à long terme a montré une amélioration
significative des symptômes et de la qualité de vie
des patients, mais les rechutes surviennent dans
presque 50 % des cas.
◆Le traitement chirurgical
La survenue d’une arythmie atriale doit faire rééva-
luer l’hémodynamique du patient. Une chirurgie
visant à restaurer l'hémodynamique doit aussi
comporter une procédure antiarythmique (de type
Maze, isolation des VP).
On sait que ces réinterventions chirurgicales
peuvent être à haut risque chez les adultes porteurs
de cardiopathies congénitales (10 % pour les
Fontan).
Troubles de conduction
Dysfonction sinusale
Les cardiopathies les plus atteintes sont les Fontan et
les TGV corrigées à l’étage auriculaire, conséquence
des nombreuses cicatrices chirurgicales.
Pour certaines cardiopathies, la dysfonction sinusale
s’explique par une anomalie embryologique des voies
de conduction (les hétérotaxies, anomalies de latéra-
lisation droite-gauche, dont les plus fréquentes sont
les doubles discordances). Les tachycardies atriales
paroxystiques sont fréquemment associées à ces
anomalies du nœud sinusal, ce qui augmenterait
le risque de MS.
Blocs auriculoventriculaires
Les anomalies de conduction interventriculaires sont
très fréquentes, principalement en postopératoire
et à type de blocs de branche droits.
Ils peuvent être favorisés par des anomalies
préexistantes de la conduction (cf. supra). Les plus
fréquentes sont secondaires aux chirurgies de levée
d’obstruction du cœur gauche et à celle des inver-
sions ventriculaires. La chirurgie du canal atrioven-
triculaire, celle du septum interventriculaire, voire
celle de l’Ebstein sont aussi à risque.
Les blocs auriculoventriculaires (BAV) peuvent ne
pas être liés à la chirurgie (BAV congénitaux, immu-
nologiques ou évolutifs de la double discordance)
[figure 3].
Ils peuvent aussi s’intégrer dans des syndromes
comme le syndrome de Holt-Oram, qui associe
des troubles conductifs pouvant évoluer pour leur
propre compte à des anomalies de la septation (CIA
et communication interventriculaire [CIV] parfois
multiples) et à des anomalies des membres supérieurs.
Troubles du rythme
ventriculaires
Épidémiologie et physiopathologie
La MS est une cause fréquente de décès dans cette
population jeune : 26 % (4). Les principales cardio-
pathies à risque de MS sur une tachycardie ventri-
culaire (TV) sont :
➤
la TOF, sur le patch de fermeture de CIV et sur la
cicatrice, voire sur le patch infundibulaire (figures 4
et 5, p. 26). Les TDRV sont un peu moins fréquents
que les TDRA (14,6 % versus 20,1 %) [6], mais ils ont
une incidence de 1 à 2 % tous les 5 ans ;
➤la TGV palliée à l’étage auriculaire : le risque de
MS est d’environ 4 % à 10 ans et de 9 % à 20 ans.
La MS chez ces patients est surtout liée aux TDRA
rapides. Le substrat des tachycardies ventriculaires
est aujourd’hui mal connu, mais elles sont souvent
coexistantes ou précédées de TRSV ;
➤
les sténoses aortiques, liées à l’hypertrophie
myocardique et à l’obstruction.
Facteurs de risque
De nombreux facteurs de risque ont été identifiés
comme prédictifs de TV et de MS. Dans les TOF,

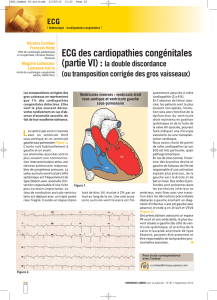
Figures 4 et 5. Cartographie d’une tachycardie ventriculaire autour du patch infundibulaire dans une TOF (à droite), pièce anatomopathologique d’une
réparation de TOF (à gauche) avec la présence des 2 patchs (ventriculaire et infundibulaire), substrats de la majorité des TV.
AP : artère pulmonaire ; inf : infundibulum ; TV : tachycardie ventriculaire ; VD : ventricule droit ; VG : ventricule gauche.
Patch inf
Patch inf
VD
AP
CIV patch
VG
VD
TV
26 | La Lettre du Cardiologue • n° 454-455 - avril-mai 2012
Troubles du rythme etcardiopathies congénitales
DOSSIER THÉMATIQUE
Prise en charge
descardiopathies congénitales
de l’enfant devenu adulte
la diminution de la fonction systolodiastolique du
VD, sa dilatation, la présence d’un obstacle résiduel
avec une pression intraventriculaire droite élevée, la
dysfonction ventriculaire gauche associée à une frac-
tion d'éjection du ventricule gauche inférieure à 30 %
sont des facteurs prédictifs indépendants (4). L’âge
de la réparation, le nombre de chirurgies cardiaques,
particulièrement les antécédents de shunts systé-
micopulmonaires palliatifs, une durée de QRS supé-
rieure ou égale à 180 ms, ainsi que l’âge du patient
sont également des facteurs prédictifs de MS (5).
Dans les TGV corrigées à l’étage auriculaire, les
facteurs prédictifs de TV sont : la dysfonction du
ventricule systémique sous-aortique, une classe
fonctionnelle NYHA supérieure ou égale à III, des
QRS supérieurs ou égaux à 140 ms (7) et les anté-
cédents de troubles supraventriculaires (TSV) [8].
La fibrose du VD mise en évidence à l’IRM par réhaus-
sement tardif et la diminution de la consommation
d’oxygène (pic inférieur à 36 %) sont corrélées à la
mortalité et sont à rechercher (9).
Traitement
◆Le traitement médical
Aucun traitement antiarythmique n’a montré une
amélioration de la survie des patients (5).
Les bêtabloquants sont toutefois très utilisés pour
leur propriétés antiarythmiques, pour allonger
la période réfractaire nodale, mais aussi pour
augmenter le temps de remplissage diastolique
et diminuer l’ischémie (8). Les classes 1C sont à
proscrire, principalement en cas de dysfonction
ventriculaire.
◆La place du défibrillateur automatique
implantable
L’hétérogénéité des cardiopathies congénitales et la
petite population ne permettent pas, aujourd’hui,
la rédaction de recommandations pour la pose d’un
défibrillateur automatique implantable (DAI) en
prévention primaire.
Dans les TGV palliées à l’étage auriculaire, le nombre
de chocs appropriés après l'implantation en prévention
primaire est faible (4,3 % sur 3,5 ans versus 28,6 %
pour les DAI implantés en prévention secondaire) [8],
et celui de chocs inappropriés est élevé (21,7 % pour
les implantations en prévention primaire versus 28,6 %
pour les implantations en prévention secondaire).
Dans les TOF, l’implantation en prévention primaire
semble justifiée selon les critères précédemment
décrits. P. Khairy et al. rapportent un taux de
chocs appropriés annuel de 7,7 % en prévention
primaire versus 9,8 % en prévention secondaire, au
regard de 5,8 % de chocs inappropriés par an (10).
 6
6
1
/
6
100%