UNIVERSITE DES SCIENCES ET DE LA TECHNOLOGIE HOUARI

REPUBLIQUE ALGERIENNE DEMOCRATIQUE ET
POPULAIRE
MINISTERE DE L’ENSEIGNEMENT SUPERIEUR ET DE LA RECHERCHE
SCIENTIFIQUE
UNIVERSITE DES SCIENCES ET DE LA TECHNOLOGIE
HOUARI BOUMEDIENE (U.S.T.H.B)
FACULTE DES SCIENCES BIOLOGIQUES (FSB)
MEMOIRE DE FIN D’ETUDES
En vue de l’obtention du diplôme d’ingéniorat d’Etat en Biologie
Soutenu publiquement le 27.06.2009 devant le jury :
Mme Touil-Boukoffa C. Présidente
Mme Mezioug D. Promotrice
Mr Ahmedi M. Examinateur
Melle Belguendouz H. Examinatrice
Melle Bouaziz S. Invité

A Madame le professeur Touil-Boukoffa C.,
directrice du laboratoire de Biologie Cellulaire et Moléculaire (B.C.M) et de l’équipe cytokines et
NO Synthases à la Faculté des Sciences Biologiques (F.S.B/ U.S.T.H.B), pour nous avoir accueilli au
laboratoire, pour l'intérêt qu'elle a manifesté pour ce travail et pour nous avoir fait honneur d’accepter
la présidence de notre Jury de mémoire.
Nous lui présentons notre Hommage respectueux.
A Mademoiselle Mezioug D.,
enseignant-chercheur en biochimie-immunologie au laboratoire de Biologie Cellulaire et Moléculaire
et membre de l’équipe cytokines et NO Synthases à la Faculté des Sciences Biologiques, qui nous
suit depuis les prémices de ce travail, Avec toujours la même disponibilité et attention.
Nous la prions de croire à notre profonde gratitude et à notre respectueux attachement.
A Monsieur Ahmedi M.,
chargé de cours à la Faculté des Sciences Biologiques et membre de l’équipe cytokines et NO
Synthases au laboratoire de Biologie Cellulaire et Moléculaire, qui nous a fait l’honneur d’accepter
de participer à notre jury de mémoire, avec la spontanéité et la gentillesse qui le caractérisent.
A Mademoiselle Belguendouz H.,
maître assistante en biochimie-immunologie au laboratoire de Biologie Cellulaire et Moléculaire à la
Faculté des Sciences Biologiques et membre de l’équipe cytokines et NO Synthases, pour avoir
accepté d’examiner notre travail.
Nous leurs témoignons ici notre sincère reconnaissance.
A Mademoiselle Bouaziz S.,
assistante en biochimie-immunologie au laboratoire de Biologie Cellulaire et Moléculaire et de
l’équipe cytokines et NO Synthases à la Faculté des Sciences Biologiques, pour ses renseignements
et orientations.
Nous sommes heureux de vous voir participer à ce jury et vous assurons de notre gratitude.
A toute l’équipe des cytokines et NO Synthases,
Ce stage a été rendu très agréable par l’ambiance que vous savez faire régner au sein de l’équipe.
Merci pour vos précieux conseils.

Je dédie ce modeste travail à mes très chers parents, qui n’ont cessé de m’encourager et qui ont
toujours donné le meilleur d’eux même pour me voir réussir. Que dieux vous protège et vous garde à
nos cotés.
A toute ma famille à laquelle je témoigne toute mon affection.
A mes amis(es) qui m’ont soutenu tout au long de mon cursus universitaire.
A tout le personnel du centre hospitalo-universitaire de Tizi-Ouzou, qui m’ont aidé et orienté avec
leurs précieux conseils.
A tous ceux qui ont croisé mon chemin et qui ont participé de prêt ou de loin à la réalisation de ce
travail.

Introduction générale………………………………………………….……………………….1
Chapitre I : RAPPELS BIBLIOGRAPHIQUES
I.A. Hydatidose
I.A.1. Définition de l’hydatidose……………………………………………………………....3
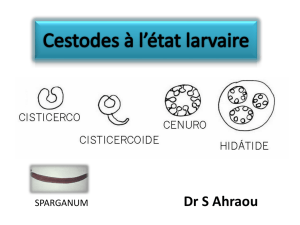
I.A.2. Formes du parasite…………………………………………………...………………….4
I.A.3. Cycle biologique……….. .………………………………………………….…………..9
I.A.4. Epidémiologie et zones d’endémie………………………….…………………………10
I.A.5. Antigènicité de l’hôte…………………………………………………………………..12
I.A.6. Diagnostic radiologique et bilan biologique…………………………………………...12
I.A.7. Réponse immunitaire..............................................................................................…...14
I.A.8. Traitement……………………………………………………………………………...15
I.A.9. Prophylaxie…………………………………………………….………………………15
I.B. Les cytokines
I.B.1. Caractéristiques générales des cytokines…………………………………...………….17
I.B.2. Réseau des cytokines…………………………………………………...……………...21
I.B.3. Transduction du signal par les récepteurs des cytokines……………………………....23
I.B.4. Les cellules T auxiliaires……………………………………….………………...........25
I.B.5. Cytokines en pathologie et en applications thérapeutiques…………………...……….27
I.B.6. Cytokines et hydatidose…………………………………….………………………….28
I.C. Le monoxyde d’azote (NO)
I.C.1. Définition………………………………………………………………………………30
I.C.2. Propriétés physico-chimiques du NO.………………………………………………...31
I.C.3. Biosynthése du NO…………………………………………………………………….31
I.C.4. Isoformes de la NOS……………………………………………………….….……….32
I.C.5.Types de régulation des NOS………………………………………………………......34
I.C.6. NO et cytokines…………………………………………………………………...…...34
I.C.7. NO et systèmes immunitaires………………………………………………………….35
I.C.8. Effets du NO…………………………………………………………………………...35
Chapitre II : MATERIELS ET METHODES
II.A. Matériels………………………………………………………………………….……..36
II.A.1. Matériel non biologique………………………………………………………………36
II.A.2. Matériel biologique……………………………………………………………….......36
II.B. Méthodes………………………………………………………………………..……….38
II.B.1. Test de viabilité des protoscolex……………………………………………………....38
II.B.2. Dosage des protéines par la méthode de BRADFORD…………………………….…38
II.B.3. Isolement des PBMC…………………………………………………………………40

II.B.4. Dosage des nitrites totaux par la méthode de Griess modifiée………………………..42
Chapitre III : RESULTATS ET DISCUSSIONS
III.1. Dosage des protéines par la méthode de Bradford……………………………………...47
III.2. Test de viabilité des protoscolex………………………………………………………..46
III.3. Dosage des nitrites dans les cultures des PBMC induites par les antigènes et l’extrait des pépins
de raisin………………………………………………………..………………….49
Chapitre IV :CONCLUSION………………………………………………………………56
Chapitre V : BIBLIOGRAPHIE………………………...…………………………………57
ANNEXES……………………………………………………………………………………62
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
 70
70
 71
71
 72
72
 73
73
 74
74
 75
75
 76
76
 77
77
 78
78
 79
79
1
/
79
100%