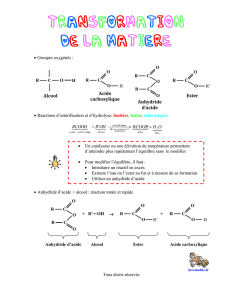
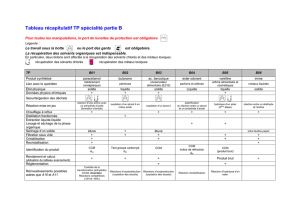
synthèse d`un arôme, la vanilline

Correction : synthèse d'un arôme: la vanilline
1. Le chauffage permet d'augmenter la vitesse de la réaction. Le reflux permet de
prolonger le contact entre les réactifs en recondensant les vapeurs qui voudraient
s'échapper.
2.a L'utilisation d'un anhydride impose de travailler avec une verrerie parfaitement
sèche car il peuvent réagir violemment avec l'eau. La manipulation doit se faire sous la
hotte avec utilisation de gants et de lunettes.
2.b On utilise l'anhydride éthanoïque à la place de l'acide éthanoïque car il permet
d'avoir une réaction totale au lieu d'une réaction limitée par l'hydrolyse de l'ester.
3. L'acide orthophosphorique catalyse cette synthèse. Il augmente la vitesse de la
réaction en remplaçant une réaction lente par plusieurs réactions rapides. Il est consommé
puis régénéré et n'entre donc pas dans le bilan de la réaction.
4. A = CH3-COOH C'est l'acide éthanoïque
5. L'acétate d'isoeugénol est insoluble dans l'eau glacée. Il précipite donc, ce qui permet
de l'isoler.
6.a
(nanhydride)0 =
mol
M
Vd
M
V
M
m
anhydride
eauanhydride
anhydride
anhydride
anhydride
anhydride 212,0
102 0,2000,108,1
...
(nisoeugénol)0 =
isoeugénol
isoeugénol
M
m
=
mol0610,0
164
0,10
6.b
L'anhydride est en excès.
(nester)formé si réaction totale = (nisoeugénol)0 = 0,0610 mol
(nester)formé =
mol
M
m
ester
ester 0551,0
205
3,11
Rendement de la synthèse =
0
0
...
3,90100
0610,0 0551,0
100
)(
)(
totaleréactionsiforméester
forméester
n
n

Partie B: troisième étape - synthèse de la vanilline
1. B = CH3-COOH C'est l'acide éthanoïque
2. Cette réaction correspond à l'hydrolyse d'un ester.
3. On peut déplacer l'équilibre dans le sens de la formation de la vanilline en :
- ajoutant un excès de réactif, eau ou acétate de vanilline.
- en éliminant le produit le plus volatil au fur et à mesure de sa formation (distillation)
afin d'éviter que la réaction inverse qui limite la réaction directe ne se produise.
1
/
2
100%