Chébaro Alexandre Arzul Vincent 21/03/11 Cancérologie Pr Karine

Chébaro Alexandre
Arzul Vincent
21/03/11
Cancérologie
Pr Karine Tarte
BASES BIOLOGIQUES DE
L’IMMUNOTHERAPIE DES CANCERS
Introduction :
Pourquoi l’immunologie a-t-elle un rôle primordial en oncologie ?
On sait aujourd’hui que tous les cancers sont capables de générer une réponse anti-tumorale de
l'organisme, s’initiant dans les ganglions drainant la tumeur. Les LT cytotoxiques vont dans la
tumeur pour la détruire. On peut visualiser expérimentalement le modèle immunologique:
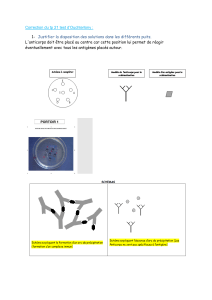
Expérience chez la souris :
Injection d’une tumeur portant de l’ovoalbumine (marqueur), la tumeur est verte car on y a ajouté
du GFP (green fluorescence protein) , et injection de LT et de lymphocytes anti-OVA reconnaissant
la tumeur.
On regarde alors à quel endroit les LT prolifèrent. Prolifération des cellules T dans les ganglions
drainant la tumeur, mais pas dans les autres ganglions. Les LT activés migrent ensuite vers la
tumeur pour aller la détruire.
Donc quand injection de LT spécifiques de la tumeur : ils détruisent la tumeur. Ce sont
des T anti-tumoraux qui s’amplifient au niveau du ganglion et détruisent la tumeur.
Expérience chez l’homme :
Patients atteints d’un cancer colo-rectal .
Quelles sont les cellules présentes dans la tumeur ? On regarde dans la tumeur la signature
immunologique par PCR (gènes codant pour CD8, facteurs Th1, Th2...) et si la présence de ces
gènes est corrélée à l’état métastatique ou à la rechute.
On remarque que plus il y a de T cytotoxiques et de Th1 dans la tumeur, moins il y a de rechutes et
moins il y a de métastases, donc meilleur est le pronostic.
Donc si on a une réponse T cytotoxique efficace dans la tumeur, elle favorise l’éradication de la
tumeur.
On a bien la preuve que in vivo chez l’homme, la réponse immunologique a un rôle important à
jouer en oncologie. On veut donc amplifier cette réponse immunologique.

I. L’immunothérapie :
Il en existe 3 types :
l’immunothérapie passive
l’immunothérapie adoptive
l’immunothérapie active
A. L’immunothérapie passive (anticorps) :
Utilisation d’anticorps dirigés contre des antigènes exprimés à la surface de l’ensemble des
cellules tumorales :
de façon stable : il ne doit pas y avoir de variation de l’expression au cours de la
maladie
de façon homogène : toutes les cellules tumorales doivent exprimer l’antigène
et le plus spécifique possible : pour qu’il n’y ait pas de destruction des cellules non
cancéreuses.
Les anticorps sont toujours les immunoglobulines G1 (IgG1).
Pendant longtemps, on a travaillé avec des anticorps murins (de souris). Problème :l’homme
s’immunise contre cet anticorps reconnu comme étranger, et lors de la deuxième injection,
l’anticorps est totalement éliminé.
Révolution de l’utilisation des anticorps : les anticorps chimères (60-70%humain) : seule la
partie variable est murine, la partie constante est d’origine humaine. Donc moins
d’immunisation et une meilleure interaction avec les effecteurs de l’immunité (récepteurs Fc
des macrophages par exemple). La partie constante est d’origine humaine, elle est donc
moins immunogène.
Les anticorps humanisés (90-95% humain) : seules les régions hypervariables (CDR) sont
d’origine murine, tout le reste est d’origine humaine. A peu près équivalent aux anticorps
chimères.
B. L’immunothérapie adoptive (effecteurs) :
On transfère des effecteurs au patient :
LT conventionnels (a, b, cytotoxiques…)
LT non conventionnels (NK)
Leur but est de détruire directement la tumeur.
C. L’immunothérapie active: (induction d’une réponse immunitaire in vivo)
Injection de l’antigène sous forme immunogène, soit avec des adjuvants, soit directement
sur des cellules dendritiques.

II. L’immunothérapie passive : Les anticorps anti-
tumeur :
Ils sont utilisés dans beaucoup de cancers et marchent bien. Cependant, ils font partie des dix
médicaments les plus chers sur le marché.
Exemple : Anti-CD20 et Lymphomes :
Les lymphomes touchent les LB exprimant CD20, les patients développent des anticorps antiCD20.
CD20 :
expression stable
sur tous les LB, normaux ou tumoraux
absent des plasmocytes (heureusement car sinon on tuerait toutes les cellules
productrices d’anticorps) et des cellules souches hématopoïétiques (CD34) : donc,
on garde la mémoire immunologique des plasmocytes long survivants de la moëlle, et
de plus il y a préservation de l’hématopoïèse.
Anticorps anti-CD20 :
Rituximab (MabThera®), le plus fréquent, a été utilisé au moins une fois chez tous les
patients ayant un lymphome.
Zevalin (couplé avec un radioélément : Yttrium 90) .
Mécanisme d’action :
lyse par les cellules NK : les NK fixent le Rituximab par CD16 et lysent la cellule tumorale.
Néanmoins, chez quelques patients, l’efficacité est faible : en effet 20% des personnes
ont un polymorphisme pour CD16, et CD16 peut être moins affin pour les IgG, donc
la réponse au traitement est moins bonne.
c’est une IgG donc elle active aussi le complément : lyse par le complément.
cytotoxicité directe faible (elle active directement la mort de la cellule) .
possibilité de synergie avec la chimiothérapie .
L’efficacité est liée à la densité de CD20 : plus il y a de CD20 et meilleure est l’efficacité du
traitement. .
Ce traitement est beaucoup utilisé dans les lymphomes.
IV. L’immunothérapie adoptive :
A. Les TIL : Lymphocytes Infiltrant la Tumeur :
Histoire ancienne :
En 1985, premiers essais d’injection d’IL-2 chez des patients atteints de cancer : efficacité
clinique.
En 1988, premiers essais TIL (mélanomes et cancers du rein).
Problème : pas d’efficacité large quand les essais son faits sur un grand nombre de patients.

Actualité : regain d’intérêt
On sait que le traitement marche dans certains cas :
faible masse tumorale (exemple : après chirurgie) .
capacité d’expansion in vivo : quand on injecte des LT, il faut qu’ils puissent
se multiplier donc on fait une lymphodéplétion au préalable avec une drogue
de chimiothérapie afin de détruire les LT du patient pour que ces LT (TIL)
aient la place de se multiplier in vivo en utilisant les cytokines et les facteurs
de croissance du patient.
coinjection TCD4 et TCD8, car si on injecte seulement des T cytotoxiques,
on n’a pas de mémoire immunologique, donc il faut aussi des TCD4 .
ces protocoles peuvent marcher car il y a des épitopes spreading : en effet, les
LT détruisent la tumeur qui libère alors des antigènes, ceux-ci génèrent alors
une seconde réponse immunitaire et ainsi de suite… C’est une dissémination
antigénique, et la réponse immunitaire est dirigée contre d’autres antigènes
que ceux que l’on a injecté au départ.
plusieurs protocoles en cours (Nantes, USA)
B. Les Tγδ :
Il existe deux grands types de stratégies :
Soit on prend les cellules sanguines du malade avec T.d. On les cultive in vitro avec
BrHPP qui est un analogue de l’IPP et des IL2. Les T.d s’amplifient et on les réinjecte chez
le patient..

La deuxième technique est encore plus simple. On injecte directement au malade BrHPP
et Il2 donc l’amplification se fait in vivo.
Ces deux stratégies sont utilisées dans des cancers hématologiques. L’objectif est la
destruction des cellules tumorales.
C. Les NK allogéniques, application à la LAM (leucémie aigue
myéloide) :
Les NK sont difficiles à faire proliférer, il ne suffit pas de mettre de l'IL2 pour les faire proliférer.
On enleve les TCD3, on met de l'IL2, cela donne une prolifération des NK que l'on va injecter au
patient.
La deuxième possibilité est que l'on enlève les TCD3, on purifie les NK puis on les fait proliférer,
cette méthode est en cours d'étude donc on ne connait pas les résultats encore.
D. Immunothérapie adoptive+Ac, l'ADCC redirigée:
Leur multiplication in vitro est difficile.
Intérêt théorique : associer les NK avec un anticorps anti-tumeur pour avoir une ADCC. Il faut
donc une cellule capable d’ADCC.
Innovation:
On transfert CD16 dans un LT anti EBV
ADCC efficace et réactivation possible par EBV.
 6
6
 7
7
 8
8
 9
9
1
/
9
100%