Télécharger le poster

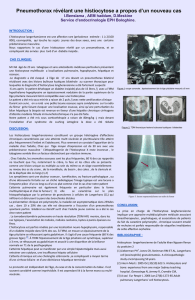
IMAGERIE DES
HISTIOCYTOSES
LANGERHANSIENNES DE
L’ADULTE
C. Lacombe¹, C. Viala², M. Lewin¹, M Svrcek³,
P Cervera³, L. Monnier-Cholley¹, A. Belkacem¹,
C. Pradel¹, L. Arrivé¹, J. Cabane² et JM. Tubiana¹
¹Service de radiologie, hôpital Saint-Antoine, Paris
² Service de médecine interne, hôpital Saint-Antoine, Paris
³ Service d’anatomopathologie, hôpital Saint-Antoine, Paris

INTRODUCTION
• Les histiocytoses constituent un groupe de maladies
chroniques hétérogènes caractérisées par une
atteinte multiviscérale et pluritissulaire. Elles sont
divisées en 3 groupes:
–Histiocytoses langerhansiennes (objet du poster)
–Histiocytoses non langerhansiennes :les plus connues sont la
maladie de Whipple, d’origine infectieuse, les maladies de
Gaucher et de Niemann-Pick, héréditaires, et la maladie
d’Erdheim-Chester, à expression sporadique, d’étiologie
inconnue
–Histiocytoses malignes, très rares. Elles se rapprochent plutôt de
la famille des hémopathies malignes.

DEFINITIONS
•L’histiocytose à cellules de Langerhans (HL), également appelée
histiocytose X ou granulomatose à cellules de Langerhans regroupe
plusieurs syndromes dont la caractéristique commune est
histologique : infiltration tissulaire par des cellules de Langerhans
organisées en granulomes.
•On distingue cliniquement 3 formes
–Formes unitissulaires, localisées, de relativement bon pronostic,
intéressant surtout l’adulte
–Formes pluritissulaires, multifocales (syndrome de Hand-Schüller-
Christian) concernant le grand enfant ou l’adolescent, mais également
l’adulte, de novo, ou dans le cadre d’une forme pédiatrique passée à la
chronicité.
–Formes disséminées (syndrome de Letterer-Siwe) qui sont plutôt des
formes pédiatriques (nourrisson), généralement gravissimes.
• La sémiologie radiologique pour un même organe est la même, que
la forme soit uni ou pluritissulaire.

PATHOGENIE
• L’origine de l’HL est inconnue, sans agent étiologique identifié.
Néanmoins, il existe un lien étroit entre le tabagisme et la forme
pulmonaire isolée d’HL, suggérant un rôle pathogène du tabac.
• Plusieurs équipes considèrent l’HL comme une maladie clonale,
bénigne dans la plupart des cas, mais l’hypothèse immunitaire
n’est pas exclue.
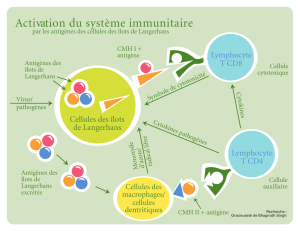
• Certains facteurs impliqués dans la pathogénie de l’HL ont été
individualisés :
– Les cellules de Langerhans secrètent du GM-CSF, facteur essentiel
pour la prolifération cellulaire.
– L’interleukine 17, dont il existe des récepteurs partout dans
l’organisme, apparaît également impliquée dans la maladie,
expliquant ainsi le caractère polymorphe des manifestations.

ANATOMOPATHOLOGIE
La lésion élémentaire de l’HL est un granulome où les cellules de Langerhans sont
associées à une quantité variable d’éosinophiles, de lymphocytes, de neutrophiles, de
macrophages, de fibroblastes et de cellules géantes aux propriétés ostéoclastiques
(nombreuses dans les lésions osseuses ostéolytiques).
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
1
/
34
100%