La protéine amyloïde sérique A

Diagnostic
Update
Juin 2015
La protéine amyloïde sérique A :
un biomarqueur sensible pour la détection des
réactions inflammatoires du cheval et du chat
L‘identification comme le suivi des processus inflammatoires
représentent souvent un défi en médecine vétérinaire. Les
symptômes cliniques sont la plupart du temps non spéci-
fiques et les modifications causées par l‘inflammation au
sein de l‘organisme ne sont pas toujours détectables lors de
l‘examen clinique général. La détection d‘une concentration
élevée de protéine amyloïde sérique A (SAA) dans le sang
permet non seulement de déceler une inflammation systé-
mique, mais aussi d‘assurer un suivi fiable de l‘évolution et
de la thérapie. Il s‘agit en outre d‘une analyse facile à intégrer
à l‘examen clinique.
La réaction de phase aiguë
La réaction de phase aiguë (RPA) est constituée d‘une cas-
cade très complexe de réactions immédiates déclenchées
par l‘organisme en réponse à des lésions tissulaires. Il s‘agit
d‘un mécanisme de défense inné qui va dans le sens d‘une
réponse non spécifique aux lésions tissulaires. La RPA est
déclenchée par diverses causes comme une infection bac-
térienne, virale ou parasitaire, un processus néoplasique, un
traumatisme, une brûlure, etc.
Les cellules et les tissus endommagés libèrent des média-
teurs (acide arachidonique ou radicaux libres oxygènés par
exemple) qui conduisent à l‘activation des monocytes, des
macrophages et du stroma. Ceux-ci produisent à leur tour
des médiateurs de l‘inflammation, notamment des cytokines
(IL-1, IL-6 ou TNF-α) qui ont un effet endocrine et paracrine
local, et propagent la RPA dans l‘organisme. C‘est à la fin de
cette cascade de réactions que sont produites les protéines
de phase aiguë (PPA) (fig. 1). La RPA vise à éliminer la cause
du phénomène nocif, à favoriser le processus de guérison et
à rétablir l‘homéostasie.
Les protéines de phase aiguë
Les protéines de phase aiguë (PPA) sont principalement syn-
thétisées par les hépatocytes. En cas de RPA, leur concen-
tration varie d‘au moins 25 % par rapport au niveau basal.
Les PPA remplissent différentes fonctions parmi lesquelles:
activation du complément et phagocytose par opsonisation
des agents infectieux, chimiotactisme des monocytes, des
neutrophiles et des cellules T, modulation de la réaction
inflammatoire, etc.
Fig. 1 :
représentation schématique de la réaction de phase aiguë
Inhibition
Cellules de
Kupffer Cortisol
Cortisol
Tissu extra-hépatique,
épithélium par exemple Hépatocytes
Les protéines de phase aiguë
Lésion tissulaire et activation
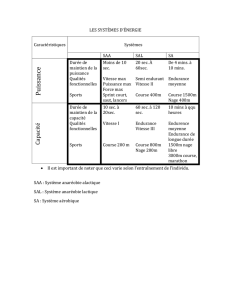
En cas de RPA, la concentration de certaines PPA peut aug-
menter ou diminuer. Elles sont par conséquent réparties en
deux groupes: les PPA positives et les PPA négatives. Dans
le cadre d‘une RPA, les PPA positives peuvent à nouveau
être divisées en deux catégories selon leur dynamique et leur
concentration sérique (tableau 1).
Les protéines de phase aiguë positives peuvent être soit
majeures soit modérées, en fonction de l‘espèce animale
considérée. La protéine amyloïde sérique A est une PPA
majeure chez le cheval comme chez le chat.
Endotoxine Agent pathogène Traumatisme/lésion Cancer
Monocyte Stroma
Endothélium
Muscle
Dégradation
tissulaire
Leucocytes
Activation
Moelle osseuse
Leucopoïèse
Hypothalamus
Fièvre
Axe HPA
Glandes
surrénales
Cortisol
Cytokines (IL-1, IL-6, TNFα)

Les protéines de phase aiguë comme
biomarqueurs
La détection des PPA et d‘autres paramètres comme mar-
queurs permettant d‘évaluer les processus inflammatoires
fait depuis de nombreuses années l‘objet de recherches et
a déjà été appliquée en médecine humaine et vétérinaire.
Le biomarqueur idéal des réactions inflammatoires doit :
• présenter des caractéristiques permettant une évaluation
fiable et dynamique de l‘état du patient,
• présenter une concentration sérique très faible chez le sujet
sain et, si possible, ne pas être influencé par des facteurs
intrinsèques comme le sexe ou la race,
• indiquer une réponse mesurable rapide et marquée, en
rapport avec le déroulement de l‘inflammation (i.e. para-
mètre fiable pour le suivi thérapeutique),
• être facilement mesurable.
La protéine amyloïde sérique A comme
biomarqueur des processus inflammatoires
La protéine amyloïde sérique A (SAA) est un biomarqueur
sanguin sensible des lésions tissulaires et des réactions
inflammatoires. Sa concentration montre un comportement
très dynamique en relation avec le degré d‘inflammation et
de lésion. Comparée à d‘autres PPA comme le fibrinogène,
la SAA est un paramètre représentatif de l‘inflammation plus
pertinent car en cas de RPA, sa concentration augmente de
manière plus rapide et plus marquée. Cette augmentation
est directement liée à l‘ampleur de la lésion tissulaire ou de
l‘inflammation et reflète son évolution. En outre, la SAA a une
demi-vie très courte et est dégradée par la clairance hépa-
tique en 30 minutes à 2 heures après synthèse. Ainsi, sa con-
centration diminue très vite dès le début de la récupération.
En cas de récidive ou de complication secondaire, (infection
post-chirurgicale par exemple), la concentration
de SAA augmente à nouveau.
Les tableaux 2 (cheval) et 3 (chat) récapitulent les patho-
logies et troubles où une augmentation de la concentration
de la SAA peut être observée.
La protéine amyloïde sérique A
chez le cheval
Infections bactériennes et virales : la concentration san-
guine de SAA augmente quelques heures à peine après le
début de l‘infection. Cette augmentation est plus forte pour les
infections bactériennes que pour les infections virales. Le niveau
Les protéines de phase aiguë positives : Leur concentration sanguine augmente en cas de RPA. Ce groupe rassemble la
plupart des PPA (notamment la SAA et le fibrinogène).
Les protéines de phase aiguë majeures
• Chez les sujets sains, les concentrations sanguines sont
très faibles.
• Au cours de la RPA, ces concentrations augmentent
d‘un facteur 10 à 100, voire 1000, comme c‘est le cas
par exemple de la SAA chez le chat ou le cheval.
• L‘augmentation est rapide (fenêtre de 12 à 24 h) et une
diminution s‘observe après quelques jours.
Les protéines de phase aiguë modérées
• Chez les sujets sains, les concentrations sanguines sont
déjà plus élevées.
• Au cours de la RPA, ces concentrations augmentent d‘un
facteur 2 à 10 ; c‘est notamment le cas du fibrinogène.
• Les concentrations augmentent moins vite et stagnent
plus longtemps.
Les protéines de phase aiguë mineures
Leurs concentrations augmentent d‘un facteur inférieur à 2.
Les protéines de phase aiguë négatives :
leurs concentrations sanguines diminuent au cours de la RPA ; c‘est par exemple le cas de l‘albumine.
Augmentation de la concentration sérique de SAA
dans divers processus et pathologies du cheval
Pathologie
Infections
bactériennes
Arthrite septique
Septicémie du poulain
Pneumonie (Rhodococcus equi)
Gourme
Abcès
Infections post-chirurgicales
Infections virales EHV-1 (poulain, cheval adulte)
Virus de la grippe
Tractus gastro-
intestinal
Colique
Diarrhée et entérite
Péritonite
Parasitose
Reproduction Mise bas (augmentation
physiologique chez la jument)
Avortement septique
Avortement de cause inconnue
Poulains
(autres causes)
Rétention de méconium
Syndrome de désadaptation
Mise bas difficile (traumatique)
Post-opératoire
augmentation due
à une intervention
chirurgicale sans
complications)
Castration
Laryngoplastie
Ovariectomie
Arthroscopie
Tableau 2
Tableau 1 : les catégories de protéines de phase aiguë

d‘augmentation de la concentration de SAA ne donne aucune
indication sur l‘agent pathogène. Le suivi de l‘évolution de cette
concentration permet toutefois un suivi thérapeutique chez
certains patients. En outre, en cas d‘infection épizootique dans
l‘écurie (EHV S. equi equi), la détermination de la concentration
de SAA peut servir à la détection des cas d‘infection subclinique.
En cas d‘inflammations focales (abcès intra-abdominal par
exemple), la concentration de SAA peut éventuellement rester
dans la plage des valeurs usuelles.
Pathologies néonatales : une augmentation de la concentra-
tion sanguine de SAA chez le poulain nouveau-né peut indiquer
aussi bien une infection aiguë que chronique ou une septicémie.
Il y a cependant des études contradictoires concernant la con-
centration sanguine de SAA en cas de transfert passif inadéquat,
d‘isoérythrolyse, de syndrome de désadaptation ou de rétention
du méconium. En cas d‘infections focales (abcès ombilical par
exemple), la concentration de SAA peut rester dans la plage des
valeurs usuelles.
Interventions chirurgicales : une augmentation biphasique
de la concentration de SAA postopératoire a été rapportée chez
le cheval. La longueur de l‘incision et l‘ampleur des lésions tis-
sulaires dues à la chirurgie influent sur la réaction inflammatoire
physiologique. Après une castration, la concentration de SAA
maximale est observée deux ou trois jours après l‘intervention ;
une deuxième augmentation peut survenir après 4 à 5 jours. Une
augmentation persistante de cette concentration peut indiquer
une infection postopératoire.
Maladies respiratoires : une augmentation de la concentration
de SAA a été rapportée chez le cheval dans certaines maladies
infectieuses des voies respiratoires (tableau 2). Il n‘a toutefois
pas été clairement établi si les maladies respiratoires d‘origine
allergique ou à médiation immune s‘accompagnent ou non
d‘une telle augmentation.
Amyloïdose : les processus inflammatoires récidivants accom-
pagnés d‘une augmentation de la concentration de SAA peuvent
conduire à une amyloïdose systémique réactive. Cette maladie
peut conduire à la mort de l‘animal.
La sécrétion de PPA (SAA par exemple) est une réaction non
spécifique survenant en cas de RPA. La concentration de SAA
sert au suivi de la réaction inflammatoire dans l‘organisme ;
elle ne permet cependant pas de poser un diagnostic étiolo-
gique spécifique.
Il convient d‘éviter de faire travailler le cheval durant la phase
de convalescence si la concentration de SAA n‘est pas reve-
nue dans la plage des valeurs usuelles.
Quels sont les facteurs pouvant influer sur
la concentration de SAA chez un cheval en
bonne santé ?
Le sexe : la concentration de SAA chez le cheval ne varie pas
en fonction du sexe de l‘animal.
L‘âge : en principe, l‘âge n‘a aucune influence sur la concen-
tration de SAA chez le cheval. Il existe toutefois des études
contradictoires quant à une augmentation légère au cours des
2 premières semaines de vie. Celle-ci débuterait 72 heures
après la mise bas, probablement en réponse aux processus
inflammatoires liés à la naissance et à l‘effort physique qu‘elle
représente, ou au transfert de SAA via le colostrum. Il convient
donc de considérer d‘un œil critique les légères augmentations
de la concentration de SAA chez le nouveau-né au cours de la
période mentionnée ci-dessus ; la détermination de la concen-
tration à intervalles réguliers peut être une aide précieuse pour
mieux cerner l‘état de santé du poulain.
La gestation : la concentration de SAA chez la jument peut
augmenter légèrement vers la fin de la gestation, pour des
raisons physiologiques. La concentration diminue de nouveau
environ 1 mois après la mise bas. La concentration de SAA ne
peut pas être utilisée pour poser un diagnostic de gestation.
La protéine amyloïde sérique A chez le chat
Infections : quel que soit l‘agent pathogène en cause, une
infection peut conduire à de très fortes concentrations de
SAA. Même si l‘on admet que les infections bactériennes
provoquent des hausses plus importantes que les infections
virales, des augmentations particulièrement fortes ont été
rapportées chez les chats atteints de péritonite infectieuse
féline cliniquement déclarée.
Inflammations : les essais d‘induction expérimentale aussi
bien que les études cliniques ont montré que différents types
d‘inflammations systémiques conduisent chez le chat à une
augmentation importante de la concentration de SAA. Dans
un rapport de cas portant sur un chat atteint de pancréatite
aiguë nécrosante, la concentration de SAA était corrélée à
l‘évolution clinique et plus exactement à la récidive de la ma-
ladie. Elle s‘avérait supérieure à la numération leucocytaire
Augmentation de la concentration sérique de SAA
dans divers processus et pathologies du chat
Pathologie
Inflammation Pancréatite
Traumatisme/lésion
Intervention chirurgicale
Études
expérimentales
Lipopolysaccharide bactérien,
essence de térébenthine
Maladie virale PIF
Processus
néoplasique
Tumeur à cellules rondes
Mésothéliome malin
Carcinome
Sarcome
Endocrinopathie Hyperthyroïdie
Diabète sucré
Autres Maladie polykystique
Néphropathie chronique
Maladie des voies urinaires
inférieures du chat
Tableau 3

Diagnostic
Update
une élévation du taux d‘interleukine 6 a été observée chez les
patients atteints d‘hyperthyroïdie et de polykystose rénale. En
outre, il a été établi que la SAA est libérée non seulement par
le foie, mais aussi par d‘autres organes comme les reins et la
thyroïde.
Amyloïdose : la SAA est le précurseur de l‘amyloïde A et peut
jouer un rôle dans le développement d‘une amyloïdose systé-
mique. Des études antérieures évoquent des chats abyssins
atteints d‘amyloïdose simple et présentant des concentrations
de SAA plus élevées que celles observées chez des sujets sains
de même race ou des sujets malades de race différente.
Quels sont les facteurs pouvant influer
sur la concentration de SAA chez un chat
en bonne santé ?
Le sexe : les études existantes font état de résultats contradic-
toires quant à l‘influence du sexe sur la concentration de SAA. La
plupart n‘établissent pas de différence liée au sexe ou n‘évoquent
pas explicitement cet aspect. Une seule étude a mis en avant un
taux de SAA plus élevé chez les femelles malades. Il n‘est pas
possible de tirer de conclusion quant à des concentrations
généralement plus élevées chez les femelles saines.
L‘âge et la race : une étude a mis en avant des concentrations
de SAA plus élevées chez le chat âgé (de plus de 5 ans) par
rapport au chat jeune et en bonne santé. Toutefois, leur état de
santé n‘avait été établi qu‘à partir des antécédents et d‘un exa-
men clinique. Les auteurs ne peuvent donc exclure que les diffé-
rences de concentration observées soient causées par une plus
grande incidence des maladies subcliniques dans le groupe des
animaux plus âgés. À ce jour, aucune étude ne s‘est penchée
sur une éventuelle différence de concentration de SAA entre les
différentes races chez le chat sain.
La gestation : il n‘existe pour le moment aucune étude sur la
concentration de SAA pendant les différentes étapes de la gesta-
tion chez le chat.
totale ainsi qu‘à l‘immunoréactivité trypsinogène sérique
comme paramètre pour l‘évaluation de l‘état du patient.
Les sujets atteints de gastroentérite et de bronchopneu-
monie ne montrent que peu ou pas d‘augmentation de la
concentration de SAA.
Toutefois, le nombre de cas est trop faible pour permettre une
généralisation. La formation d‘un foyer focal et la chronicité des
maladies sont des causes possibles. En cas de maladie hépa-
tique d‘origine inflammatoire, on considère que l‘absence d‘une
forte augmentation de la concentration de SAA est due à une
capacité de synthèse limitée.
Processus néoplasiques : chez certains chats atteints de
tumeurs, on peut observer une forte augmentation de la concen-
tration de SAA. Ce phénomène a été observé pour les carcino-
mes, les sarcomes, les mésothéliomes malins et les lymphomes.
Interventions chirurgicales : des études ont montré que chez les
chats pour lesquels le type exact de castration n‘a pas été spéci-
fié, ainsi que chez les chats ayant subi une ovariohystérectomie,
on observe une augmentation de la concentration de SAA entre
3 et 6 (voire 8) heures après l‘opération ! Les pics de concentra-
tion interviennent à 21 – 24 heures et 48 heures respectivement
après l‘opération ; puis la concentration diminue de nouveau
pour revenir dans les valeurs usuelles le quatrième jour après
l‘intervention. On considère donc que chez le chat aussi, une
augmentation persistante de cette concentration peut indiquer
une infection postopératoire ou une complication.
Autres : il est également possible d‘observer une augmentation
de la concentration de SAA chez les chats atteints d‘endocrino-
pathies (hyperthyroïdie, diabète sucré par exemple) et d‘autres
maladies non inflammatoires (néphropathie chronique, polykysto-
se rénale). On considère que l‘augmentation de la concentration
de SAA est en fait causée par des infections sous-jacentes et/ou
des lésions de l‘endothélium vasculaire. En médecine humaine,
IDEXX Diavet AG
Schlyffistrasse 10
8806 Bäch (SZ)
www.idexx.ch
Conseil spécialisé
Tel: 044 786 90 20
Dr. Cécile Rohrer Kaiser
Dipl. ACVIM, ECVIM-CA
Tel: 044 380 28 61
Fax: 044 380 28 62
Tous les noms de marque cités sont la propriété d’IDEXX Laboratories, Inc. ou de sociétés affiliées aux États-Unis et/ou dans d’autres pays.
La déclaration de confidentialité d’IDEXX peut être consultée sur le site www.idexx.ch
© 2015 IDEXX Laboratories. Inc. Tous droits réservés · 1505007-0615-CH/FR
Test IDEXX de la protéine amyloïde sérique A
Espèces : chat, cheval
Échantillon : 0,3 ml de sérum (aucun plasma)
Durée du test : 1 jour après réception de l‘échantillon
au laboratoire
Méthode : test d’agglutination au latex
Disponible en test individuel et en tests additionnels aux
bilans.
Documentation sur demande par e-mail à l’adresse [email protected]
Autoren
Dr. med. vet. Anastasios Moschos, Vétérinaire
Responsable grands comptes cheval
Consultant scientifique Vétérinaire FEI IDEXX Laboratories
Dr. med. vet. Stephanie Nather, Vétérinaire
Vétérinaire spécialisée dans les petits animaux
Responsable grands comptes petits animaux
Consultante scientifique, IDEXX Laboratories
1
/
4
100%