20/10/2014 LANDRIOT Fanny L2 CR : Julie Chapon TSSI Pr

Tissu sanguin et système immunitaire – Les groupes sanguins érythrocytaires
20/10/2014
LANDRIOT Fanny L2
CR : Julie Chapon
TSSI
Pr Jacques Chiaroni
16 pages
les groupes sanguins érythrocytaires – applications en transfusion sanguine
Les objectifs pédagogiques de ce cours :
–Décrire les principaux antigènes et anticorps des groupes sanguins érythrocytaires.
–Prescrire les analyses pré-transfusionnelles adéquates
–Comprendre et appliquer les règles de compatibilité érythrocytaire en vue d'assurer la sécurité immuno-
hémolytique des transfusions
1/16
Plan
A. Les groupes sanguins érythrocytaires
I. Définitions de la notion de groupes sanguins
II. Pourquoi en tenir compte en transfusion sanguine ?
III. Qu'est ce qu'un groupe sanguin ? Combien y en a t'il ?
IV. Quels antigènes ?
V. Le système ABO
VI. Les systèmes protéiques
VII. A quoi servent les groupes sanguins ? A quoi servent ces différents polymorphismes
VIII. Existe-t-il une répartition géographique préférentielle ? Quels facteurs peuvent contribuer à
cette répartition ?
B. Groupes sanguins et sécurité transfusionnelle
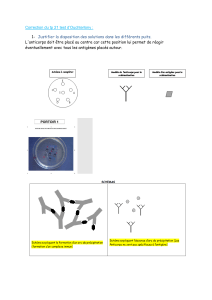
I. Comment éviter la rencontre ?
II. Les analyses pré-transfusionnelles
III. Choisir l'unité adéquate
a. Éviter le conflit dans le système ABO chez tout le monde
b. Les règles de compatibilité dans les autres systèmes
IV.Maîtriser l'acte transfusionnel
C. Conséquences de la rencontre
I. Conséquences biologiques
II. Conséquences cliniques
D. Diagnostic de la rencontre

Tissu sanguin et système immunitaire – Les groupes sanguins érythrocytaires
A. Les groupes sanguins érythrocytaires
I. Définition de la notion de groupes sanguins
Dans l'expression « groupe sanguin » on retrouve le terme de groupe et l'adjectif sanguin. On parle donc ici d'un
ensemble d'individus qui possèdent un caractère commun au niveau du sang.
Il faut bien comprendre que la notion de groupes sanguins est extrêmement large. Elle comprend le
polymorphisme génétique qui est si étendu que en dehors des vrais jumeaux chacun d'entre nous a un profil
génétique unique. On introduit alors la notion de solitude biologique.
Cette notion a été largement exploités par exemple en médecine légale (scène de crime), pour connaître un
profil génétique...
On va s'intéresser dans ce cours uniquement aux variations qui peuvent être présentes sur le globule rouge.
Définition du groupe sanguin érythrocytaire :
Ceux sont des antigènes (AG) définis par des anticorps(AC) spécifiques et génétiquement induits (ne
changent pas au cours de la vie) et exprimés sur des molécules de la membrane érythrocytaire.
II. Pourquoi en tenir compte en transfusion sanguine ?
Les groupes sanguins érythrocytaires sont immunogènes (capacité à induire une réponse immunitaire).
Ils s'opposent donc à la transfusion incompatible et même grossesse incompatible (lorsque le fœtus a un
groupe sanguin différent de sa mère, les AC de la mère vont attaquer le fœtus et conduire à son décès ; c'est le
cas notamment quand la mère est Rhésus – et l'enfant Rhésus +).
L'introduction d'un antigène érythrocytaire « étranger » va entraîner la synthèse de l'anticorps correspondant. Si
on réintroduit l'antigène, il va y avoir fixation de l'anticorps sur l'antigène, ce qui condamne l'hématie transfusée
à la destruction. On a donc une hémolyse.
Les conséquences de cet accident transfusionnel sont doubles :
→ persistance du besoin transfusionnel, car le manque de globules rouges n'est pas corrigé.
→ nocivité du conflit immunologique, qui peut aller jusqu'à tuer le malade.
La transfusion incompatible est non seulement inefficace, mais elle va aggraver l'état du patient.
Pour garantir la sécurité immunologique des transfusions de globules rouges, il faut éviter la rencontre in vivo
entre antigène et anticorps !
III.Qu'est un groupe sanguin ? Combien y en a-t-il ?
Un groupe sanguin peut être défini comme une étiquette portée par nos GR.
Les individus qui portent la même étiquette appartiennent au même groupe sanguin.
2/16

Tissu sanguin et système immunitaire – Les groupes sanguins érythrocytaires
Les étiquettes A et B sont donc codées par 2 allèles d'un même gène et appartiennent à un même ensemble. Cela
forme un système : ici le système ABO.
Rappels :
♦ Allèle : « variante d'un gène »
♦ Système : « gène qui va coder pour les différentes formes alléliques »
A coté du système ABO il existe de nombreux autres systèmes.
Il y a par exemple le Rhésus
→ si vous avez l'étiquette « Rhésus » D → vous êtes rhésus positif
→ si vous n'avez pas l'étiquette « Rhésus »D → vous êtes rhésus négatif
En plus ces étiquettes s’accumulent :
→ si vous avez l'étiquette A et l'étiquette rhésus → vous êtes A positif
→ Si vous avez l'étiquette A et pas l'étiquette rhésus → vous êtes A négatif
Ainsi de suite avec les 350 étiquettes qui ont été décrites sur le globule rouge (GR).
IV. Quels antigènes ?
Il y a 350 antigènes (AG) présents sur l globule rouge, regroupés en 35 systèmes.
On peut classer ces AG selon leur caractéristiques biochimiques.
Les sucres :
► Ce sont des produits secondaires des gènes. En effet un gène code pour des protéines et non des sucres. Il
faut donc un intermédiaire (une enzyme).
Le système ABO fait parti de cette catégorie.
En 1900 : classement de personnes prises au hasard par groupes sanguins A, B, O ou AB.
En 1929 : classement en prenant des familles => on se rend compte que les groupes sanguins sont codés
génétiquement (A et B dominent O et sont co-dominants entre eux).
Dans les années 60, on se rend compte que les caractères A et B sont des sucres. Ils ne peuvent pas être transmis
génétiquement !!
Après des recherches ils se sont rendus compte de l'intervention
d'enzymes (codés génétiquement) qui permettaient l'insertion de ces
sucres sur le GR.
3/16

Tissu sanguin et système immunitaire – Les groupes sanguins érythrocytaires
► Ils sont ubiquitaires dans l'organisme
► Ils sont largement répandus dans la nature
► Ce sont des anticorps « naturels » : ils apparaissent en dehors d'une transfusion car leur production est
stimulée par l'environnement.
D'autres espèces que l'homme expriment le système ABO : les primates... mais aussi les bactéries ! Notamment
les bactéries intestinales : Nous sommes donc constamment stimulés par d'autres Ag que nous, et nous allons
fabriquer des Ac contre ces Ag que nous n'avons pas (une personne ayant un Ag A fabriquera des Ac anti B)
Les protéines :
Tous les autres systèmes sont des protéines
►Ce sont des produits primaires
►Il existe des équivalents dans d'autres tissus de l'organisme
►Ils ont une tendance à une restriction humaine (on ne les trouve pas chez d'autres êtres vivants)
►On les a appelé les anticorps « immuns », et il n'apparaissent qu’après stimulation interhumaine
(transfusion, ou grossesse incompatible)
Tous les systèmes, de manière plus ou moins intense, peuvent être impliqués dans une incompatibilité
transfusionnelle.
Comment fait on pour avoir une transfusion « parfaite »?? cela paraît presque impossible !!
Heureusement il y a 6 systèmes constitués de 14 antigènes qui permettent d'assurer une compatibilité d'environ
95% :
6 systèmes 14 antigènes
ABO A - B
RH D / C-c , E-e
KEL K
Duffy Fya - Fyb
Kidd Jka - Jkb
MNS S - s
Grâce à des analyses on va pouvoir déterminer la compatibilité entre 2 personnes :
–l'analyse ABO.D qui consiste à rechercher les Ag A -B et D
–le phénotype RH.K qui consiste à rechercher les Ag C-c, E-e et K
–le phénotype Étendu qui consiste à rechercher les Ag Fya-Fyb, Jka-Jkb, S-s
Mais ces analyses restent incomplètes pour assurer une bonne compatibilité, il faut donc à coté de ces analyses
d'Ag détecter les Ac présents chez le patient :
–la recherche d'anticorps irréguliers RAI
4/16

Tissu sanguin et système immunitaire – Les groupes sanguins érythrocytaires
V. Le système ABO
Il contient 2 antigènes : A et B
Ce sont des sucres, donc des produits secondaires des gènes.
Le gène code pour une enzyme qui pose A ou B sur un antigène appelé H et qui est déjà sur le globule rouge.
L'antigène H est donc converti en A (groupe A) ou converti en B (groupe B) ou non converti (groupe O).
Chez un individu de groupe O, ce gène code soit pour rien, soit pour une enzyme qui ne marche pas. Donc sur
le globule rouge de l'individu de groupe O, on a un antigène H sans A ni B, c'est-à-dire non converti.
Du phénotype, on ne peut pas toujours déduire le génotype.
Ex : pour un phénotype « groupe A », le génotype sera A/A ou A/O
L'absence d'antigène H (phénotype Bombay) empêche l'expression des antigènes A et/ou B, même si les gènes
sont là. Ce phénotype est très rare, présent surtout en Inde et ressemble donc au phénotype O.
Les antigènes de ce système ont une maturation post-natale. C'est-à-dire qu'il y a une augmentation du
nombre d'antigènes après la naissance. Cela est lié au fait que l'enzyme mature après la naissance.
2 conséquences :
→ Ce phénomène explique que l'incompatibilité foeto-maternelle ABO soit moins grave que l'incompatibilité
foeto-maternelle rhésus.
ex : si la mère est O et l'enfant est A => la mère a des anticorps qui peuvent traverser le placenta et
détruire les globules rouges du fœtus. Mais comme il y a maturation post-natale, c'est comme si il y
avait moins de cibles pour les anticorps sur les globules rouges du fœtus.
Ce n'est pas le cas pour le rhésus où les antigènes apparaissent très tôt.
→ La validation définitive du groupe ABO d'un nouveau-né ne peut se faire qu'après l'âge de 6 mois.
Le système ABO est largement répandu dans la nature : ubiquité dans l'organisme et dans la nature :
–les gènes A et B sont actifs dans toutes les cellules de l'organisme.
–le gène H est actif dans les cellules endothéliales.
Les Anticorps du système ABO :
L'antigène n'existe que parce que l'anticorps spécifique à cet antigène existe.
Les anticorps du système ABO sont les anticorps anti-A et anti-B.
Ils ont 2 caractéristiques principales :
–ils sont « naturels »
◦ ils préexistent à toute stimulation inter-humaine
◦ ils sont nés de l'hétérostimulation (bactéries du tube digestif)). C'est une stimulation environnementale,
possible du fait de l'ubiquité environnementale du système ABO
5/16
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
1
/
16
100%