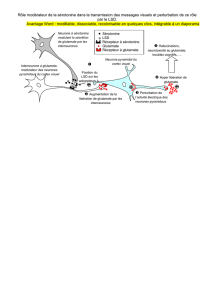
regulation des transporteurs vesiculaires du glutamate chez les

THESE DE DOCTORAT DE L’UNIVERSITE PARIS XII
Spécialité
Neurosciences
Présentée par
Jacqueline GILCHRIST-VINATIER
Pour obtenir le grade de
DOCTEUR de l’UNIVERSITE PARIS XII
Sujet de la thèse :
REGULATION DES TRANSPORTEURS
VESICULAIRES DU GLUTAMATE
CHEZ LES RONGEURS
Soutenue le 9 janvier 2006
Devant le jury composé de :
Dr Bruno Giros Directeur de Thèse
Dr Bruno Gasnier Rapporteur
Dr Nicole Ropert Rapporteur
Dr Dominique Aunis Examinateur
Pr Romain Gherardi Examinateur
Dr Anne Schmidt Examinateur

REMERCIEMENTS
Le travail présenté dans cette thèse a été réalisé dans le laboratoire de Bruno Giros, sous sa
direction scientifique. Il est donc naturel de commencer avec celui par qui tout a commencé…
Je tiens à te remercier pour la grande confiance que m’a témoignée depuis le début sur ce projet
ambitieux, ainsi que pour ta créativité qui fût le moteur de cette grande aventure.
Bruno Gasnier, Nicole Ropert, Anne Schmidt, Dominique Aunis et Romain Gherardi m’ont fait
l’honneur de juger ce travail, malgré un emploi du temps souvent surchargé. Je vous suis
reconnaissante de votre participation à mon jury de thèse et de vos commentaires, qui ne
pourront qu’enrichir mon travail.
Mes débuts dans la recherche et dans l’unité 513 ont été encadrés par Marie-Pascale Martres. Je
tiens à te témoigner toute ma gratitude pour ta disponibilité au cours de mon DEA et pour ta
relecture attentive de ce manuscrit lorsqu’il était en préparation.
Salah El Mestikawy m’a adoptée pour me faire découvrir l’univers des VGLUTs et m’a fourni
un encadrement tout au cours de ces années. Merci d’avoir su m’intégrer dans ton équipe et me
faire profiter de ta grande expérience de la paillasse. Etienne Herzog, Christelle Gras, Margot
Bournaud, Bénédicte Amilhon, Eve Lepicard et Odile Poirel ont tous contribué au succès de
mes travaux sur les VGLUTs. Je remercie également Marie-Aude Plamont, sans qui mon projet
« endophiline » n’aurait sans doute pas abouti…
De nombreuses collaborations ont permis de faire avancer mes projets, et je suis reconnaissante
à tous ceux avec qui j’ai travaillé, de près ou de moins près, pour mener à bien ces études. En
particulier, je tiens à remercier Laurent Daviet de la societé Hybrigenics, Anne Schmidt, Bruno
Gasnier, Agnès Hémar, Véronique Bernard, Patricia Gaspar, Sonja Wojcik, Nils Brose pour leur
aide.

RESUME
Les transporteurs vésiculaires du glutamate, VGLUT1, -2 et -3, sont des protéines localisées sur
la membrane des vésicules synaptiques des neurones glutamatergiques. Ils sont responsables de
l’accumulation du neuromédiateur dans les vésicules. VGLUT1 et VGLUT2 sont les sous-types
majoritaires dans le cerveau et ils sont exprimés dans la totalité des neurones glutamatergiques
avec des profils d’expression complémentaires. VGLUT3 est exprimé de façon plus discrète,
dans des populations de neurones contenant d’autres neuromédiateurs dont on ne suspectait pas
jusqu'alors qu'ils pouvaient être glutamatergiques.
Au cours de cette thèse, j’ai participé à la description détaillée de la localisation de VGLUT3
dans le cerveau adulte de rat, ainsi qu’à l’étude de l’ontogenèse des trois sous-types. Alors que
l'expression de VGLUT2 est assez précoce, l'ARNm et la protéine VGLUT1 sont exprimés plus
tardivement puisque le profil d’expression adulte n’apparaît que vers le 21ème jour post-natal.
Pour VGLUT3, nous avons pu mettre en évidence des expressions ectopiques très élevées dans
des territoires dont il est totalement absent à l'âge adulte, comme les cellules de Purkinje du
cervelet.
Avec pour lointain objectif de pouvoir identifier des différences fonctionnelles entre VGLUT1,
-2 et -3, j’ai également réalisé un crible double-hybride avec l'extrémité C-terminale
cytoplasmique de VGLUT1. J’ai ainsi caractérisé l’interaction entre VGLUT1 et l’endophiline,
une protéine impliquée dans l’endocytose des vésicules synaptiques. Cette interaction se fait
entre l’un des deux domaines riches en prolines de VGLUT1 et le domaine SH3 de
l'endophiline. Les territoires d'expression dans le cerveau, ainsi que les compartiments
cellulaires dans lesquels sont présents VGLUT1 et l'endophiline sont compatibles avec une
interaction in vivo. Cette interaction suggère un lien fonctionnel entre l’accumulation de
neuromédiateur et le recyclage des vésicules synaptiques dans la terminaison nerveuse.
L'ensemble de ces résultats nous permet de considérer que, loin d'être des acteurs passifs de la
neurotransmission, les transporteurs vésiculaires du glutamate, chacun avec ses caractéristiques
spécifiques, interviennent de manière contrôlée au cours du développement, puis établissent des
profils d'expression prédéterminés chez l'adulte. De plus, ils jouent un rôle important dans la
dynamique synaptique générale, même si ce rôle n'est pas encore totalement élucidé.

PREAMBULE
En 1999, dans une revue sur les vésicules synaptiques, T. Südhof expliquait son approche de la
neurobiologie de la synapse en ces termes : « We discuss nerve terminal function from the
perspective of synaptic vesicles (…) The overall goal is a systematic analysis of an eukaryotic
organelle to completion (…) The working hypothesis is that synaptic vesicles are composed of a
limited number of proteins that perform distinct, identifiable functions. » (Fernandez-Chacon et
Sudhof, 1999). Des progrès considérables sur la compréhension de la transmission synaptique
ont découlé de l’ensemble des travaux décrits dans cette revue.
Après avoir disséqué d’un point de vue moléculaire la synapse et avoir cloné et muté la plupart
des protéines impliquées dans la transmission synaptique, le défi du 21ème siècle sera d’avoir une
vision dynamique de la synapse. Il faut désormais relier les molécules synaptiques avec la
physiologie de la synapse.
Lorsque j’ai démarré ce travail de thèse, la caractérisation moléculaire des transporteurs
vésiculaires du glutamate venait d’être réalisée. L’existence de trois sous-types a tout de suite
suscité de nombreuses questions, dont celles sur sont les différences fonctionnelles entre
VGLUT1, -2 et-3 qui n’étaient pas des moindres. Jusqu’à présent, aucune différence notable n’a
été trouvée dans les proprietés de transport de glutamate, ni dans les caractéristiques
bioénergétiques ou pharmacologiques. Par contre, il existe d’importantes différences de
localisation entre les transporteurs : VGLUT1 et VGLUT2 ont une répartition largement
complémentaire dans le cerveau et sont exprimés dans tous les neurones connus pour utiliser le
glutamate comme neuromédiateur. La découverte de VGLUT3 a donc été une surprise puisque
ce dernier sous-type n’est pas exprimé dans des neurones considérés jusqu’alors comme
glutamatergiques.
Le travail entrepris au cours de ces quatres années a donc eu pour objectif de comprendre les
régulations de la transmission synaptique apportées par les transporteurs vésiculaires du
glutamate et aurait pu s’intituler : « à la recherche d’une diversité fonctionnelle entre les
neurones glutamatergiques ».
Plusieurs axes d’étude ont été entrepris :
- l’étude de VGLUT3, sous-type atypique car il n’est pas exprimé dans neurones considérés
comme glutamatergiques : étude de sa localisation détaillée et étude de son expression au cours
du développement. Les travaux présentés dans les parties I et II sont des études anatomiques des
VGLUTs dans le cerveau de rat.
- la recherche de partenaires protéiques pour VGLUT1. La partie III concerne donc la biologie
cellulaire des VGLUTs et établit un lien avec le recyclage des vésicules synaptiques.

SOMMAIRE
INTRODUCTION _____________________________________________________________ 8
I/ La synapse chimique ________________________________________________________ 9
I.1/ La structure de la synapse chimique__________________________________________________9
I.2/ Les principaux neuromédiateurs du système nerveux central _____________________________11
I.3/ Les étapes de la transmission synaptique _____________________________________________14
I.4/ La clathrine et les protéines accessoires ______________________________________________19
II/ Les transporteurs vésiculaires du glutamate comme marqueurs de la
transmission glutamatergique ________________________________________________24
II.1/ Le métabolisme du glutamate _____________________________________________________24
II.2/ Les récepteurs et les transporteurs plasmiques du glutamate _____________________________25
II.3/ Les transporteurs vésiculaires du glutamate __________________________________________30
II.4/ Anatomie des systèmes glutamatergiques____________________________________________36
III/ Les modulations de la transmission nerveuse : la plasticité synaptique à
l'échelle d'une synapse ______________________________________________________45
III.1/ Plasticité pré-synaptique et plasticité post-synaptique__________________________________45
III.2/ Régulation de la quantité de neuromédiateur dans les vésicules synaptiques ________________46
III.3/ Régulation du type de neuromédiateur : co-transmission _______________________________49
III.4/ Régulation du recyclage des vésicules synaptiques ____________________________________50
RESULTATS _________________________________________________________________58
Partie I :étude de la répartition anatomique de VGLUT3 dans le cerveau de
rat adulte
Contexte de l’étude _________________________________________________________________60
Principaux résultats_________________________________________________________________60
Conclusion _______________________________________________________________________61
Partie II : étude de l’ontogenèse des VGLUTs au cours du développement
post-natal
Contexte de l’étude _________________________________________________________________82
Principaux résultats_________________________________________________________________82
Conclusion _______________________________________________________________________83
Partie III : étude de l’interaction entre VGLUT1 et une protéine impliquée
dans l’endocytose, l’endophiline
Contexte de l’étude _________________________________________________________________96
Principaux résultats_________________________________________________________________96
Résultats complémentaires ___________________________________________________________97
Conclusion _______________________________________________________________________98
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
 70
70
 71
71
 72
72
 73
73
 74
74
 75
75
 76
76
 77
77
 78
78
 79
79
 80
80
 81
81
 82
82
 83
83
 84
84
 85
85
 86
86
 87
87
 88
88
 89
89
 90
90
 91
91
 92
92
 93
93
 94
94
 95
95
 96
96
 97
97
 98
98
 99
99
 100
100
 101
101
 102
102
 103
103
1
/
103
100%