Contrôle génétique de la réponse immune à Plasmodium falciparum

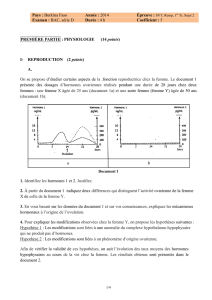
Florence Migot-Nabias
UMR 216 «Mère et enfant face aux infections tropicales»
IRD, Paris
Contrôle génétique de la réponse immune
àPlasmodium falciparum
12 mars 2011

Existence d’une régulation génétique des
réponses immunitaires spécifiques du paludisme
ÊDifférences ethniques, familiales et individuelles des
réponses immunitaires contre P. falciparum, dans des
conditions d’exposition identiques
ÊConcordance plus importante entre jumeaux monozygotes
que dizygotes:
9Pour le développement de fièvre lors d’un accès palustre: régulation
génétique des cytokines pyrogènes
9Pour la production d’anticorps dirigés contre différents antigènes
plasmodiaux

Plusieurs systèmes de contrôle génétique
ÊPolymorphisme érythrocytaire
9Trait drépanocytaire
9Alpha-thalassémie
9Déficit en G6PD
ÊComplexe Majeur d’Histocompatibilité (CMH)
ÊPolymorphismes de gènes de cytokines
ÊAllotypes d’immunoglobulines
ÊMécanismes de l’immunité innée
Ê…

Polymorphisme érythrocytaire & paludisme
ÊProtection clinique
9Trait drépanocytaire, alpha-thalassémie, déficit en G6PD, ovalocytose, groupe
sanguin ABO, groupe Duffy négatif
ÊMécanismes proposés
9Modification des antigènes érythrocytaires de surface favorisant la
reconnaissance immunitaire (alpha-thal)
9Sensibilité accrue au stress oxydant favorisant la phagocytose des
parasites (déficit G6PD)
9Ralentissement de la croissance parasitaire dans les hématies anormales
(Hb S)
9Facilitation (groupe A) ou limitation (groupe O) de la formation de rosettes
ÊAutres polymorphismes érythrocytaires moins directement
liés à la protection
9Hb C, Hb E, béta-thalassémie, récepteur du complément CR1

Distributions comparées du paludisme et de
l’hémoglobine S en Afrique
L’Afrique regroupe plus de 80% des cas de
décès par paludisme à P.falciparum
G Périquet, Univ. Tours
Hémoglobine S:
Mutation ponctuelle au locus des βglobines:
- Hémoglobine AS: trait drépanocytaire
- Hémoglobine SS: drépanocytose
SI Hay et al., PLoS Medicine 2010
Endémicité mondiale de P. falciparum en 2007
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
1
/
38
100%