recueil de pratiques professionnelles en soins palliatifs

Recueil de Pratique Professionnelle
en Soins Palliatifs
Version 3 : 6 février 2006
Coordination : G. Laval, M-L. Villard
Comité de rédaction
C. Armari-Alla, C. Arvieux, E. Bardonnenche, D. Barnoud, P. Basset, S. Batier, C. Belleville, S. Bergé,
E. Berland, M. Besson, N. Beuriot, B. Boillot, P.Y. Brard, N. Carlin, I. Cauvin,
C. Clercq, A. Coppo, P. Cornier, C. Crotti, A. Derniaux, M. Dufour, S. Dugat, H. Dupont,
J. Durin, C. Dussud, L. Enrione, M. Felix-Faure, E. Fossier, Ph. Fourneret, A. François-Joubert,
B. Franck, J.F. Gaide, C. Gaillard, C. Garnier, F. Giraud, V. Indirli, B. Jammes, B. Lafond,
G. Laval, L. Lavigne, K. Liatard, J. Martin, S. Mayot, B. Morzol, L. Nicolas, F. Nougier,
J. Pachon, D. Paillet, F. Pailleux, J.M. Pellat, C. Peyrard, J. Provençal, J.P. Ramponneau,
C. Ravier, C. Rebischung, M.O. Rieussec, C. Righini, D. Roisin, R. Schaerer, S. Schmitt,
L. Stéfani, M.F. Vaillant, M.L. Villard.

Département De l’Isère
CHU de Grenoble
Pédiatrie Dr Corinne Armari-Alla,
Département de Chirurgie Digestive et de l’Urgence, Dr Catherine Arvieux,
Assistante sociale, Hospitalisation à Domicile (HAD), Eliane Bardonnenche,
Réanimation médicale, Dr Didier Barnoud,
Chirurgie urologique et de la transplantation rénale, Dr Bernard Boillot,
Cadre Infirmier, Equipe mobile de Soins Palliatifs, Noëlle Carlin,
Assistante sociale, Service de Gérontologie, Christine Crotti,
Psychologue, Unité de Concertation de cancérologie, Marion Dufour,
Diététicienne, Sophie Dugat,
Oncologie médicale, Hôpital de jour, IDE, Joëlle Durin,
IDE, Oncologie thoracique, Françoise Giraud,
Equipe mobile de Soins Palliatifs, Dr Guillemette Laval,
IDE, équipe mobile de Soins Palliatifs, Laurence Lavigne,
Réseau Palliavie et équipe mobile de soins palliatifs Karine Liatard,
Hospitalisation à Domicile, Dr Lydie Nicolas,
Cadre diététicienne, Service de Diététique, Denise Paillet,
Assistante sociale, équipe mobile de Soins Palliatifs, Florence Pailleux,
Oncologie médicale, Hôpital de jour, Dr Christine Rebischung,
Service de chirurgie ORL, Dr Christian Righini,
Psychologue, Unité de Concertation de cancérologie, Danielle Roisin,
Oncologie médicale, Dr Laetitia Stéfani,
Diététicienne, Comité de Liaison Alimentation et Nutrition (CLAN), Marie-France Vaillant,
Equipe mobile de Soins Palliatifs, Dr Marie-Laure Villard,
Autres établissements, réseau, clinique, centre médical Isère
Réseau Palliavie, Grenoble Dr Sylvie Batier,
Médecine Interne, Clinique Mutualiste, Grenoble Dr Caroline Belleville,
IDE, Centre Médical de Rocheplane Annick Coppo,
CHS de St Egrève Dr Pierre Cornier,
Oncologie, gastroentérologie et médecine polyvalente,
Centre Médical de Rocheplane Dr Marc Félix-Faure,
Equipe mobile de Soins Palliatifs, Clinique Mutualiste, Grenoble Dr Carol Dussud,
IDE, Oncologie et médecine polyvalente, Centre Médical de Rocheplane Laurence Enrione,
Oncologie Médicale, Clinique du Mail, Grenoble Dr Claire Garnier,
Assistante sociale, SCAPH 38, Grenoble Brigitte Jammes,
IDE, équipe mobile de Soins Palliatifs, Clinique Mutualiste, Grenoble Françoise Nougier,
Lits identifiés Soins palliatifs, Clinique des Cèdres, Grenoble Dr Bernard Morzol,
Centre de la douleur de l’adulte et de l’enfant, CH de Grenoble Dr Jean-Michel Pellat,
Equipe mobile Douleur et soins palliatifs, CH de Vienne Dr Colette Peyrard,
Réseau de Soins Palliatifs Palliavie Dr Jean-Pierre Ramponneau,
Oncologie et médecine polyvalente, Centre Médical de Rocheplane Dr Marie-Odile Rieussec,
Professeur honoraire, Oncologie médicale, Grenoble Pr René Schaerer,
Département de la Savoie (73) CH de Chambéry (73)
Unité de Soins Palliatifs et Equipe mobile Douleur et Soins Palliatifs, Dr Pierre Basset,
Radiothérapie Dr Emmanuel Berland, Dr Philippe Fourneret,
Médecine Nucléaire Dr Pierre-Yves Brard, Dr Anne François-Joubert,
Oncologie médicale Dr Isabelle Cauvin,
Equipe mobile Douleur et soins palliatifs, Dr Catherine Ravier,
Département de la Haute Savoie (74)
Unité de soins continus, Centre Médical MGEN de St Jean d’Aulps Dr Christophe Clercq,
Equipe mobile de Soins Palliatifs, CH d’Annemasse-Bonneville Dr Sylvie Bergé,
IDE, Unité de soins continus, Centre Médical MGEN de St Jean d’Aulps Nadia Beuriot,
Accueil Chirurgical, CH d’Annemasse-Bonneville Dr Marianne Besson,
Neurochirurgien, Clinique d’Argonay, Annecy
Dr Bruno Franck,
Réseau de Soins Palliatifs du Faucigny, Cluses (74)
Dr Jacques Martin,
IDE, Unité de soins continus,Centre Médical MGEN de St Jean d’Aulps Josette Pachon,
Oncologie Médicale, CH d’Annecy (74) Dr Jocelyne Provençal,
Equipe mobile de soins palliatifs, CH des pays de Morlaix (29) Dr Eric Fossier,
Département de la Drome (26) CH de Romans
IDE, Equipe mobile et unité de soins palliatifs,
Béatrice Lafond,
Equipe mobile et unité de soins palliatifs,
Dr Jean-François Gaide,
Département des Hautes Alpes (05) CH de Briançon
Psychologue, Equipe mobile de Soins Palliatifs, Solange Schmitt,
Equipe mobile de Soins Palliatifs, Dr Alain Derniaux,
Psychologue, équipe mobile de Soins Palliatifs, Héloïse Dupont,
Equipe mobile de Soins Palliatifs, Dr Corinne Gaillard,
Coordination : Dr Guillemette Laval, Dr Marie-Laure Villard, Equipe mobile de soins palliatifs, CHU de Grenoble

I
Introduction (G. Laval, A. Derniaux)
II
Asthénie (M. L. Villard, G. Laval)
III Douleur
................................
3.1
Démarche décisionnelle face à la douleur
3.2
Rotation des
3.3
PCA (analgésie autocontrôlée par le patient) et soins palliatifs
3.4
Prise en charge des douleurs neuropathiques
3.5
Prise en charge des douleurs par métastases osseuses
3.6
L’analgésie interventionnelle en soins palliatifs
3.7
Kétamine et douleurs rebelles
3.8
Soins douloureux en pratique palliative
3.9 MEOPA
et soins douloureux
IV
Symptômes neuropsychiques
4.1
Etat confusionnel
4.2 Dépression
4.3
Compression médullaire
4.4
Méningite carcinomateuse
4.5
Hypertension intracrânienne
V
Symptômes respiratoires
5.1 Dyspnée
................................
5.2
Encombrement et râles de l’agonie
5.3
Les soins de trachéotomie
VI
Troubles digestifs et nutrition
6.1
Bouche sèche, bouche douloureuse, bouche mycosique et ulcérée
6.2
Nausées et vomissements
6.3
Constipation
6.4
Occlusion intestinale maligne non résécable
6.5
Colostomie et iléostomie en soins palliatifs
6.6
Anorexie, nutrition
6.7
Les compléments nutritionnels
6.8
La nutrition entérale
6.9
La nutrition parentérale
VII Symptômes cutanéo
-
7.1 Escarres
................................
7.2
Ulcérations malignes
7.3
Mauvaises odeurs
VIII
Principaux symptômes urologiques
IX Anémie
................................
X
Traitements anticoagulants en soins palliatifs
XI
Place de la chimiothérapie en soins palliatifs
XII
Spécificité des soins palliatifs en pédiatrie
XIII La sédation
................................
XIV Interd
isciplinarité et transversalité
XV Accomp
agnement psychologique et deuil
XVI
Ethique et soins palliatifs
16.1 Les
annonces au cours de la maladie
16.2 Face à un
e demande d’euthanasie
16.3
Les refus de traitement et de soins
XVII Aspects sociaux
................................
XVII Soins palliatifs à domicile
18.1
Aspects pratiques pour u
18.2
Procédure d’admission en hospitalisation à domicile
18.3
Procédure de retour à domicile d’un patie
et hors réseau
18.4
Procédure de sortie à domicile d’un patient en soins palliatifs
avec l’aide d’un réseau de soins palliatifs
18.5
Difficultés de maintien à domicile d’un patie
Légende :
Retour Sommaire
Sommaire
Introduction (G. Laval, A. Derniaux)
................................
................................
Asthénie (M. L. Villard, G. Laval)
................................
................................
................................
................................
................................
Démarche décisionnelle face à la douleur
................................
Rotation des
opiacés ................................
................................
PCA (analgésie autocontrôlée par le patient) et soins palliatifs
Prise en charge des douleurs neuropathiques
................................
Prise en charge des douleurs par métastases osseuses
................................
L’analgésie interventionnelle en soins palliatifs
................................
Kétamine et douleurs rebelles
................................
................................
Soins douloureux en pratique palliative
................................
................................
et soins douloureux
................................
................................
Symptômes neuropsychiques
................................
................................
Etat confusionnel
................................................................
................................
................................................................
................................
Compression médullaire
................................
................................
Méningite carcinomateuse
................................
................................
Hypertension intracrânienne
................................
................................
Symptômes respiratoires
................................................................
................................
................................
................................
................................
Encombrement et râles de l’agonie
................................
................................
Les soins de trachéotomie
................................
................................
Troubles digestifs et nutrition
................................
................................
Bouche sèche, bouche douloureuse, bouche mycosique et ulcérée
Nausées et vomissements
................................
................................
Constipation
................................................................
................................
Occlusion intestinale maligne non résécable
................................
Colostomie et iléostomie en soins palliatifs
................................
Anorexie, nutrition
................................................................
................................
Les compléments nutritionnels
................................
................................
La nutrition entérale
................................................................
................................
La nutrition parentérale
................................
................................
-
muqueux ................................
................................
................................
................................
................................
Ulcérations malignes
................................
................................
Mauvaises odeurs
................................................................
................................
Principaux symptômes urologiques
................................
................................
................................
................................................................
................................
Traitements anticoagulants en soins palliatifs
................................
................................
Place de la chimiothérapie en soins palliatifs
................................
................................
Spécificité des soins palliatifs en pédiatrie
................................
................................
................................
................................
................................
isciplinarité et transversalité
................................
................................
agnement psychologique et deuil
................................
................................
Ethique et soins palliatifs
................................................................
................................
annonces au cours de la maladie
................................
................................
e demande d’euthanasie
................................
................................
Les refus de traitement et de soins
................................
................................
................................
................................
................................
XVII Soins palliatifs à domicile
................................................................
................................
Aspects pratiques pour u
ne continuité des prescriptions
................................
Procédure d’admission en hospitalisation à domicile
................................
Procédure de retour à domicile d’un patie
nt en soins palliatifs hors HAD
et hors réseau
................................................................
................................
Procédure de sortie à domicile d’un patient en soins palliatifs
avec l’aide d’un réseau de soins palliatifs
................................
Difficultés de maintien à domicile d’un patie
nt en soins palliatifs
................................
..................... 1
................................
.......................... 5
................................
...................................... 10
................................
..................................... 10
................................
..................................... 20
PCA (analgésie autocontrôlée par le patient) et soins palliatifs
................................... 27
................................
............................... 34
................................
.................. 40
................................
........................... 47
................................
....................... 53
................................
........ 57
................................
......................... 61
................................
.................................. 66
................................
.......... 66
................................
................... 71
................................
............................... 78
................................
............................ 82
................................
......................... 82
................................
.......... 83
................................
........................ 83
................................
............... 89
................................
............................. 92
................................
.................................. 97
Bouche sèche, bouche douloureuse, bouche mycosique et ulcérée
.............................. 97
................................
............................. 102
................................
.................. 107
................................
................................ 112
................................
.................................. 116
................................
........ 123
................................
...................... 127
................................
....... 133
................................
................................. 141
................................
................................... 145
................................
.......................... 145
................................
..................................... 150
................................
........... 152
................................
........................ 154
................................
....... 159
................................
....... 164
................................
......... 171
................................
.............. 174
................................
................................ 175
................................
........................ 176
................................
............... 181
................................
........ 187
................................
............ 189
................................
................. 194
................................
................ 199
................................
........................ 202
................................
......... 209
................................
.............. 209
................................
.................... 214
nt en soins palliatifs hors HAD
................................
................ 216
Procédure de sortie à domicile d’un patient en soins palliatifs
................................
.................................... 219
nt en soins palliatifs
............................... 224

Le présent recueil de pratique professionnelle de soins palliatifs a pour but d’aider les
oncologues, les spécialistes d'organes, les médecins généralistes ainsi que les professionnels de
santé engagés auprès des patients concernés par les soins palliatifs et d’une manière plus
générale par le soin de support.
Le comité Soins Palliatifs – Soins de Support (Réunions de Concertation Pluridisciplinaire)
constitué dans le cadre du Réseau de Cancérologie de l’Arc Alpin, contribue de la sorte aux soins
destinés au maintien de la qualité de vie des patients au cours de leur parcours thérapeutique ; il a
suscité ce travail collectif de professionnels de santé exerçant en équipe mobile de soins
palliatifs , en unité de soins palliatifs, en réseau de soins palliatifs, en services d’oncologie
médicale ou de spécialité à forte composante cancérologique.
De rédaction simple, enrichi de tableaux et d’arbres décisionnels, cet ouvrage propose des
conduites thérapeutiques sur la douleur et les symptômes qui hypothèquent le bien-être des
patients ; ces conduites sont élaborées à partir d’une expérience clinique qui repose sur des
recommandations nationales et internationales, en intégrant les aspects psychologiques, éthiques,
sociaux et organisationnels des soins palliatifs.
22 février 2006
Pr M. BOLLA Dr G. LAVAL Dr M.L. VILLARD

I. Introduction G. Laval, A. Derniaux
Ce recueil de pratiques professionnelles en soins palliatifs a pour but d'aider les oncologues, les médecins
hospitaliers, les médecins généralistes et tous les cliniciens engagés auprès de patients cancéreux en soins
palliatifs.
Il s'agit pour chaque patient, chaque situation clinique de considérer les questions posées par l'apparition
ou la persistance de symptômes gênants et de tout mettre en œuvre pour leur soulagement.
Une démarche évaluative et thérapeutique s'impose.
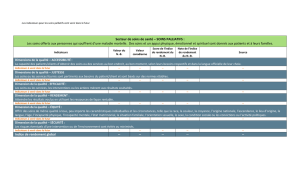
Les principes de traitement de la douleur et des autres symptômes sont résumés au tableau 1.
Il nous semble important de rappeler que les soins palliatifs sont le plus souvent destinés aux patients
atteints de cancer, mais non exclusivement (Sida, maladies neurodégénératives, insuffisance terminale des
grandes fonctions vitales…). Il s'agit de soins actifs mettant en œuvre tout ce qui peut soulager le malade, y
compris quand elles sont raisonnables les thérapeutiques étiologiques (chimiothérapie palliative,
radiothérapie, tumorectomie partielle…) utiles à restaurer ou à maintenir la qualité de vie du patient. Les
soins palliatifs offrent une prise en charge globale et pluridisciplinaire des besoins physiques,
psychologiques, sociaux et spirituels du malade ainsi qu'un soutien de ses proches avant et après le décès.
La définition des soins palliatifs proposée par la Société Française d'Accompagnement et de Soins Palliatifs
(SFAP – encadré 1) rappelle que leur définition est aussi d'ordre éthique "cherchant à éviter les
investigations et les traitements déraisonnables et se refusant à provoquer intentionnellement la mort".
Le champ d'application est représenté en cancérologie par les patients au stade évolutif ou terminal de leur
maladie. C'est l'apparition des premières métastases ou d'un diagnostic d'évolution locale, incurable qui
marque l'entrée d'un patient en Soins Palliatifs (schéma 1). Les soins palliatifs correspondent en partie aux
soins de support destinés au maintien de la qualité de vie des patients dès l'annonce du cancer jusqu'à leur
guérison ou leur décès.
Les aspects législatifs et organisationnels ont beaucoup évolué reconnaissant ainsi "le droit à toute
personne malade dont l'état le requiert d'accéder à des soins palliatifs et à un accompagnement" (encadré 3
– Loi du 9 juin 1999). Les équipes mobiles de soins palliatifs (EMSP), et les unités d'hospitalisation de
soins palliatifs (USP) sont créées pour permettre la prise en charge des cas les plus difficiles, former les
professionnels de santé et développer la recherche en soins palliatifs. Le tableau 2 présente les modalités
organisationnelles des soins palliatifs en France selon la circulaire 2002/98.
Dans tous les cas, il s'agira de suivre et d'accompagner le patient cancéreux tout au long de sa maladie dans
une démarche à visée curative lorsqu'elle est possible ou palliative lorsqu'il n'est plus raisonnable d'espérer
la guérison. Cette période de non guérison peut être longue de plusieurs mois, voire plusieurs années.
Comme le dit le Pr Schaerer, "quand on ne peut plus influencer le cours d'une maladie incurable, le malade
n'en continue pas moins à demeurer un être vivant qui présente des symptômes sources de souffrance. Le
traitement qui s'adresse à cette souffrance-là est dit palliatif. Il ne traite pas la maladie mais le malade ; il ne
prétend pas guérir mais soulager". Nous nous devons d'allier le savoir-faire et le savoir-être afin de
soulager, accompagner et soutenir les patients à travers l'épreuve de la maladie. Compétences, écoute,
disponibilité et travail dans l'interdisciplinarité reconnaissant chaque partenaire de soins dans son efficacité
et ses complémentarités sont seuls garants de la qualité des soins et de l'accompagnement du patient
cancéreux.
1
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
 70
70
 71
71
 72
72
 73
73
 74
74
 75
75
 76
76
 77
77
 78
78
 79
79
 80
80
 81
81
 82
82
 83
83
 84
84
 85
85
 86
86
 87
87
 88
88
 89
89
 90
90
 91
91
 92
92
 93
93
 94
94
 95
95
 96
96
 97
97
 98
98
 99
99
 100
100
 101
101
 102
102
 103
103
 104
104
 105
105
 106
106
 107
107
 108
108
 109
109
 110
110
 111
111
 112
112
 113
113
 114
114
 115
115
 116
116
 117
117
 118
118
 119
119
 120
120
 121
121
 122
122
 123
123
 124
124
 125
125
 126
126
 127
127
 128
128
 129
129
 130
130
 131
131
 132
132
 133
133
 134
134
 135
135
 136
136
 137
137
 138
138
 139
139
 140
140
 141
141
 142
142
 143
143
 144
144
 145
145
 146
146
 147
147
 148
148
 149
149
 150
150
 151
151
 152
152
 153
153
 154
154
 155
155
 156
156
 157
157
 158
158
 159
159
 160
160
 161
161
 162
162
 163
163
 164
164
 165
165
 166
166
 167
167
 168
168
 169
169
 170
170
 171
171
 172
172
 173
173
 174
174
 175
175
 176
176
 177
177
 178
178
 179
179
 180
180
 181
181
 182
182
 183
183
 184
184
 185
185
 186
186
 187
187
 188
188
 189
189
 190
190
 191
191
 192
192
 193
193
 194
194
 195
195
 196
196
 197
197
 198
198
 199
199
 200
200
 201
201
 202
202
 203
203
 204
204
 205
205
 206
206
 207
207
 208
208
 209
209
 210
210
 211
211
 212
212
 213
213
 214
214
 215
215
 216
216
 217
217
 218
218
 219
219
 220
220
 221
221
 222
222
 223
223
 224
224
 225
225
 226
226
 227
227
 228
228
 229
229
 230
230
1
/
230
100%