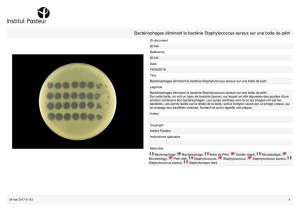
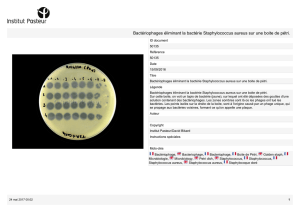
Résistance aux antiseptiques et aux désinfectants - chu

Résistance aux antiseptiques (et
désinfectants)
Dr Joseph HAJJAR
Consultant – Valence


RÉSISTANCE AUX
ANTISEPTIQUES
PRODUITS BIOCIDES
Pr. Jean-Yves Maillard
Cardiff School of Pharmacy and
Pharmaceutical Sciences
Cardiff University

Parmi une 50aine d’articles…
•Maillard JY. Antimicrobial biocides in the healthcare environment:
efficacy, usage, policies, and perceived problems. Therapeutics and
Clinical Risk Management 2005:1(4)307-320.
•Scientific Committee on Emerging and Newly Identified Health Risks
(SCENIHR). Assessment of the Antibiotic Resistance Effects of Biocides.
2009, 87 pages.
•Mounier M, et al. Les détergents et les désinfectants : les risques liés à
l’usage médical des biocides (2e partie). Antibiotiques 2009; 11:234-242.
•Harbarth S, et al. Is reduced susceptibility to disinfectants and antiseptics
a risk in healthcare settings? A point/counterpoint review. J Hosp Infect
2014;87:194-202.
•Rondeau C et al. Current molecular epidemiology of methicillin-resistant
Staphylococcus aureus in elderly French people: troublesome clones on
the horizon. Front Microbiol 2016 vol 7 art 31.

Préambule
•Structure bactérienne
–Modes d’action des antiseptiques
–Mécanismes de résistance
Diapositives empruntées au Dr Olivier Castel, CHU de Poitiers
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
1
/
33
100%