Lire l'article complet

14 | La Lettre du Cardiologue • N° 502-503 - février-mars 2017
MISE AU POINT
Diamètre (µm)
100
50
0200 400 Longueur (µm)
Diamètre extérieur
Diamètre intérieur
Épaisseur pariétale
A
B
C
Reflet axial
Mur
SegmentationImage moyennée
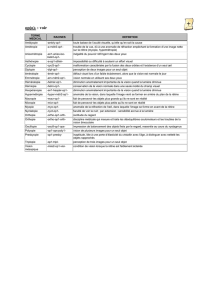
Figure 1. Images et segmentation d’une artériole rétinienne en optique adaptative.
A. Image obtenue (à droite : grossissement). On voit les structures pariétales entre les
flèches (A : artériole, V : veinule ; échelle = 250 µm). B. Image finale et sa segmentation.
C. Morphogramme du vaisseau (d’après [5]).
Explorations des artères
de la rétine dans les maladies
cardiovasculaires
Retinal arteries imaging in cardiovascular disease
D. Rosenbaum*, A. Gallo*, A. Mattina*, X. Girerd*
* Unité de prévention des maladies
cardiovasculaires, hôpital univer-
sitaire de la Pitié-Salpêtrière, Paris.
L
a microcirculation, c’est-à-dire les artères de
moins de 300 µm de diamètre, représente la
plus grande partie du système circulatoire,
et pourtant, son rôle dans les maladies cardio-
vasculaires est moins bien connu que celui des
grosses artères. Cela est en partie dû au fait que les
méthodes auxquelles on a recours pour l’explorer
sont complexes, invasives et hautement spécialisées,
ce qui limite grandement leur utilisation. En effet, la
méthode de référence est la biopsie de tissu sous-cu-
tané glutéal où sont disséquées des artérioles qui
sont ensuite montées sur un myographe.
La rétine est un territoire unique où la microvascula-
risation peut être visualisée directement. Des avan-
cées récentes dans l’imagerie optique ont permis le
développement de techniques semi-automatiques
permettant de mesurer et de quantifier des varia-
tions subtiles des petits vaisseaux de la rétine.
Appliquées à de larges populations ou à des profils
de patients particuliers, elles ont pu montrer des
liens entre la rétine et les pathologies cardio-
métaboliques.
L’imagerie vasculaire rétinienne est, pour l’instant,
utilisée dans 2 grands domaines de recherche :
l’exploration de la physiologie et de la physio-
pathologie des petites artères dans le dévelop-
pement des maladies cardiovasculaires et le rôle
de la microcirculation comme marqueur de risque
cardiovasculaire (1).
Techniques d’exploration
de la vascularisation rétinienne
Le classique fond d’œil manque de précision et, en
dehors des stades de rétinopathie hypertensive, il ne
permet pas d’analyser précisément le remodelage
artériolaire. La technique la plus utilisée et validée
est celle qui permet de mesurer un ratio artério-
veineux. Celui-ci est obtenu en utilisant une caméra
de fond d’œil de haute résolution couplée à un logiciel
dédié (le Retinal Vessel Analyzer [RVA]) [2]. Un logiciel
semi-automatique identifie les artères et les veines
de la rétine et calcule un ratio en additionnant tous
les diamètres des artères et des veines visualisées. On
obtient ainsi un ratio reflétant le rétrécissement relatif
des artères par rapport aux veines. Cette technique,
relativement facile et peu coûteuse, a été utilisée
dans de très larges cohortes multicentriques, mais
n’a pas pu montrer de lien avec d’autres atteintes
d’organes cibles dans l’hyper tension artérielle (HTA).

La Lettre du Cardiologue • N° 502-503 - février-mars 2017 | 15
Points forts
»
Les progrès très récents réalisés en imagerie permettent désormais de mesurer in vivo de façon non
invasive, fiable, répétée et reproductible d’infimes variations et anomalies dans un territoire auparavant
totalement non exploré : les artèresde moins de100 µm.
»
Ces appareils de très haute résolution fournissent des images qui valident ou invalident les théories
sur la microcirculation.
»L’atteinte des artérioles rétiniennes est reliée au risque cardiovasculaire et cérébrovasculaire.
»La rétine est une fenêtre ouverte sur la microcirculation corporelle.
Mots-clés
Microcirculation
Remodelage
Imagerie de haute
résolution
Risque
cardiovasculaire
Résistances
périphériques
Highlights
»
Recent technical progress
have enabled reliable, non
invasive, in vivo and repro-
ducible imaging of very refined
abnormalities and variations in
arteries below 100µm of diam-
eter. This territory has never
been explored before
»
Those high resolution camera
produce images and data that
validate or invalidate previous
theories on microcirculation
»
Retinal small arteries abnor-
malities reflect cardiovascular
and cerebrovascular risk
»
The retina is an open window
into the global microcirculation
network.
Keywords
Microcirculation
Remodeling
High-resolution imaging
Cardiovascular risk
Peripheral resistances
La technique pionnière d’imagerie des artérioles
rétiniennes de précision a été développée, il y a
une quinzaine d’années, par une équipe allemande
(Heidelberg Retinal Flowmeter, Heidelberg Enginee-
ring). Il s’agit du Scanning Laser Doppler Flowmetry
(SLDF) [3]. Cette technique est la combinaison d’une
image optique de précision, qui permet d’obtenir le
diamètre total du vaisseau, et d’une image doppler,
qui permet de connaître le diamètre de la lumière
circulante. L’addition ou la soustraction des 2 images
permet d’obtenir le diamètre de la lumière et de la
paroi artériolaires. Sa résolution est d’environ 15 µm.
Cette technique a été validée contre le gold standard
mais, étant donné la disponibilité limitée de l’appa-
reil et sa non-commercialisation, les recherches qui
l’ont utilisée ont porté sur de plus petites cohortes
de patients ou sur des phénotypes particuliers
comme les patients atteints d’une HTA secondaire
ou ayant des antécédents cérébrovasculaires (4).
La caméra d’optique adaptative (OA) est une troi-
sième technique qui vient, quant à elle, de l’imagerie
spatiale. Elle est actuellement utilisée dans tous
les nouveaux téléscopes, mais son application à la
médecine est récente. Il s’agit d’une caméra de fond
d’œil couplée à un système d’analyse combinant
des miroirs déformables et un algorithme de cor-
rection, qui va permettre de corriger les aberrations
de l’image pour en orienter a résolution. Ainsi, l’op-
tique adaptative permet d’obtenir des images de
1,4 µm de résolution (5). Cela permet la visualisa-
tion directe de toutes les structures vasculaires de
la rétine. Les mesures sont ensuite effectuées par
l’intermédiaire d’un logiciel semi-automatique qui
assure la reproductibilité des mesures (figure 1) [5].
Cet appareil français prometteur est validé CE et
commercialisé, mais son coût important en limite
la disponibilité à quelques centres en Europe.
Ni le SLDF ni l’OA ne demandent une dilatation par
des collyres, mais la contrepartie est que le champ
d’exploration est réduit à une petite portion de la
rétine. Les autres limites de ces techniques sont la
cataracte et la coopération du patient.
Par ailleurs, aucune des techniques précédentes ne
permet, à l’heure actuelle, d’étudier de façon validée
les capillaires, soit à cause d’une résolution insuffi-
sante (pour le SLDF), soit en raison de leur structure
tortueuse difficile à analyser.
L’angiographie-OCT (Optical Coherence Tomo-
graphy) au contraire est en plein développement.
L’OCT est une technique comparable à l’échographie
sauf qu’elle utilise des ondes laser au lieu des ondes
ultrasonores. L’angiographie-OCT, elle, analyse les
interférences et le bruit générés par les mouvements
des hématies pour reconstituer tout le réseau vas-
culaire, capillaires compris. Les images sont remar-
quables et comparables à celles de l’angiographie à
la fluorescéine, mais l’utilisation de cet appareil est
pour l’instant limitée au domaine ophtalmologique.
Enfin, en ce qui concerne l’étude de la motricité
artério laire rétinienne, en dehors de l’injection de
vasodilatateurs, la méthode la plus courante est celle
du stroboscope (flicker light). Elle est cependant peu
utilisée car non formellement validée, non standardisée
et pas forcément bien tolérée. De plus, comme le stro-
boscope augmente l’activité des photorécepteurs, il
n’est pas possible de faire la différence entre une vasodi-
latation métabolique ou endothélium-dépendante.
Apports des explorations
rétiniennes dans la physiologie
des maladies cardiovasculaires
Dans l’hypertension artérielle
La première étape pour les différents “imageurs
cardiovasculaires” de la rétine a été de reproduire
les résultats initiaux obtenus sur les artérioles glu-
téales sous-cutanées.
Pour de multiples raisons, notamment historiques,
c’est dans le domaine de l’HTA que les travaux de
physiologie ont été le plus importants.
La majeure partie des modifications structurelles
observées chez les patients hypertendus consiste
en un remodelage eutrophique centripète, c’est-
à-dire un épaississement pariétal, une réduction
de la lumière et du diamètre extérieur du vaisseau
sans modification de la quantité totale de tissu de la
paroi. Il s’ensuit donc une augmentation du rapport
mur/lumière (WLR) et l’impression d’un remode-
lage “vers l’intérieur”, d’où son nom de remode-
lage eutrophique centripète. Il est dit spécifique de
l’hypertension essentielle parce que les artères de

16 | La Lettre du Cardiologue • N° 502-503 - février-mars 2017
MISE AU POINT Explorations des artères delarétine dans les maladies cardiovasculaires
résistance chez les patients souffrant d’hypertension
secondaire sont caractérisées par un remodelage
hypertrophique avec épaississement de la média,
diminution de la lumière et surtout augmentation
de la quantité totale de tissu de la paroi médiée par
une hypertrophie des cellules musculaires lisses.
Ces résultats ont été retrouvés sur les artérioles réti-
niennes soit grâce à l’optique adaptative dans de larges
populations de patients hypertendus ou présentant
des facteurs en risque, soit grâce au SLDF chez des
patients ayant des antécédents cérébro vasculaires
ou une HTA secondaire à un phéochromocytome ou
à un hyperaldostéronisme.
Concernant les corrélations entre les anomalies de diffé-
rents territoires microvasculaires, il est à rappeler que les
artérioles rétiniennes et cérébrales ont la même origine
embryologique et la même structure. Par ailleurs, des
relations ont pu être démontrées avec la microcircu-
lation rénale ou coronaire, témoignant du fait que la
rétine pourrait aussi être une fenêtre sur le corps entier.
Nous avons également pu retrouver la relation entre
le remodelage rétinien et les résistances périphériques
dans une population de patients hypertendus (6).
Enfin, la reproductibilité de ces techniques non inva-
sives permet d’étudier l’effet de thérapeutiques sur le
même segment de la même artère à différents temps,
ce qui était impossible auparavant. Ainsi, des études
d’intervention sur la pression artérielle ont permis de
montrer avec le SLDF et l’OA un remodelage inverse
après diminution du niveau de pression artérielle. Les
données concernant l’efficacité supérieure de telle ou
telle classe d’antihypertenseurs sont contradictoires,
mais les inhibiteurs du système rénine-angiotensine
réunissent le plus de preuves au contraire des diuré-
tiques et des bêtabloquants, peut-être en raison de
leurs propriétés antiprolifératives et antioxydantes.
Dans le vieillissement vasculaire
L’étude de grandes populations en prévention pri-
maire avec l’OA a aussi permis la validation in vivo
de phénomènes observés en histologie. En particulier
celui du vieillissement microvasculaire, pour lequel
nous avons pu démontrer qu’il provoquait un épais-
sissement pariétal structurel indépendant du remo-
delage causé par les autres facteurs de risque (7).
Dans les maladies métaboliques
Chez les diabétiques, l’OA et le SLDF ont permis
de visualiser, au niveau de la rétine, comme en
sous-glutéal, un remodelage artériolaire hyper-
trophique. Celui-ci consiste aussi en une élévation du
rapport WLR (Wall-to-Lumen-Ratio) due à un épais-
sissement pariétal qui résulte d’une prolifération
et d’une hypertrophie des cellules et de la matrice
extracellulaire, menant à une augmentation de la
masse du vaisseau (contrairement à l’hypertension
où la masse du vaisseau est inchangée, l’épaissis-
sement étant dû à un réarrangement des cellules).
L’étude de la vasoréactivité artériolaire, quant à elle,
a fait l’objet de quelques études qui ont pu revalider
sa diminution dans l’HTA ou son amélioration chez
des diabétiques traités par saxagliptine (8).
En ce qui concerne les autres facteurs de risque
métabolique, l’étude de larges populations en OA
a pu montrer des relations entre indice de masse
corporelle (IMC) et remodelage. Les relations avec
les paramètres lipidiques sont encore à l’étude.
Dans la connaissance de la physiologie
de la microcirculation
Au-delà de la validation in vivo, l’exploration de
la rétine a apporté de nouvelles données sur la
physiologie de la microcirculation.
Tout d’abord, la haute résolution de ces nouvelles
technologies a ouvert de nouveaux champs d’ex-
ploration portant sur des territoires vasculaires
jamais visualisés auparavant in vivo. En effet, les
artérioles étudiées en sous-cutané sont de l’ordre
de 200 à 300 µm alors que celles visualisées dans
la rétine sont entre 20 et 100 µm ! À ce niveau, les
équations théoriques prédisent qu’il n’y a plus de
pulsatilité, mais cela n’a jamais été corroboré par
des observations in vivo. La résolution temporelle
de l’OA nous permet de l’évaluer, et la pulsatilité
des artérioles est actuellement à l’étude. La très
haute résolution de l’OA nous a aussi permis de
constater que, au fur et à mesure que le calibre de
l’artère se rétrécit, l’épaisseur diminue de façon non
proportionnelle, c’est-à-dire que la WLR augmente
de façon physiologique à mesure qu’on avance dans
l’arbre artériel de l’aorte jusqu’au capillaire.
Deuxièmement, la reproductibilité des techniques a
aussi permis de voir que la correction du remodelage
en cas de diminution de pression est à la fois rapide
(< 6 semaines), probablement en raison d’une simple
vasodilatation (9), et prolongée, laissant penser qu’il
s’agit aussi d’un remodelage inverse structurel (10).
Enfin, l’OA nous a permis de repenser complète-
ment la physiopathologie classique des croisements
artérioveineux. Nous avons pu constater des stric-

La Lettre du Cardiologue • N° 502-503 - février-mars 2017 | 17
MISE AU POINT
Figure 2. Image de striction veineuse (*) à distance de l’artère (A : artériole, V : veine),
entre les flèches blanches, on voit la paroi de l’artère dont le calibre est régulier (échelle
[barre blanche] = 125 µm) [d’après (5)].
tions veineuses en dehors de tout contact avec
l’artère (figure 2) [5]. Ce n’est donc pas l’artère
qui comprime la veine, mais peut-être une gangue
de matrice extracellulaire ou une striction due à
une sécrétion artérielle paracrine. De même, il a
été possible d’observer finement les “rétrécisse-
ments” artériels qui sont décrits comme les signes
précoces et pathognomoniques de la rétinopathie
hyper tensive. Nous avons pu, d’une part, montrer
qu’à leur niveau il existe un rétrécissement de la
lumière sans épaississement pariétal et, d’autre part,
que ce sont des phénomènes dynamiques qui évo-
luent au cours du temps ! Tout cela laisse à penser
que ce sont des phénomènes vasomoteurs et non
structurels. On voit bien là comment la visualisation
de nouveaux phénomènes permet de générer de
nouvelles hypothèses.
La rétine comme marqueur
de risque (11)
Une question clé en physiologie cardiovasculaire
est de savoir si les changements détectés dans la
microvascularisation précèdent ou accompagnent la
maladie. Par exemple, une caractéristique de l’HTA
est l’augmentation des résistances périphériques
déterminée en grande partie par le diamètre des
artérioles. Quelques études ont notamment
démontré que le rétrécissement artériolaire réti-
nien précédait de plusieurs années le dévelop-
pement de l’HTA chez des individus initialement
normotendus (12).
Une autre question clé est de pouvoir améliorer
simplement la prédiction des maladies cardio-
vasculaires. De la simple relation entre les ano-
malies du fond d’œil et le risque cérébrovasculaire
dans une immense cohorte d’hypertendus japo-
nais (13) au lien démontré dans des études pros-
Tableau. Comparaison entre les différentes techniques d’imagerie rétinienne.
Nom Technique Paramètre mesuré Validation contre
gold standard
histologique
Résultats Avantages Points négatifs
Fond d’œil Imagerie optique Critères cliniques Non Relation entre
signes de
rétinopathie et risque
cardiovasculaire
Disponible Manque de précision
Retinal Vessel
Analyzer
Imagerie optique
+ logiciel
Ratio artérioveineux Non Relation avec le
risque d’hypertension
Étude de l’anatomie
du réseau
Disponible
Moyennement
onéreux
Facile
Indice composite
Manque de précision
Scanning Laser
Doppler Flowmetry
Imagerie optique
+imagerie doppler
+ logiciel dédié
Lumière
Épaisseur
du vaisseau
Surface sectionnelle
Rapport mur/lumière :
WLR
Oui Validation des études
in vitro
Lien avec le risque
cardiovasculaire
Données
fonctionnelles
Large littérature
Pas de dilatation
nécessaire
Non commercialisé
Résolution “faible”
Mesures indirectes
Petit champ étudié
Optique adaptative Imagerie optique
+logiciel dédié
Lumière
Épaisseur
du vaisseau
Surface sectionnelle
Rapport mur/lumière :
WLR
Non, en cours Vieillissement
microvasculaire
Lien avec les
résistances
périphériques
Nouvelles hypothèses
physiologiques
Larges cohortes
Ultrahaute précision
Disponible,
marquéCE
Mesures directes
Pas de dilatation
nécessaire
Prix
Petit champ étudié

18 | La Lettre du Cardiologue • N° 502-503 - février-mars 2017
MISE AU POINT Explorations des artères delarétine dans les maladies cardiovasculaires
pectives américaines (14), il existe plusieurs preuves
montrant une relation entre microcirculation réti-
nienne et risque cardiovasculaire. Tout d’abord, il
semble établi que la diminution du rapport artério-
veineux déterminée par le RVA prédit l’incidence
d’HTA. Ensuite, un lien entre risque cardiovasculaire
et diminution du RVA a été démontré chez les
femmes dans de larges cohortes. En revanche, le
rétrécissement artériolaire, quant à lui, n’était pas
corrélé aux accidents vasculaires cérébraux. Enfin,
la nouveauté et la faible disponibilité des nouvelles
techniques d’imagerie rétinienne de haute précision
font malheureusement qu’il n’existe pas encore,
à l’heure actuelle, d’études prospectives stricte-
ment “rétiniennes” permettant de valider l’OA ou
le SLDF comme des outils de prédiction du risque
cardiovasculaire (tableau, p. 17).
En revanche, la possibilité de visualiser un remodelage
artériolaire rétinien peut aussi permettre de détecter
une HTA. Chez 1 500 patients, un WLR des artérioles
rétiniennes supérieur à 0,31 est en faveur d’une HTA
de consultation, et un diamètre inférieur à 78 μm fait
évoquer une HTA masquée. L’évaluation des artérioles
de la rétine avec la caméra d’optique adaptative peut
apporter une aide au diagnostic de l’HTA, en particu-
lier dans sa forme masquée (15).
Enfin, une autre approche de recherche a été d’étu-
dier, avec le RVA cette fois, la structure du réseau
artériolaire rétinien, sa longueur, l’angle de ses bifur-
cations, sa tortuosité, le nombre des ramifications,
etc., afin de déterminer un schéma spécifique qui
pourrait témoigner d’une maladie génétique du col-
lagène ou d’un risque cardiovasculaire particulier.
Les résultats de cette approche particulièrement
innovante sont encore faibles.
Conclusion : le renouveau
du fond d’œil en hypertension ?
Les progrès de l’imagerie ces 20 dernières années
ont permis aux cliniciens et aux chercheurs de
mesurer d’infimes variations de façon non inva-
sive dans un territoire jusqu’à présent inexploré.
Ces techniques nous ont permis d’en apprendre
davantage sur la physiologie microvasculaire et
le risque cardiovasculaire, notamment dans le
domaine de l’HTA. La facilité et la reproductibilité
de l’OA ouvrent un champ d’exploration immense :
effet des médicaments antihypertenseurs dans une
étude prospective, recherche d’un marqueur ayant
un rôle pronostique du risque cérébrovasculaire ou
de démence, aide au diagnostic et au suivi des HTA
masquées, prédiction d’une future HTA chez les
patients à risque, etc.
Pendant longtemps, l’examen ophtalmologique a
fait partie du bilan cardiovasculaire des patients
hypertendus. Les progrès technologiques récents
sont en train de lui redonner ses lettres de
noblesse. ■
1. Liew G, Wang JJ, Mitchell P, Wong TY. Retinal vascular
imaging: a new tool in microvascular disease research. Circ
Cardiovasc Imaging 2008;1(2):156-61.
2. Neubauer AS, Lüdtke M, Haritoglou C, Priglinger S,
Kampik A. Retinal vessel analysis reproducibility in assessing
cardiovascular disease. Optom Vis Sci 2008;85(4):247-54.
3. Michelson G, Schmauss B, Langhans MJ, Harazny J, Groh
MJ. Principle, validity, and reliability of scanning laser
Doppler flowmetry. J Glaucoma 1996;5(2):99-105.
4. Harazny JM, Ritt M, Baleanu D et al. Increased wall: lumen
ratio of retinal arterioles in male patients with a history of a
cerebrovascular event. Hypertension 2007;50(4):623-9.
5. Koch E, Rosenbaum D, Brolly A et al. Morphometric ana-
lysis of small arteries in the human retina using adaptive
optics imaging: relationship with blood pressure and focal
vascular changes. J Hypertens 2014;32(4):890-8.
6. Rosenbaum D, Kachenoura N, Koch E et al. Relationships
between retinal arteriole anatomy and aortic geometry
and function and peripheral resistance in hypertensives.
Hypertens Res 2016;39(7):536-42.
7. Rosenbaum D, Mattina A, Koch E et al. Effects of age, blood
pressure and antihypertensive treatments on retinal arte-
rioles remodeling assessed by adaptive optics. J Hypertens
2016;34(6):1115-22.
8. Ott C, Raff U, Schmidt S et al. Effects of saxagliptin on
early microvascular changes in patients with type 2 diabetes.
Cardiovasc Diabetol 2014;13:19.
9. Mattina A, Rosenbaum D, Kanagasabapathy C, Koch E,
Paques M, Girerd X. 7D.02: effect of a short-term antihy-
pertensive treatment on retinal arterioles evaluated with
adaptive optics retinal camera J Hypertens 2015;33 Suppl
1:e100.
10. De Ciuceis C, Savoia C, Arrabito E et al. Effects of a long-
term treatment with aliskiren or ramipril on structural alte-
rations of subcutaneous small-resistance arteries of diabetic
hypertensive patients. Hypertension 2014;64(4):717-24.
11. Agabiti Rosei E, Rizzoni D. Microvascular structure as a
prognostically relevant endpoint. J Hypertens 2017; January
11, doi: 10.1097/HJH.0000000000001259.
12. Wang JJ, Rochtchina E, Liew G et al. The long-term relation
among retinal arteriolar narrowing, blood pressure, and inci-
dent severe hypertension. Am J Epidemiol 2008;168(1):80-8.
13. Sairenchi T, Iso H, Yamagishi K et al. Mild retinopathy is
a risk factor for cardiovascular mortality in Japanese with
and without hypertension: the Ibaraki Prefectural Health
Study. Circulation 2011;124(23):2502-11.
14. Wong TY, Klein R, Sharrett AR et al.Retinal arteriolar
narrowing and risk of coronary heart disease in men and
women. The Atherosclerosis Risk in Communities Study.
JAMA 2002;287(9):1153-9.
15. Gallo A, Mattina A, Rosenbaum D, Koch E, Paques M,
Girerd X. Retinal arteriolar remodeling evaluated with adap-
tive optics camera: relationship with blood pressure levels.
Ann Cardiol Angeiol (Paris) 2016;65(3):203-7.
Références bibliographiques
D. Rosenbaum déclare ne pas
avoir de liens d’intérêts.
Les autres auteurs n’ont pas
précisé leurs éventuels liens
d’intérêts.
1
/
5
100%