Caryologie et évolution chromosomique de certains petits

1 Introduction
L’information génétique dont les organismes
vivants héritent de leurs progéniteurs est encodée
dans les séquences moléculaires de l’ADN. L’ADN
des animaux et des autres eucaryotes est associé à
des protéines et organisé en chromosomes. Les chro-
mosomes sont essentiels à la division cellulaire, qui
a lieu au cours de la mitose et de la méiose, deux
processus de distribution de l’information génétique
aux cellules filles. Le processus d’évolution produit
souvent des modifications de la forme, du nombre
ou de la taille des chromosomes. Le caryotype d’un
individu est constitué du complément chromo-
somique de ses cellules. Le caryotype est souvent
uniforme à l’intérieur d’une espèce. Dans de nom-
breux cas toutefois, on observe d’importantes varia-
tions caryotypiques parmi les populations ou les
individus d’une même espèce. La comparaison des
caryotypes peut fournir de précieux renseignements
sur les mécanismes de l’évolution et les liens de par-
enté entre les espèces.
De nombreux documents scientifiques ont été
publiés sur les caryotypes de petits mammifères
d’Afrique (p. ex. Robbins et Baker 1978, Haiduk et
al. 1980, 1981, Viegas-Péquignot et al. 1983,
Reumer et Meylan 1986, Zima et al. 1998, Schlitter
et al. 1999, Biltueva et al. 2001). Cependant, la
région présente une importante diversité biologique,
et il existe de nombreuses espèces chez lesquelles le
caryotype n’a pas encore été étudié. Par exemple, le
genre de musaraigne Crocidura compte plus de 150
espèces, parmi lesquelles une centaine se trouvent en
Afrique. Seule la moitié environ des espèces
africaines ont été caryotypées, et l’on signale beau-
coup de variations caryotypiques dans le nombre
chromosomique chez des espèces africaines de
Crocidura, avec des nombres diploïdes variant de 36
à 68 (Zima et al. 1998, Schlitter et al. 1999). Malgré
le peu de données chromosomiques dont on dispose
pour de nombreuses espèces de Crocidura, les don-
nées caryotypiques ont été utilisées dans bon nombre
d’analyses sur l’évolution et la systématique de ce
genre, qui présente une grande diversité sur les plans
taxinomique et caryotypique (Maddalena et Ruedi
1994, Zima et al. 1998, Biltueva et al. 2001). Bien
que certains rongeurs et chauves-souris d’Afrique
aient été abondamment étudiés, il existe de nom-
breuses espèces pour lesquelles on ne dispose d’au-
cune donnée caryotypique.
Puisque l’on sait que chez certaines espèces, les cary-
otypes varient entre les populations et entre les indi-
vidus, il est important d’examiner les caryotypes de
nombreux individus de différentes localités. Une grande
partie des études de caryotypes faites sur les petits mam-
mifères d’Afrique tropicale a porté sur ceux de la Côte
d’Ivoire, du Cameroun et de la République cen-
trafricaine. Certaines des plus vastes étendues de forêt
tropicale humide se trouvent au Gabon, et la région
présente une grande biodiversité. Cependant, malgré
cette diversité, relativement peu d’études ont porté sur la
caryologie des petits mammifères du Gabon.
Récemment, nous avons participé à un recensement
de la biodiversité mammalienne du Complexe d’Aires
Protégées de Gamba, sous les auspices de l’Institution
Smithsonian et avec l’appui de la Fondation Shell et
Shell Gabon. Nous avons prélevé des petits mammifères
Bulletin of the Biological Society of Washington, No. 12 155
Caryologie et évolution chromosomique de
certains petits mammifères de la forêt tropicale
humide du champ pétrolifère de Rabi, Gabon
Ashley PRIMUS1, Jessica HARVEY1, Sylvain GUIMONDOU2, Serge MBOUMBA3,
Raphaël NGANGUI4, Federico HOFFMANN5, 6, Robert BAKER5et Calvin PORTER5, 1
1Department of Biology, Xavier University of Louisiana, 1
Drexel Drive, New Orleans, LA 70125, USA. Auteur pour la
correspondance Email: cpor[email protected]
2Direction de la Faune et de la Chasse, BP 159, Tchibanga,
Gabon. Email: guimondou@yahoo.fr
3Gabon Biodiversity Program, Smithsonian Institution,
S/C Shell Gabon, BP 48, Gamba, Gabon.
Email: mboumbamoussoundaditona@yahoo.fr
4IRAF - CENAREST, BP 2246, Libreville, Gabon. Email:
nganguiraphael@yahoo.com
5Department of Biological Sciences, Texas Tech University,
Lubbock, TX 79409, USA. Email: rjbaker@TTU.EDU
6Adresse actuelle: School of Biological Sciences, University
of Nebraska, Lincoln, NE 68588. USA. Email:

du champ pétrolifère de Rabi, au Gabon, dans la forêt
tropicale humide, juste au sud de l’équateur. À Rabi, les
zones dans lesquelles se déroulent des activités
humaines se limitent à de petites clairières isolées de la
forêt tropicale. Dans le cadre de ce recensement, nous
avons préparé les caryotypes d’un certain nombre d’e-
spèces de petits mammifères, dont des musaraignes, des
rongeurs et des chauves-souris. Nous présentons ici les
données chromosomiques concernant les musaraignes,
les rongeurs et les chauves-souris du sous-ordre des
Mégachiroptères. Les caryotypes standard des chauves-
souris du sous-ordre des Microchiroptères seront
présentés dans un autre article. Nous comparons nos
résultats aux données publiées et discutons des con-
séquences de la variabilité chromosomique des taxons
étudiés sur les plans de la systématique et de l’évolution.
2 Matériel et méthodes
Nous avons prélevé des petits mammifères dans le
champ pétrolifère de Rabi, du Complexe de Gamba,
province de l’Ogooué-Maritime, au Gabon (Lee et
al. ce volume; voir carte page xxxii). Les animaux
ont été prélevés au cours des mois de février et mars
2002 selon la technique décrite par Rodriguez et al.
(ce volume) et O’Brien et al. (ce volume).
Les préparations de chromosomes mitotiques ont
été effectuées au laboratoire de Rabi, à partir de
moelle osseuse, au moyen des méthodes de Baker et
al. (2003), sauf que l’éthanol a été utilisé pour la fix-
ation, en raison d’un manque de méthanol. Les pré-
parations méiotiques proviennent de tissus testicu-
laires de mâles sélectionnés et ont été faites à l’aide
des mêmes méthodes. Les chromosomes ont été col-
orés au Giemsa. Le Gouvernement du Gabon a
autorisé la recherche et nous a permis d’utiliser cer-
tains spécimens comme échantillons de référence.
Nous avons préparé des spécimens standard mon-
tés et d’autres conservés dans l’alcool, que nous
avons déposés comme spécimens de référence dans
les collections de mammifères du programme de
biodiversité du Gabon, à Gamba, de l’Institution
Smithsonian à Washington ou du Natural Science
Research Laboratory de la Texas Tech University.
Des préparations de chromosomes sur lames et des
suspensions cellulaires sont conservées avec les
échantillons de tissus à la Texas Tech University, et
chacune porte un numéro de référence unique (TK)
renvoyant au spécimen dont elle provient. Les spéci-
mens examinés sont indiqués au tableau 1.
156 Gamba, Gabon: Biodiversité d'une forêt équatoriale africaine
Tableau 1. Spécimens examinés et nombres diploïdes observés (2n). TK numéro de référence unique renvoyant au
spécimen témoin dont provient la préparation.
TK Espèces sexe 2n TK Espèces sexe 2n
110269
Crocidura crenata
M 48? 110258
Hypsignathus monstrosus
F36
110322
Crocidura goliath
M 50 110263
Megaloglossus woermanni
F34
110417
Crocidura goliath
M 50 110267
Megaloglossus woermanni
M34
110400
Crocidura grassei
M 40 110287
Megaloglossus woermanni
M34
110262
Sylvisorex ollula
M 38 110290
Megaloglossus woermanni
F34
110327
Sylvisorex ollula
M 38 110338
Megaloglossus woermanni
M34
110285
Heimyscus fumosus
M 40 110264
Myonycteris torquata
F36
110328
Hylomyscus parvus
F 46 110265
Myonycteris torquata
F36
110368
Hylomyscus stella
M 46 110266
Myonycteris torquata
F36
110389
Hylomyscus stella
M 46 110291
Myonycteris torquata
F36
110415
Lophuromys nudicaudus
F 56 110292
Myonycteris torquata
F36
110367
Malacomys longipes
M 48 110293
Myonycteris torquata
F36
110397
Mus musculoides
F 34 110295
Myonycteris torquata
F36
110398
Mus musculoides
M 34 110299
Myonycteris torquata
F36
110302
Praomys tullbergi
F 34 110300
Myonycteris torquata
F36
110251
Epomops franqueti
F 36 110339
Myonycteris torquata
F36
110253
Epomops franqueti
F 36 110390
Myonycteris torquata
F36
110254
Epomops franqueti
F 36 110392
Myonycteris torquata
M36
110463
Epomops franqueti
F 36 110481
Myonycteris torquata
F36
110475
Epomops franqueti
M 35 110465
Scotonycteris zenkeri
M32

3 Résultats et discussion
Nous avons étudié les caryotypes de 17 espèces
de petits mammifères du Complexe de Gamba (qua-
tre espèces d’insectivores, sept espèces de rongeurs
et six espèces de chauves-souris) dont cinq espèces
dont le caryotype n’avait jamais été documenté:
Crocidura crenata, C.goliath,C.grassei,
Heimyscus fumosus et Scotonycteris zenkeri. Pour
certaines autres espèces, nous décrivons des cary-
otypes qui diffèrent à certains égards de ceux déjà
présentés dans la littérature. Nos résultats confir-
ment que la biodiversité de Rabi comprend des
aspects chromosomiques aussi bien que taxi-
nomiques. Comme notre laboratoire de terrain n’é-
tait pas équipé pour l’étude des bandes chromo-
somiques, nous n’avons pas encore examiné les pro-
fils des bandes chromosomiques des spécimens de
l’étude. C’est pourquoi nous ne pouvons être cer-
tains des homologies chromosomiques entre les
espèces. Très souvent, les préparations standard de
caryotypes ne révèlent pas toute l’étendue des
réarrangements chromosomiques (Haiduk et al.
1981, Baker et al. 1987). Néanmoins, nos résultats
donnent une idée de l’évolution caryotypique surv-
enue chez certaines espèces et soulèvent des ques-
tions qui pourront être élucidées à l’aide des profils
de bandes chromosomiques.
3.1 Ordre des Insectivora, famille
des Soricidés
Crocidura crenata
Il est généralement admis que le genre Crocidura tire
son origine d’Afrique, et qu’il a ensuite colonisé
l’Eurasie, probablement avant la fin du Miocène
(Maddalena et Ruedi 1994, Butler 1998). Les lignées
africaine et eurasienne ont toutes deux fait l’objet
d’une importante différenciation des espèces pen-
dant et après le Pliocène. Selon Maddalena et Ruedi
(1994), le caryotype de 2n = 3640 serait primitif
dans le genre, le nombre diploïde augmentant dans le
clade africain, et diminuant dans l’embranchement
eurasien. La majorité des Crocidura africaines qui
ont été étudiées ont un caryotype de 2n = 50
(Schlitter et al. 1999).
L’espèce C. crenata a été décrite sur base de
spécimens gabonais en 1965, et depuis, elle a été
identifiée au Cameroun et dans la République
démocratique du Congo (Hutterer et Schlitter 1996).
Bien qu’elle soit considérée rare, Goodman et
Hutterer (2004) signalèrent une série de 13 spéci-
mens de cette espèce dans la région des Monts
Doudou, au Gabon. Le caryotype de cette espèce
n’avait pas encore été publié.
Les préparations de chromosomes d’un mâle de
cette musaraigne n’ont produit qu’un seul étalement
de qualité moyenne (figure 1A). Dans la cellule en
question, le nombre diploïde est 2n = 48. Les chro-
mosomes de cette cellule présentent un certain pro-
fil de bandes, bien qu’ils n’aient pas été traités avec
des agents de mise en évidence des bandes. Le pro-
fil des bandes était toutefois suffisant pour permet-
tre d’identifier les chromosomes homologues, mais
nous n’avons pas pu identifier clairement une quel-
conque homologie avec les bandes G d’autres
espèces de Crocidura (Biltueva et al. 1999, 2001).
Nous n’avons pas pu identifier de chromosomes sex-
uels, non plus.
Comme nous n’avons examiné qu’une seule cel-
lule, nous devons tenir compte de la possibilité que
le complément chromosomique que nous avons
observé ait été incomplet ou non représentatif de
Bulletin of the Biological Society of Washington, No. 12 157
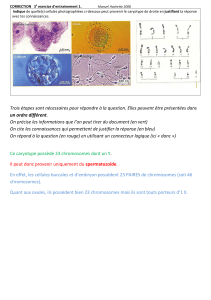
Figure 1. Caryotypes standard de musaraignes provenant
du champ pétrolifère de Rabi. (A) Crocidura crenata,
mâle, TK110269; (B) Crocidura goliath, mâle,
TK110322; (C) Crocidura grassei, mâle, TK110400;
(D) Sylvisorex ollula, mâle, TK110316.

l’individu ou de l’espèce. Une autre espèce africaine
de Crocidura (C. nigrofusca du Burundi;
Maddalena et Ruedi 1994, Schlitter et al. 1999) a un
caryotype de 2n = 48.
Crocidura goliath
Le statut taxinomique de l’espèce C. goliath a
changé plus d’une fois (voir Nowak 1997). Le taxon
a été placé dans un genre ou sous-genre distinct
(Praesorex) et a parfois été considéré comme une
sous-espèce de C. odorata. Des études moléculaires
ont placé C. goliath dans le groupe monophylétique
des Crocidura (Quérouil et al. 2001). Goodman et
al. (2001) ont signalé que l’espèce vivait en sympa-
trie avec C. olivieri dans le nord-est du Gabon.
Nous avons analysé le caryotype de deux C.
goliath mâles et trouvé un nombre diploïde de 50
chez les deux sujets (figure 1B). Le caryotype mon-
tre 3 paires de grands autosomes subtélocentriques
et 17 paires d’autosomes acrocentriques classés de
grands à petits. Trois paires additionnelles sont méta-
centriques ou submétacentriques et une paire de
petits autosomes sont subtélocentriques. Les chro-
mosomes sexuels apparents de C. goliath compren-
nent un grand X submétacentrique et un grand Y
subtélocentrique. Les autosomes de C. goliath sont
identiques à ceux de C. odorata giffardi, mais cette
dernière espèce diffère de C. goliath par son grand
chromosome X métacentrique (Meylan et Vogel
1982). Chez le genre Crocidura, le chromosome X
est habituellement grand et métacentrique, mais chez
certaines espèces, on observe plutôt un X subméta-
centrique (Maddalena et Ruedi 1994).
Crocidura grassei
Au cours des 35 années qui ont suivi la description
de cette espèce (Brosset et al. 1965), moins de 10
spécimens de C. grassei ont été signalés au Gabon,
au Cameroun, en République centrafricaine et en
Guinée-Équatoriale (Lasso et al. 1996, Goodman et
al. 2001). Cependant, des études récentes (Goodman
et Hutterer 2004, Nicolas et al. 2004) montrent que
l’espèce est abondante dans des endroits précis de
certaines régions du Gabon. Crocidura grassei
n’avait pas encore été caryotypée.
Nous avons analysé le caryotype d’une C. grassei
mâle provenant de Rabi et trouvé un nombre diploïde de
40 (figure 1C). Cinq paires de petits autosomes sont
métacentriques ou submétacentriques, trois paires d’au-
tosomes sont subtélocentriques et dix sont acrocen-
triques. Les deux autosomes restants sont hétéromor-
phes, l’un étant acrocentrique, l’autre subtélocentrique.
158 Gamba, Gabon: Biodiversité d'une forêt équatoriale africaine
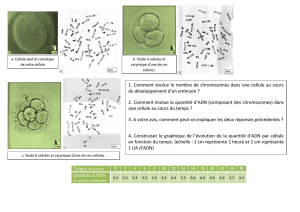
Figure 2. Préparations chromosomiques méiotiques
provenant de petits mammifères prélevés dans le champ
pétrolifère de Rabi. Tous les spécimens illustrés sont des
mâles. (A) Diacinèse chez Crocidura grassei, TK110400;
(B-C) Diacinèse chez Sylvisorex ollula, TK110316; (D)
Spermatocyte secondaire de Sylvisorex ollula, TK110316;
(E) Diacinèse chez Hylomyscus stella, TK110389; (F)
Diacinèse chez Epomops franqueti, TK110475. La flèche
indique la possibilité d’un univalent.
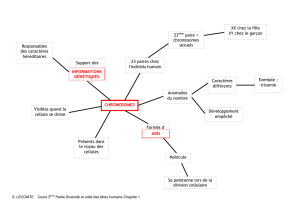
Figure 3. Caryotypes standard de rongeurs provenant du
champ pétrolifère de Rabi. (A) Heimyscus fumosus,
mâle, TK110285; (B) Hylomyscus parvus, femelle,
TK110328; (C) Hylomyscus stella, mâle, TK110389;
(D) Lophuromys nudicaudus Malacomys longipes,
mâle, TK110367.

Le chromosome acrocentrique a la même taille que le
bras long de son homologue subtélocentrique. Le bras
court est probablement hétérochromatique, et peut-être
polymorphe dans la population. Il faudrait déterminer
les profils des bandes G et C pour confirmer cette inter-
prétation. Le chromosome X est grand et submétacen-
trique; le Y, plus petit et subtélocentrique. Les chromo-
somes homologues des cellules en diacinèse de méiose
sont appariés et forment la disposition prévue de 20
chromosomes bivalents (figures 2A).
Le caryotype 2n = 40 de C. grassei est l’un des plus
bas qui aient été caractérisés chez les espèces
africaines, bien que l’on trouve un nombre diploïde
aussi peu élevé que 22 chez des espèces asiatiques du
même genre (Zima et al. 1998). Meylan (1971) sig-
nala un caryotype semblable de 2n = 40 chez l’e-
spèce africaine C. bottegi. Les caryotypes standard de
C. grassei et de C. bottegi diffèrent par les éléments
suivants : 1) la possibilité d’une inversion péricen-
trique ayant entraîné la formation d’un chromosome
acrocentrique de taille moyenne chez C. grassei et un
métacentrique chez C. bottegi; 2) un bras court sur le
chromosome X plus long chez C. grassei; et 3) une
fixation, chez C. bottegi, de la forme subtélocen-
trique de la paire hétéromorphe de C. grassei.
Il existe un degré de similarité élevé entre les
caryotypes de C. grassei et de C. bottegi, de même
qu’avec d’autres espèces africaines de Crocidura au
nombre diploïde peu élevé (2n = 3644) (Maddalena
et Ruedi 1994, Schlitter et al. 1999). Toutefois, ces
caryotypes sont très semblables au caryotype ances-
tral proposé pour le genre (Maddalena et Ruedi
1994, Zima et al. 1998), ce qui ne signifie donc pas
nécessairement une parenté étroite entre les espèces
africaines avec un nombre diploïde peu élevé.
Néanmoins, ces espèces ont probablement divergé
tôt dans le processus de diversification des espèces
africaines et dans certains cas, la divergence peut
avoir précédé l’embranchement eurasien. D’ailleurs
les études morphologiques, moléculaires et chromo-
somiques ont permis de classer C. bottegi comme
un taxon primitif ayant commencé à diverger avant la
division donnant lieu aux deux grands clades
(africain et eurasien) (Maddalena et Ruedi 1994,
Ruedi 1998). En se fondant sur la morphologie,
Brosset et al. (1965) suggérèrent un lien de parenté
étroit entre C. grassei et C. dolichura, cette
dernière ayant également été identifiée comme l’un
des membres plus primitifs du genre (McClellan
1994, Butler 1998). Le caryotype de C. grassei et
ses similarités avec ceux de C. bottegi et de C.
dolichura laissent supposer que cette espèce est issue
d’une des premières branches du genre.
Sylvisorex ollula
Les préparations de chromosomes mitotiques de
deux S. ollula mâles ont toutes les deux révélé des
caryotypes de 2n = 38 (figure 1D). Nous avons
observé 13 paires de chromosomes à deux bras et
cinq paires d’autosomes acrocentriques. Le chromo-
some X est acrocentrique, le Y, métacentrique. Nous
avons compté le nombre prévu de 19 bivalents en
diacinèse (figure 2C-2B), et les spermatocytes sec-
ondaires avaient un nombre haploïde de 19 (figure
2D). Le complément autosomal est identiques à
celui décrit pour deux spécimens du Cameroun
prélevés par Schlitter et al. (1999). Le chromosome
Y est cependant plus grand que celui observé chez
les spécimens du Cameroun, et il est métacentrique
plutôt qu’acrocentrique. Les chromosomes Y que
nous avons observés chez les spécimens de Rabi
peuvent différer dans l’addition de bras hétérochro-
matiques. Cette hypothèse pourrait être vérifiée par
la coloration des bandes C.
En se fondant sur le caryotype, Schlitter et al.
(1999) ont révélé l’existence de deux groupes de
Sylvisorex. Les espèces S. megalura et S. lunaris
ont des nombres diploïde et basal élevés, tandis que
les caryotypes des espèces S. johnstoni, S. isabel-
lae, S. morio et S. ollula ont des nombres diploïde
et basal faibles. Le fondement systématique de cette
différence a été étayé par l’analyse des séquences
géniques de l’ARNr 16S (Quérouil et al. 2001), qui
a indiqué que S. megalura est plus étroitement
apparentée au genre Suncus qu’au genre Sylvisorex à
nombre diploïde faible, qui comprend S. ollula.
3.2 Ordre des Rodentia, famille des Muridés
Heimyscus fumosus
Le caryotype de Heimyscus consiste en 40 chromo-
somes (figure 3A). Trois paires de microchromo-
somes ont deux bras et les autosomes restants sont
acrocentriques. Le chromosome X est grand et sub-
télocentrique, tandis que le Y est légèrement plus
petit et acrocentrique. H. fumosus a été observé au
Gabon, au Cameroun et en République cen-
trafricaine. Brosset et al. (1965) avaient décrit cet
animal comme un Hylomyscus. Par la suite, Misonne
(1969) a choisi le nom de Heimyscus comme nou-
Bulletin of the Biological Society of Washington, No. 12 159
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%