16. Chap.4. Ecologie

Contribution à l’étude écologique des poissons de la partie congolaise de l’Inkisi
229
IV.1. CARACTERISATION DES EAUX
Un écosystème qu’il soit aquatique ou terrestre est caractérisé par un ensemble des facteurs
écologiques. Ces derniers sont soit abiotiques, soit biotiques. Les facteurs abiotiques
comprennent l’ensemble des caractéristiques physico-chimiques du milieu et les facteurs
biotiques constituent l’ensemble des interactions qui se réalisent entre des individus de la
même espèce ou d’espèces différentes (Dajoz, 1996).
Dans ce chapitre, nous nous intéressons d’une manière très sommaire à quelques facteurs
écologiques dans les eaux de la partie congolaise du bassin de l’Inkisi, essentiellement
pendant nos échantillonnages. En effet, il est connu que les facteurs écologiques ont un rôle
déterminant pour le nombre et la nature des espèces susceptibles de cohabiter dans un
environnement donné (Hugueny et Lévêque, 2006). Matthews et al. (1992) et Philippart
(1989) ont montré que la distribution des poissons est largement influencée par la qualité
physique et chimique de l’eau (oxygène dissous, température, pH, matières en suspension,
dureté, ammoniaque, etc.…). Welcomme (1979, 1985), Welcomme & Hagborg (1977), Junk
& Welcomme (1990) ont montré l’importance du cycle saisonnier des régimes de crues, de la
durée et de l’intensité de ces dernières dans les captures des poissons des rivières en milieu
tropical. De même, Statzner & Highler (1986); Junk et al. (1989); Lowe-McConnell (1987)
soulignent le rôle de l’hydrologie comme facteur structurant de l’écologie aquatique. Enfin,
Lévêque (2006a) note que la variabilité hydrologique qui résulte de la répartition saisonnière
des pluies ou la variabilité inter-annuelle des précipitations a, des conséquences importantes
sur la biologie des espèces et sur la dynamique des peuplements de poissons.
La caractérisation de l’environnement abiotique est un des éléments clés dans la
compréhension du fonctionnement d’un écosystème. Ainsi l’objectif de ce chapitre demeure
de dégager les grands traits caractéristiques des eaux (physico-chimie) de la partie congolaise
du bassin de l’Inkisi.
IV.1.1. RAPPEL DES METHODES
L’étude a porté sur la portion du bassin où les données sur la diversité de l’ichtyofaune ont été
collectées. Sur le terrain, l’évaluation de la physico-chimie a consisté d’une part en des
mesures ponctuelles prises lors des échantillonnages et d’autre part à des observations
réalisées au fond et autour des eaux. Le plan d’échantillonnage, la liste des variables et les
appareils de mesure utilisés ont été présentés dans le chapitre 2.

Chapitre IV
230
Des prélèvements des échantillons d’eau ont été effectués dans certaines stations pour des
observations microscopiques. Les pentes moyennes et partielles ont été calculées à partir de la
différence d’altitude et de la distance entre deux points pour la représentation du profil
longitudinal.
IV.1. 2. CARACTERISTIQUES PHYSICO-CHIMIQUES DES EAUX
IV.1.2.1. Profil longitudinal de l’Inkisi
Le cours principal reste bien évidemment le premier des milieux importants du bassin. Son
état varie fortement suivant les saisons. Les eaux ont une coloration jaunâtre. La rivière Inkisi
pénètre dans le territoire congolais à une altitude de 548 m et se jette dans le fleuve Congo à
211 m d’altitude (fig.4.1). La dénivellation moyenne dans la partie congolaise, très contrastée,
est de 1,9 m par km. De la frontière angolaise à la cité de Inkisi/Kisantu, la rivière Inkisi est
navigable ; Sur cette distance de près de 130 km la dénivellation est de 39 cm par km. De
Inkisi/Kisantu à Nsanga, deux agglomérations distantes de près de 35 km, la dénivellation
passe à 1,5 m par km. A Nsanga apparaît une chute, la chute de Sanga, en forme d’escalier, de
24 m de haut, au sommet de laquelle est érigé un barrage hydroélectrique. Du bas de la pente
de Sanga au sommet de la chute de Zongo, un tronçon de 10 km, la pente s’évalue à 2,2 m au
km. A Zongo se trouve une chute dont la hauteur est de 58 m. En amont et à moins d’une
centaine de mètres de la chute est érigé un autre barrage hydroélectrique. Du bas de la chute
au confluent avec le fleuve Congo, un parcours de 6 km, la dénivellation atteint 19,7 m par
km. A l’entrée de l’Inkisi dans le fleuve se trouve une autre chute d’environ 8 m de haut.
IV.1.2.2. Variables physico-chimiques
Les données moyennes de quelques variables physico-chimiques sont consignées dans le
tableau 4.1. Les données par saison sont présentées en annexe.
IV.1.2.2.1. Profondeur et Transparence
Sur le cours principal, le niveau d’eau observé et relevé, durant les expéditions révèle un
minimum de 1,5 m (au pied de la chute de Nsanga, 04°50’39,4’’S - 15°57’28,1’’E) contre un
maximum de 4,2 m (au niveau du barrage Nsanga, 04°50’35,5’’S - 14°57’37,6,1’’E). La
profondeur maximale dans les affluents varie de quelques cm à 2,2 m.

Contribution à l’étude écologique des poissons de la partie congolaise de l’Inkisi
231
La transparence est un des facteurs souvent avancés pour expliquer la productivité et le
fonctionnement trophique des milieux aquatiques (Blaber & Blaber, 1980 ; Cyrus & Blaber,
1987a,b ; Albaret et al., 2004). La transparence de l’eau permet d’évaluer la zone euphotique
nécessaire dans l’estimation de la production primaire et la teneur de l’eau en charges solides
de diverses natures. Durant la saison sèche et compte tenu de la faible profondeur du lit de
certains affluents (moins d’un mètre par endroit) au fond duquel on aperçoit le substrat, la
pénétration des rayons solaires est totale dans la plus grande majorité des stations
prospectées. Elle est partielle et diminue pendant la saison pluvieuse du fait de nombreuses
particules entraînées par les eaux de ruissellement qui gagnent le lit des rivières. Ces
particules se trouvent généralement sous forme de grains isolés. La floculation et l’agrégation
de certains de ces particules ne se produisent globalement que lorsque la vitesse du courant
devient faible (Boucart & Francis-Boeuf, 1942).
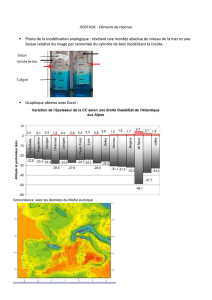
Fig. 4.1. Profil longitudinal de la partie congolaise de l’Inkisi
0255075100125150175
Distance (en km)
211
311
411
511
611
Altitude (en m)
Chute de Sanga
Chute de Zongo
Vila
Fidi
Bongolo
Luguga
Pont Inkisi/Kisantu
Fleuve Congo

Chapitre IV
232
Tableau 4.1. Variables physico-chimiques dans divers cours d’eau avec leur valeur minimale et maximale durant les pêches expérimentales
Légende C. d’eau : Cours d’eau T° : température Cond : conductivité Moy ± SD : Moyenne ± déviation standard
Min : minimum Max : maximum Kink : Kinkutu Nge : Ngeba
C. d'eau T°air T° eau pH Cond Durété O
2
(mg/l) O
2
(%) Largeur Profondeur
Vitesse Transparence
Inkisi Moy ± SD 26,9 ± 1,3
25,2 ± 0,8 7,0 ± 0,5 70,1 ± 28,9 2,1 ± 0,8 8,3 ± 0,6 97,1 ± 3,4 63,6 ± 16,0 2,2 ± 1,0 1,2 ± 0,9 1,1 ± 0,4
Min - Max 24,5 - 30,5
23,2 - 26,2 6,0 - 7,7 21,6 - 128,2 1,0 - 4,2 7,8 - 8,9 94 -106 48,0 - 84,0 1,5 - 4,2 0,1 - 3,6 0,4 - 1,8
Affluents de la rive gauche
Lamba Moy 25,3 24,0 7,1 17,5 1,0 8,0 98 4,0 0,3 0,4 0,3
Luidi Moy ± SD 27,1 ± 3,0 24,6 ± 1,3 7,4 ± 0,2
209,8 ± 64,7
6,9 ± 2,4 8,2 ± 0,5 97 ± 2,8 12,3 ± 2,0 1,2 ± 0,3 0,7 ± 0,2 0,8 ± 0,3
Min - Max 21,6 - 31,2
23,1 - 27,4 7,1 - 7,8 126,2 -294,0 4,0 - 9,9 7,9-8,5 94-101 9,3 – 22,0 0,9 -1,8 0,5 - 1,0 0,3 - 1,0
Muala Moy ± SD 26,6 ± 2,1
24,0 ± 2,1
7,4 ± 0,5
233,3 ± 96,1
7,5 ± 2,6 8,9 ± 0,4 95 ± 2,6 6,5 ± 2,6 0,8 ± 0,6 0,4 ± 0,1 0,7 ± 0,4
Min - Max 24,3 - 29,1
22,1 - 26,4 6,8 - 8,0 145,8 -362,0 5,0 - 12,0
8,3 - 9,1 88 - 99 4,0 - 10,0 0,3 - 1,5 0,3 - 0,6 0,3 - 1,0
Niama Valeurs 26,8 21,8 7,2 35,2 1 7,7 96 2,0 0,3 0,4 0,3
N'soni Moy ± SD 25,6 ± 3,3 22,5 ± 1,7 6,5 ± 0,5
12,6 ± 2,4 0,5 ± 0,2 8,9 ± 0,3 100 ± 3,6 3,3 ± 0,4 0,4 ± 0,2 0,4 ± 0,1 0,3 ± 0,1
Min - Max 20,6 - 30,7
19,7 - 24,0 5,6 - 6,9 9,5 - 15,8 0,3 - 0,5 8,6 -9,1 94 -102 2,5 - 3,6 0,3 - 0,8 0,3 - 0,6 0,2 - 0,6
Nua Moy ± SD 29,1 ± 2,5 27,3 ± 2,6 7,8 ± 0,4
135,5 ± 16,3
4,3 ± 0,5 8,8 ± 0,3 99 16,3 ± 2,7 0,6 ± 0,1 0,6 ± 0,1 0,6 ± 0,2
Min - Max 23,4 - 31,0
22,2 - 30,4 7,2 - 8,3 112,4 -159,5 4,0 - 5,2 8,5 - 9,2 94-104 13,0 - 20,6 0,4 - 0,8 0,4 - 0,8 0,2 - 0,7
Vila Valeurs 26,7 25,8 7,2 231 8 7,5 92 14,5 1,6 0,3 0,4
Affluents de la rive droite
Bongolo Moy ± SD 25,6 ± 2,9 23,6 ± 1,1 7,1 ± 0,4
87,7 ± 15,3 3,3 ± 0,7 9,7 ± 0,4 99 ± 3,8 10,8 ± 2,5 1,0 ± 0,1 1,1 ± 0,3 0,7 ± 0,3
Min - Max 20,3 - 29,4
22,3 - 25,4 6,8 - 7,8 66,7 - 102,5 2,0 – 3,5 9,4 -10,2 94 -105 8,0 - 16,0 0,6 - 1,2 0,8 - 1,2 0,4 - 1,0
Fidi Moy ± SD 28,0 ± 3,0 24,0 ± 1,5 6,7 ± 0,3
26,8 ± 8,2 1,0 ± 0,0 9,2 ± 0,3 101 ± 4,1 33,3 ± 2,5 1,7 ± 0,3 0,8 ± 0,1 1,3 ± 0,2
Min - Max 24,3 - 31,5
21,8 - 25,2 6,4 - 7,0 16,5 - 35,0 0,5 - 1,0 8,8 -9,3 95-103 32,0 - 37,0 1,3 - 2,0 0,8 - 0,9 1,1 - 1,5
Luhuha Moy ± SD 27,9 ± 2,0 24,7 ± 1,5 7,3 ± 0,4
139,8 ± 35,9
4,0 ± 1,2 8,6 ± 0,6 97 ± 2,7 4,1 ± 0,9 0,8 ± 0,1 0,5 ± 0,2 0,7 ± 0,2
Min - Max 25,6 - 29,9
22,7 - 26,1 6,9 - 7,9 89,7 - 168,8 3,0 - 5,2 8,4 - 9,3 92 - 99 3,0 - 5,0 0,6 - 1,2 0,3 - 0,7 0,4 - 0,9
Lukusu /Kink Valeurs 28,6 23,4 7,1 62,1 2,0 8,2 95 8,0 1,0 0,5 0,5
Lukusu/Nge Moy ± SD 26,4 ± 2,8 25,1 ± 1,2 7,0 ± 0,7
98,8 ± 36,0 3,5 ± 1,3 7,3 ± 0,3 96 ± 3,4 4,2 ± 0,9 0,5 ± 0,1 0,4 ± 0,1 0,5 ± 0,1
Min - Max 23,4 - 28,8
23,6 - 26,1 6,4 - 7,8 66,9 - 148,5 2,0 - 5,0 7,0-7,6 90 - 98 3,0 - 5,0 0,4 - 0,6 0,4 - 0,6 0,4 - 0,6
Ngeba Moy ± SD 26,0 ± 1,6 23,6 ± 1,4 7,1 ± 0,3
120,8 ± 31,7
4,4 ± 0,9 8,6 ± 0,2 96 ± 2,4 9,6 ± 3,7 1,5 ± 0,4 0,4 ± 0,1 1,5 ± 0,4
Min - Max 23,7 - 28,7
21,9 - 25,6 6,5 - 7,5 73,1 - 151,4 3,0 - 5,0 8,3 -8,8 92 -100 7,0 - 18,0 0,8 - 2,0 0,3 - 0,6 0,8 - 1,4
Vini Moy ± SD 27,8 ± 1,2 24,3 ± 0,9 6,4 ± 0,1
15,7 ± 3,3 0,5 ± 0,3 8,1 ± 0,2 94 ± 2,3 11,7 ± 3,2 0,8 ± 0,2 0,5 ± 0,1 0,5 ± 0,1
Min - Max 26,8 - 29,1
23,4 - 25,1 5,6 - 6,5 11,9 - 17,6 0,3 - 0,6 7,9 - 8,4 90 - 99 8,0 - 14,0 0,6 - 1,8 0,4 - 0,6 0,4 - 0,8

Contribution à l’étude écologique des poissons de la partie congolaise de l’Inkisi
233
C. d'eau T°air T° eau pH Cond Durété O
2
(mg/l) O
2
(%) Largeur Profondeur
Vitesse Transparence
Sous-affluents
Manzanza Moy ± SD 24,3 ± 0,2 22,5 ± 0,6 6,1 ± 0,4
9,8 ± 1,9 0,3 ± 0,1 8,6 ± 0,3 97± 2,6 2,7 ± 1,2 1,3 ± 1,0 0,3 ± 0,1 0,9 ± 0,5
Min - Max 23,2 - 25,6
21,3 - 24,2 5,9 - 6,6 8,7 - 12,0 0,3 – 0,4 8,3 - 8,8 91-100 2,0 - 4,0 0,2 - 2,2 0,2 - 0,4 0,2 - 1,3
Mingididi Moy ± SD 28,4 ± 1,1 25,7 ± 1,0 7,0 ± 0,6
109,7 ± 38,1
3,4 ± 0,0 8,5 ± 0,2 99 ± 2,2 3,5 ± 0,7 0,7 ± 0,2 0,4 ± 0,1 0,6 ± 0,1
Min - Max 25,2 - 31,8
24,1 - 27,4 6,6 - 7,5 82,7 - 136,6 2,7 - 4,5 8,3 - 8,8 94 -102 3,0 - 5,0 0,5 - 1,2 0,3 - 0,5 0,5 - 0,8
Nsengezi Valeurs 29,8 25,2 6,6 28,8 1,0 8,0 97 4,0 0,5 0,4 0,5
Voke Moy ± SD 27,7 ± 1,5 26,0 ± 1,7 6,0 ± 0,3
29,2 ± 3,4 1,0 ± 0,1 7,7 ± 0,2 94 ± 2,1 28,5 ± 2,1 1,4 ± 0,4 0,2 ± 0,1 0,8 ± 0,3
Min - Max 25,2 - 30,2
22,7 - 29,4 5,6 - 6,4 24,0 - 38,2 0,8 - 1,2 7,2 - 8,1 90 - 98 24,0 - 42,0
1,2 - 2,2 0,0 - 0,3 0,5 – 1,3
Wungu Moy ± SD 28,5 ± 1,9 25,1 ± 1,1 6,8 ± 0,3
40,8 ± 6,3 1,6 ± 0,3 7,8 ± 0,2 94 ± 2,1 15,2 ± 5,3 1,1 ± 0,1 0,8 ± 0,1 0,7 ± 0,2
Min - Max 24,4 - 30,7
22,4 - 26,8 6,5 - 7,3 24,6 - 56,3 0,8 - 1,9 7,3 - 8,4 90 - 99 12,0 - 25,2
0,9 - 1,5 0,5 - 1,0 0,4 - 1,3
Ruisseaux et sources
Bimbuampolo
Moy ± SD 28,1 ± 1,5 23,2 ± 0,4 5,9 ± 0,3
38,8 ± 10,1 1,3 ± 0,4 8,8 ± 0,2 99 ± 3,4 0,9 ± 0,1 0,3 ± 0,1 0,2 ± 0,1 0,3 ± 0,1
Min - Max 24,4 - 29,7
22,8 - 24,7 5,4 - 6,3 27,4 - 62,4 0,9 - 2,1 8,2 - 9,1 93 - 104 0,7 - 1,0 0,2 - 0,6 0,1 - 0,3 0,2 - 0,4
Mabuta Moy ± SD 25,4 ± 1,0 23,5 ± 1,2 5,8 ± 0,4
43,4 ± 12,8 1,5 ± 0,5 8,0 ± 0,2 98 ± 1,8 0,7 ± 0,1 0,2 ± 0,1 0,1 ± 0,1 0,2 ± 0,1
Min - Max 24,2 - 26,7
21,7 - 24,5 5,2 - 6,3 16,1 - 62,4 0,5 - 2,1 7,6 - 8,3 94 - 103 0,7 - 0,8 0,2 - 0,3 0,1 - 0,2 0,2 - 0,3
Mpika Valeurs 28,1 24,2 5,4 8,0 0,5 8,6 102 0,4 0,2 0,5 0,2
N'longo Moy ± SD 25,8 ± 0,6 24,6 ± 0,9 5,7 ± 0,3
47,8 ± 21,6 1,4 ± 0,6 8,8 ± 0,3 99 ± 2,1 0,5 ± 0,1 0,3 ± 0,1 0,1 ± 0,1 0,2 ± 0,1
Min - Max 23,4 - 26,2
23,6 - 25,6 5,3 - 6,1 23,4 - 72,3 0,8 - 2,4 8,0 - 9,3 97-103 0,4 - 0,6 0,2 - 0,4 0,0 - 0,2 0,2 - 0,3
Sanga Valeurs 28,1 25,4 5,3 12,6 0,5 8,7 99 0,7 0,3 0,2 0,3
Yabi Moy ± SD 25,9 ± 1,6 23,9 ± 0,1 5,6 ± 0,3
14,6 ± 1,5 0,5 ± 0,1 8,4 ± 0,3 95 ± 1,8 0,6 ± 0,1 0,3 ± 0,1 0,1 ± 0,1 0,2 ± 0,1
Min - Max 23,7 - 27,0
22,0 - 25,0 5,4 - 5,8 12,8 - 16,4 0,4 - 0,7 8,0 - 8,8 91 - 100 0,5 - 0,8 0,2 - 0,4 0,0 - 0,2 0,2 - 0,4
Yoyila Moy ± SD 25,8 ± 0,3
22,6 ± 0,4 5,6 ± 0,1
56,4 ± 6,2 1,6 ± 0,3 7,9 ± 0,4 94 ± 2,4 1,0 ± 0,3 0,2 ± 0,1 0,1 ± 0,1 0,2 ± 0,1
Min - Max 24,3 - 26,3
21,3 - 23,9 5,2 - 6,3 42,0 - 60,8 1,4 - 2,0 7,1 - 8,2 90 - 100 0,6 - 1,4 0,2 - 0,3 0,1 - 0,2 0,2 - 0,3
Zua Moy ± SD 26,7 ± 1,7 24,4 ± 1,6 5,8 ± 0,2
13,7 ± 3,8 0,5 ± 0,0 9,0 ± 0,2 101 ± 1,9
0,5 ± 0,1 0,3 ± 0,1 0,1 ± 0,1 0,3 ± 0,1
Min - Max 23,8 - 28,6
22,5 - 26,2 5,4 - 5,9 11,0 – 17,4 0,4 - 0,6 8,2 - 9,4 95 - 105 0,4 - 0,6 0,2 - 0,4 0,0 - 0,2 0,2 - 0,4
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
1
/
28
100%