tutorat physique

2010-2011 Tutorat UE spécifiques – Méthodes d’étude et d’analyse du génome 1 / 8
TUTORAT UE spécifiques 2010-2011
Méthodes d’étude et d’analyse du génome
Eric Badia, Bernard Carcy
CORRECTIONS
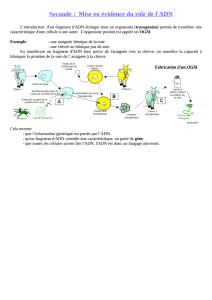
QCM n°1 : Ligature d'extrémités d'ADNs coupés par des enzymes de restriction
de type II différentes
=> si les extrémités libérées par les 2 enzymes de restriction différentes sont
franches, on pourra toujours effectuer la ligature.
=> si les extrémités libérées par les 2 enzymes de restriction différentes sont
cohésives, on ne pourra effectuer la ligature que si les extrémités cohésives libérées
sont complémentaires.
=> On ne peut ligaturer une extrémité cohésive avec une extrémité franche.
Sur le plasmide étudié il y a 2 sites SmaI (1 et 2), 1 MxaI, 1 PvuI, 1 AbrI et 1 NopI.
A- VRAI: cas d'une ligature MxaI/SmaI. La coupure du plasmide circulaire par ces 2
enzymes libérerait 3 fragments linéaires : MxaI-SmaI(1) contenant le fragment noir,
SmaI(1)-SmaI(2), et SmaI(2)-MxaI contenant le fragment grisé d'intérêt. Les 2
enzymes libérant des extrémités franches différentes, on pourrait donc effectuer
leur ligature des deux extrémités franches SmaI(2) et MxaI. Il en résulterait une
séquence GAGggg (GAG provenant de l'extrémité MxaI et ggg de l'extrémité
SmaI(2)) qui permettrait de recirculariser un plasmide ne contenant plus le fragment
noir mais toujours le fragment grisé. Notez que cette séquence ne pourrait plus être
coupée par ces 2 enzymes une fois les 2 extrémités ligaturées.
B- FAUX: cas d'une ligature SmaI seul. La coupure du plasmide circulaire par
l'enzyme SmaI libérerait 2 fragments linéaires SmaI(1)-SmaI(2). Un des deux
fragments ne contiendrait ni la séquence noire ni la séquence grisée alors que
l'autre contiendrait ces 2 séquences.
C- VRAI: cas d'une ligature AbrI/NopI. La coupure du plasmide circulaire par
ces 2 enzymes libèrerait 2 fragments linéaires NopI-AbrI. Un des deux
F
FA
AC
CU
UL
LT
TE
E
d
de
e
P
PH
HA
AR
RM
MA
AC
CI
IE
E
AbrI
SmaI(1)
SmaI(2)
Mxa1
PvuI
NopI

2010-2011 Tutorat UE spécifiques – Méthodes d’étude et d’analyse du génome 2 / 8
fragments ne contiendrait que la séquence noire alors que l'autre ne
contiendrait que la séquence grisée d'intérêt. Ces 2 enzymes, bien que
possédant des sites de reconnaissance différents, libèrent des extrémités
cohésives simple brin identiques (5'TCGA).
AbrI: 5' C/TCGAG=> 5'C3' + 5'TCGAG-3'
3' GAGCT/C 3'GAGCT5' C-5'
NopI: 5' g/tcgac=> 5'g + 5'tcgac-3'
3' cagct/g 3'cagct5' g-5'
Il serait alors possible de recirculariser le plasmide avec le fragment
grisé d'intérêt par ligature des 2 extrémités cohésives comme suit:
5'Ctcgac3' ou 5'gTCGAG3''
3'GAGCTg5' 3'cagctC5'
D- FAUX: cas d'une ligature AbrI/PvuI. La coupure du plasmide circulaire par
ces 2 enzymes libèrerait 2 fragments linéaires AbrI-PvuI. Un des deux
fragments ne contiendrait que la séquence noire alors que l'autre ne
contiendrait que la séquence grisée d'intérêt. Cependant ces 2 enzymes, qui
possédent des sites de reconnaissance différents, libèrent des extrémités
cohésives simple brin non complémentaires (5'TCGA pour AbrI et 5'CG pour
PvuI).
AbrI: 5' C/TCGAG=> 5'C3' + 5'TCGAG-3'
3' GAGCT/C 3'GAGCT5' C-5'
PvuI: 5' tt/cgaa=> 5'tt + 5'cgaa-3'
3'aagc/tt 3'aagc5' tt-5'
Malgré l'existence d'un fragment grisé d'intérêt après coupure du plasmide par
AbrI/PvuI, il est donc impossible de recirculariser le plasmide.
E- FAUX: cas d'une ligature NopI/MxaI. La coupure du plasmide circulaire par
ces 2 enzymes libèrerait 2 fragments linéaires NopI-MxaI. Cependant, aucun
des 2 fragments ne contiendrait que la séquence grisée. De plus il serait
impossible de religaturer le plasmide après coupure puisqu'une des enzymes
libère des extrémités cohésives (NopI) et l'autre (MxaI) des extrémités
franches. Donc il serait impossible de les ligaturer.
QCM2: Synthèse d'une protéine recombinante
A- VRAI: la boite de petri contenant de l'ampicilline, seules les bactéries
transformées par des plasmides peuvent croître sur cette boite. En effet, le gène
AmpR est présent sur le plasmide et les bactéries transformées sont donc
résistantes à l'antibiotique. A l'inverse, les bactéries non transformées par un
plasmide sont sensibles à l'antibiotique et sont donc éliminées par l'ampicilline.
B- FAUX: la coloration bleue signifie que le substrat X-gal (incolore) a été dégradé
en bromo-chloro-indol (bleu). La dégradation du substrat X-gal signifie donc qu'il y a
une activité -galactosidase et qu’il y a donc eu -complémentation (association des
peptides et ) dans la bactérie. Or l' -complémentation n'est possible que si le
peptide n'est pas recombinant, donc s'il n'y a pas eu insertion de l’ADNc dans le

2010-2011 Tutorat UE spécifiques – Méthodes d’étude et d’analyse du génome 3 / 8
gène lacZ porté par le plasmide. Ainsi, la coloration bleue signifie que la bactérie
est transformée par un plasmide non recombinant.
C- FAUX: Puisque le clonage concerne un seul ADNc, il suffit d'un seul clone blanc
sur la boite pour que le clonage soit réussi. Par contre si l'on avait voulu construire
une banque d'ADN, il faudrait au moins 95% de clones blancs pour considérer que la
banque est représentative du génome fragmenté.
D- FAUX: C'est l'IPTG qui assure ce rôle dans la bactérie. En fixant le répresseur
codé par lacI, il l'empêche de se fixer sur l'opérateur présent en amont du gène
lacZ. Ceci permet donc la fixation de l'ARN polymérase sur le promoteur et donc la
transcription/traduction de l’ADNc cloné. On dit que l'IPTG est l'inducteur de la
synthèse du peptide (recombinant ou non) codé par lacZ.
E- FAUX: Le choc thermique des cellules compétentes (dont la paroi est
préalablement fragilisée au CaCl2) de 0 à 42°C est une autre méthode de
transformation bactérienne.
QCM3: digestion par les enzymes de restriction de type II.
A- FAUX : le champ pulsé est utilisé pour la séparation électrophorétique de
fragments d'ADN de grande taille (>20kpb).
B- FAUX: Si l'enzyme A était inactive, le profil A+B serait identique au profil B. La
taille du plasmide étant identique qu'il soit ou non digéré par l'enzyme de restriction A
indique qu'il existe un seul site de restriction A sur ce vecteur. A a donc linéarisé le
plasmide après coupure.
C- VRAI: le profil B révèle un seul fragment de 1000pb alors que le plasmide fait
3000pb. Cela indique qu'il y a bien 3 sites B équidistants.
D- VRAI: La digestion A+B génère des fragments de 500 et 1000pb. Vu qu'il y a 3
fragments de restriction B de 1000pb, la révélation d'un fragment de restriction de
500 pb dans la digestion A+B indique obligatoirement que l'unique site A est situé au
centre d'un fragment de restriction B de 1000pb. Par conséquent, A est en position
diamétralement opposé à un site B (A localisé a 1500pb de B1 sur le schéma).
E- FAUX: La digestion A+B génère 2 fragments de 1000pb (B1-B2 et B1-B3) et 2 de
500pb (B3-A et B2-A).
QCM n°4 : PCR
A- FAUX : pour trouver la T°d'hybridation (Th) des amorces il faut calculer le point de
fusion (Tm) des 2 amorces et se placer 5°C en dessous du plus petit point de fusion
des 2 amorces.
Les séquences des 2 amorces utilisées pour amplifier la séquence d'intérêt sont
5'ATCGGGATTC3' (amorce sens) et 5'CGCTAGGTTT3' (amorce anti-sens). Le point
B1
B2
B3
A
1000pb
500pb
500pb
1000pb

2010-2011 Tutorat UE spécifiques – Méthodes d’étude et d’analyse du génome 4 / 8
de fusion de ces 2 amorces est donc de (4x5)+(2x5) soit 30°C. Ainsi, la Th de la PCR
serait réglée à 25°C.
B- FAUX: Elle est choisie aux alentours de 70°C car on utilise une ADN polymerase
thermorésistante (par exemple la Taq ADN polymerase extraite de la bactérie
thermophile Thermus aquaticus). La découverte de cette enzyme thermorésistante
(qui n'est pas dénaturée même à une T° de dénaturation de l'ADN d'environ 90°C) a
permis d'automatiser la technique et de développer les thermocycleurs.
C- FAUX: La taille du fragment amplifié comprend la taille des 2 amorces
puisqu'elles font partie des fragments d'ADN synthétisés de 5'->3' par l'ADN
polymerase (la polymérisation s'effectue par ajout de dNTP libre à l'extrémité 3' OH
de l'amorce). Le fragment amplifié fait donc 70pb.
D- FAUX: Une amorce a une orientation 5'->3'. L'hybridation d'une amorce ne peut
donc se faire que sur sa séquence complémentaire mais également uniquement de
façon anti-parallèle (sur un brin d'orientation 3'->5') afin de reconstituer un ADN
double brin anti-parallèle.
En D, les deux amorces proposées sont bien complémentaires des deux séquences
matricielles. Cependant, elles ne pourront pas s'hybrider puisque chaque amorce et
sa matrice correspondante contenant la séquence complémentaire ont la même
orientation 5'->3'.
E- VRAI: A l'inverse de D, ces deux amorces s'hybrideront sur leur séquence
matricielle complémentaire respective et de façon anti-parallèle. Il en résultera donc
une polymérisation de chaque brin de 5'->3' et donc l'amplification génique
(exponentielle) de la séquence comprise entre les 2 amorces.
QCM n°5 : Enzymes de restriction de type II
A) FAUX: La spécificité de reconnaissance des enzymes de restriction de type II est
le plus souvent absolue mais pas toujours. Par exemple, l’enzyme NspIV
reconnaît un site de 5 paires de bases 5’G/GNCC3’ où N est A,C,G ou T. Ainsi,
quel que soit N, s’il est encadré en 5’GG et CC3’ alors NspIV coupe l’ADN.
B) VRAI pour la majorité des enzymes de restriction de type II. Palindromique
signifie que la séquence d’ADN double brin se lit de la même manière de 5’ vers
3’ quel que soit le brin étudié (Ex : 5’GAATTC3’)
C) FAUX : Une fois la séquence reconnue, une enzyme de restriction de type II clive
généralement au niveau du site de reconnaissance.
D) VRAI : Dans la forme non mutée, A et B correspondent à 2 sites reconnus à la
fois par AatI (AGG/CCT) et HaeII (GG/CC). Ainsi, même si la séquence reconnue
par les deux enzymes n’est pas la même, les deux enzymes coupent au même
endroit (entre G et C) au niveau des séquences A et B. Les fragments de
restriction résultants (3+2+5kpb) sont donc les mêmes.
E) VRAI : Dans la forme mutée, la mutation A->T du site B fait qu’il ne pourra plus
être reconnu par l’enzyme AatI (site de reconnaissance absolue de 6pb). Ainsi,
contrairement à la forme non mutée où la digestion par AatI produit 3 fragments
de restriction (3+2+5kpb), une telle digestion de la forme mutée du gène ne
produira plus que 2 fragments de restriction (3+7kpb). Cette variation dans la
taille des fragments de restriction montre que la mutation sera donc décelable
grâce à AatI. A l’inverse, la mutation A->T du site B n’altère pas la coupure de ce
site par HaeIII puisque son site de reconnaissance absolue GG/CC est toujours
présent. Hae III ne pourra donc pas différencier les allèles mutés et non mutés.

2010-2011 Tutorat UE spécifiques – Méthodes d’étude et d’analyse du génome 5 / 8
QCM n°6 : Détection de la mutation par Southern blot
Dans le cas d’un individu homozygote pour la mutation : seul le site A du fragment
de 10kpb d’intérêt sera coupé par AatI et ceci sur les 2 allèles. Le site A étant situé à
3kpb de la région de référence (0kpb), on obtiendra donc deux fragments de
restriction de 3 et 7kpb. La sonde radioactive s’hybridant dans la région 2-4 kpb, elle
sera capable de s’hybrider (bien que partiellement) sur ces 2 fragments. On
observera donc un profil autoradiographique avec deux bandes de 3 et 7 kpb dans le
cas d’un individu homozygote pour la mutation (profil D).
Dans le cas d’un individu hétérozygote : l’allèle normal sera coupé par AatI au
niveau des sites A et B alors que l’allèle muté ne sera coupé qu’au site A. Il en
résulte la libération de 3 fragments de restriction de 3+2+5kpb sur la copie normale
et de 2 fragments de 3+7kpb sur la copie mutée. La sonde hybridant dans la région
2-4 kpb, elle sera capable de s’hybrider (partiellement) sur les 2 fragments de la
copie mutée mais uniquement sur les fragments de 2 et 3 kpb de la copie normale.
En effet le fragment de 5 kpb étant situé en dehors de la région d’hybridation, il ne
sera pas décelable par la sonde et donc ne sera pas visible sur l’autoradiographie.
Ainsi les seuls fragments visibles par autoradiographie seront ceux de 2, 3 et 7 kpb.
Un tel profil correspond au profil E. Il s’agit donc de l’hétérozygote.
(Attention, le profil E indiqué n’est pas le même pour certaines versions imprimées)
QCM7: Détection de la mutation par PCR-restriction
A- FAUX : C’est la PCR en temps réel qui permettrait de quantifier.
La PCR restriction permet de savoir si un individu est homozygote ou hétérozygote au
niveau d’un locus donné pour une mutation touchant un site de restriction (cette
mutation peut créer ou abolir un site de restriction). Pour ce faire, on amplifie par PCR
la région portant la mutation et l’on digère le fragment PCR par l’enzyme de restriction.
Après analyse du résultat de la digestion par électrophorèse et coloration de l’ADN au
bromure d’éthidium (intercalant de l’ADN qui permet de visualiser l’ADN sous les UV),
la présence ou non de la mutation génère 3 profils distincts selon que les individus
sont homozygote N/N, hétérozygote N/M ou homozygote M/M.
B- VRAI : Chez un sujet homozygote non muté, les séquences A et B sont coupées par
Aatl. La PCR à l’aide d’un couple d’amorces O1/O2 permet d’amplifier un fragment
d’ADN de 2 kpb pour chaque allèle. Chacun de ces fragments contient le site B non
muté situé à 1 kpb de O1 ou O2. La digestion de ce fragment de 2kpb par AatI libère
donc 2 fragments d’1kpb (O1B et BO2) pour chaque allèle normal. Il en résulte 4
fragments d’1kpb. Etant tous à la même taille, on ne visualise qu’une seule bande
d’1kpb sur gel après révélation par le bromure d’éthidium.
C- VRAI : Chez un sujet homozygote muté, seules les séquences A sont coupées par
Aatl. Comme précédemment, la PCR à l’aide d’un couple d’amorces O1/O2 permet
d’amplifier un fragment d’ADN de 2 kpb pour chaque allèle muté et chacun de ces
fragments contient le site B muté situé à 1 kpb de O1 ou O2. Cependant, de part la
mutation A->T dans lez site B, la digestion de ce fragment de 2kpb par AatI n’est plus
possible. Il en résulte donc 2 fragments de 2kpb. Etant tous à la même taille, on ne
visualise qu’une seule bande de 2kpb sur gel après révélation par le bromure
d’éthidium.
D- FAUX : Chez un sujet homozygote non muté, les séquences A et B sont coupées par
Aatl. La PCR à l’aide d’un couple d’amorces O1/O3 permet d’amplifier un fragment
d’ADN de 4 kpb pour chaque allèle. Chacun de ces fragments contient le site B non
muté situé à 1 kpb de O1 ou 3 kpb de O3. La digestion de ce fragment de 4kpb par
AatI libère donc 1 fragment d’1kpb (O1B) et de 3 kpb (BO3) pour chaque allèle
normal. Il en résulte 4 fragments (2 d’1kpb et 2 de 3kpb). On visualisera donc 2
bandes d’1 et 3kpb sur gel après révélation par le bromure d’éthidium.
 6
6
 7
7
 8
8
1
/
8
100%