Prise en charge de l`hyperhidrose primitive invalidante

Mini-revue
Sang Thrombose Vaisseaux 2010 ;
22, n° 6 : 302-10
doi: 10.1684/stv.2010.0493
Prise en charge de l’hyperhidrose primitive invalidante
Pierre Mordant, Yves Castier, Jean-Michel Maury, Alexandre Karsenti, Nikolaos Paraskevas,
Pierre Cerceau, Fadi Francis, Guy Lese
`che
Service de chirurgie vasculaire, thoracique et de transplantation pulmonaire, faculté Diderot, hôpital Bichat-Claude-Bernard,
AP-HP, Paris-VII, Paris, France
Résumé
.
L’hyperhidrose primitive invalidante est de
´finie par une hypersu-
dation pathologique pouvant toucher les mains, les aisselles ou les pieds.
L’hyperhidrose re
´sulte d’une de
´re
´gulation du syste
`me nerveux sympathique
qui re
´gule l’activite
´de circulation capillaire et de sudation. De premie
`re
intention, la prise en charge de l’hyperhidrose est base
´e sur des traitements
locaux par les sels d’aluminium et sur des se
´ances d’ionophore
`se. En
cas d’hyperhidrose axillaire, un traitement par toxine botulinique peut
e
ˆtre tente
´. En cas d’e
´chec des traitements me
´dicaux, les patients atteints
d’hyperhidrose peuvent be
´ne
´ficier d’une intervention chirurgicale visant a
`
interrompre l’hyperactivite
´pathologique du syste
`me sympathique : la
sympathectomie thoracique endoscopique. Ce traitement est efficace dans
la tre
`s grande majorite
´des cas d’hyperhidrose primitive invalidante, au
prix d’une hypersudation compensatrice fre
´quente, mais peu invalidante.
Mots cle
´s:hyperhidrose primitive, sympathectomie thoracique endoscopique
Abstract
Management of invalidating primary hyperhidrosis
Hyperhidrosis is a medical condition characterized by excessive sweating,
usually localized to specific parts of the body, such as the hands, feet and
armpits. Hyperhidrosis results from dysregulation of the autonomous
system with sympathetic hyperactivity. As a first step, the medical manage-
ment of hyperhidrosis is based on aluminium chloride antiperspirants,
iontophoresis, and botulinum toxin injections in case of axillary involve-
ment. If medical treatment fails to control the disease and to improve
patient’s quality of life, endoscopic thoracic sympathectomy can be perfor-
med. This surgical technique is associated with high satisfaction rates,
despite frequent but benign compensatory sweating.
Key words:primitive hyperhidrosis, endoscopic thoracic sympathectomy
L’hyperhidrose primitive correspond à une production de sueur plus importante
que ne le voudraient les besoins de la thermorégulation. En pratique, l’hype-
rhidrose peut être très invalidante, mais sa définition reste souvent subjective,
et peut poser des problèmes diagnostiques. Cet article rappelle l’anatomie et la
Correspondant :
Y. Castier
302 STV, vol. 22, n°6, juin/aou
ˆt 2010
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 03/06/2017.

physiologie du système nerveux sympathique, décrit
la prise en charge des patients atteints d’hyperhidrose
primitive invalidante, en insistant sur les traitements
médicaux et chirurgicaux disponibles, et leurs indications
respectives.
Anatomie
Le système orthosympathique, appelé sympathique dans la
suite de cet article, est essentiellement d’origine médullaire,
les centres siégeant au niveau de la moelle dorsale.
La chaîne ganglionnaire latérovertébrale s’étend du cou
jusqu’au coccyx. Cette chaîne ganglionnaire donne nais-
sance à des branches efférentes qui rejoignent soit les
nerfs rachidiens à chaque étage (rameaux communicants
gris), soit les nerfs splanchniques qui se dirigent vers
les plexus pré- ou intraviscéraux cervicaux, thoraciques,
abdominaux, lombaires et pelviens.
Àl’étage thoracique, la chaîne ganglionnaire latéroverté-
brale se situe au sein des tissus cellulograisseux sous-
pleuraux, en avant des articulations costotransversaires et
des vaisseaux métamériques intercostaux. Elle est généra-
lement visible à travers la plèvre pariétale, en arrière de la
veine azygos à droite et de la veine hémiazygos à gauche.
Le troisième ganglion cervical et le premier ganglion thora-
cique fusionnent pour former le ganglion stellaire, les
deuxième et troisième ganglions thoraciques ne sont pas
toujours parfaitement individualisables, et le troisième
ganglion thoracique peut être fusionné avec le quatrième.
Les ganglions de la chaîne thoracique haute ne sont pas
toujours apparents. Il existe des fibres nerveuses aberrantes
soit à récurrence cervicale, soit d’origine cervicale. À ces
limites près, la main est classiquement sous la dépendance
de T2 à T3, alors que l’aisselle dépend de T3 à T5.
Physiopathologie
Le système sympathique est composé d’un neurone prégan-
glionnaire, dont le corps cellulaire est localisé dans la moelle
épinière, et d’un neurone postganglionnaire, dont le corps
cellulaire est localisé dans un ganglion, qui présente un long
prolongement se terminant au niveau des organes. Le
neuromédiateur des neurones préganglionnaires est l’acé-
tylcholine. Les médiateurs des neurones postsynaptiques
sont les catécholamines. Ainsi, l’action générale du sys-
tème sympathique vise à préparer l’organisme à une situa-
tion de menace et d’action, en provoquant sudation,
mydriase, tachycardie, hypertension artérielle, vasocons-
triction périphérique, bronchodilatation, ralentissement du
transit intestinal et relaxation vésicale.
Aux membres supérieurs, la sudation isotonique assure la
thermorégulation et l’hydratation cutanée à partir de la
circulation capillaire au niveau des mains et des aisselles.
L’hyperhidrose correspond à une production de sueur plus
importante que ne le voudraient les besoins de la thermoré-
gulation. L’hyperhidrose peut être primitive ou secondaire à
certains états cliniques ou pathologiques spécifiques
(ménopause, obésité, anxiété, hyperthyroïdie, phéochro-
mocytome, tumeur carcinoïde). Ainsi, l’hypertonie sympa-
thique serait responsable de l’hyperhidrose primitive.
L’innervation sympathique palmaire est véhiculée par les
racines T2 et T3, la racine T2 véhiculant l’innervation
principale des glandes sudoripares de la main. L’innerva-
tion sympathique axillaire naît des racines T4 et T5.
En l’absence de pathologie médicale associée, l’origine de
cette hyperactivité sympathique reste inconnue. Si l’hyper-
hidrose primitive semble évoluer selon un mode spora-
dique, une transmission familiale autosomique dominante
à pénétrance incomplète a été évoquée [1]. Des études géné-
tiques situent un des locus incriminés entre 14q11,2 et q13,
sans que ces données n’aient été confirmées à ce jour [2]. En
pratique, des antécédents familiaux et des troubles psycho-
logiques sont parfois retrouvés sans qu’un lien de cause à
effet puisse être affirmé. L’excrétion de la sueur est pulsa-
tile, de 0,3 à 12 excrétions par minute. Dans l’hyperhidrose,
les glandes sudorales sont normales, mais leurs réponses
aux stimuli sont excessives et la sudation peut être dix fois
plus élevée que la moyenne, jusqu’à un litre par jour [3].
E
´pide
´miologie
La fréquence de l’hyperhidrose primitive est difficile à
évaluer. En Amérique du Nord, l’hyperhidrose primitive
touche entre 1,4 et 2,5 % de la population [4], dont près
d’un tiers de formes invalidantes. Sa fréquence est particu-
lièrement élevée en Asie : sa prévalence atteindrait 4,36 %
dans une étude épidémiologique récemment menée auprès
d’adolescents chinois. Dans cette population, la prévalence
des formes invalidantes serait de 0,27 % [5].
Clinique
Circonstances de découverte
L’hyperhidrose primitive des membres supérieurs débute le
plus souvent au cours de l’enfance ou de l’adolescence, et
persiste toute la vie. La symptomatologie est symétrique, et
affecte le plus souvent mains et aisselles (50 % des cas),
puis les aisselles seules (30 %) et enfin les mains seules
(20 %). L’hyperhidrose est fréquemment provoquée par
303
STV, vol. 22, n°6, juin/aou
ˆt 2010
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 03/06/2017.

un facteur émotionnel, plus rarement par la chaleur, un
exercice physique ou l’alimentation. La transpiration est
également augmentée à l’état basal et disparaît la nuit.
Retentissement psychologique et social
Cette transpiration extrême est gênante pour le patient et
visible par son entourage, entraînant un handicap social
important, allant de l’impossibilité de serrer des mains à
la difficulté d’entretenir des relations amoureuses. Les
symptômes débutent le plus souvent dans l’enfance et se
majorent à l’adolescence. Les jeunes adultes deviennent
timides et retirés. Le travail personnel à la maison, comme
l’écriture à la main, devient difficile, car la sueur tache le
papier et fait baver l’encre. L’hyperhidrose peut être
associée à une phobie sociale, une érythrophobie ou un
érythème pudique.
Examen clinique
La première étape d’évaluation de la transpiration excessive
inclut un interrogatoire et un examen clinique complet.
Le stress de la consultation favorise généralement les
phénomènes de formation de gouttes de sueur. Les patients
développent souvent des stratégies organisées pour
s’essuyer les mains (mouchoirs à la main ou pantalon en
coton absorbant). Dans les cas typiques d’hyperhidrose
primitive, aucun examen complémentaire n’est requis. En
cas de doute, des examens radiologiques et sanguins sim-
ples permettront d’éliminer une étiologie d’hyperhidrose
secondaire. Une fois porté le diagnostic d’hyperhidrose
primitive, une évaluation de la sévérité de la maladie et de
son retentissement doit être menée.
Prise en charge diagnostique
Évaluation de la gravité de l’hyperhidrose
En théorie, la quantité de sueur produite, correspondant aux
pertes insensibles en eau, peut être évaluée à l’aide d’un
tewamètre ou d’un évaporimètre en appliquant sur la peau
une sonde spécifique mesurant le flux de pression partielle
de vapeur d’eau évaporée entre deux capteurs. Cependant,
cette technique est lourde et réservée à la recherche. En
pratique, seuls le test de gravimétrie et le test du gant sont
pratiqués. La quantité de sueur axillaire peut être estimée
par gravimétrie : après avoir enlevé les lipides de surface,
une plaque absorbante est pesée avant et après application
sur la peau. La quantité de sueur palmaire est estimée par le
test du gant : une matière absorbante de poids connu est
placée sur les paumes du patient, qui enfile ensuite un
gant étanche. Après une attente d’une heure dans une
atmosphère calme et tempérée, le gant est retiré et la matière
absorbante est pesée à nouveau. La quantité de sueur
produite correspond là encore à la différence des poids.
La gravité de la maladie peut également être estimée par une
échelle. L’échelle de sévérité de l’hyperhidrose (hyperhi-
drosis disease severity scale, [HDSS]) est une échelle
spécifique établie pour mesurer la gravité de l’hyperhidrose
selon ses conséquences quotidiennes et proposer un algo-
rithme de traitement [6]. En pratique, le patient choisit la
phrase qui reflète le mieux sa gêne parmi une liste de quatre
phrases. Un score de 3 ou 4 indique une hyperhidrose
sévère, alors qu’un score de 1 ou 2 indique une hyperhi-
drose légère à modérée (figure 1).
Évaluation de l’étendue de l’hyperhidrose
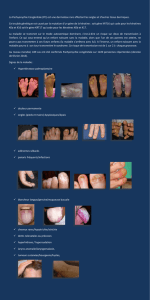
Le test au Lugol
®
(Minor’s starch-iodine test) est utilisé
pour évaluer la surface cutanée concernée par l’hypersuda-
tion, sans donner d’indication sur sa gravité. Ce test
commence par l’application d’une solution iodée (Lugol
®
)
sur les surfaces suspectes, puis l’examinateur attend que la
peau sèche et l’enduit de poudre amidonnée, le plus souvent
de la fécule de pomme de terre. En cas d’hypersudation, un
complexe amidon-iode-chlorure se forme, et la peau prend
une teinte violet foncé. Ce test est utilisé pour estimer la
surface à traiter, mais ne donne pas d’indication sur la
sévérité de la maladie.
Évaluation du retentissement sur la qualité de vie
L’hyperhidrose primitive a un impact majeur sur la qualité
de vie. L’échelle des perturbations liées à la maladie (illness
intrusive rating scale, [IIRS]) est une échelle aspécifique
qui mesure à quel point la maladie, son traitement ou la
conjonction des deux interfèrent avec les activités quoti-
diennes dans 13 domaines jugés importants pour la qualité
Hyperhidrosis Disease Severity Scale
My (underarm) sweating is never noticeable and
never interferes with my daily activities
My (underarm) sweating is tolerable but sometimes
interferes with my daily activities
My (underarm) sweating is barely tolerable and
frequently interferes with my daily activities
My (underarm) sweating is intolerable and always
interferes with my daily activities
Score 1
Score 2
Score 3
Score 4
Figure 1.Échelle de sévérité de l’hyperhidrose [6].
304 STV, vol. 22, n°6, juin/aou
ˆt 2010
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 03/06/2017.

de vie [7]. Le questionnaire d’impact de l’hyperhidrose
(hyperhidrosis impact questionnaire, [HHIQ]) est une
échelle spécifique comprenant des items pour le diagnostic
et des items pour le suivi. Ce test est plus utilisé en recher-
che qu’en pratique courante [6].
Recherche de complications médicales
Une augmentation du nombre d’infections cutanées a récem-
ment été rapportée dans une étude cas témoin incluant
387 patients atteints d’hyperhidrose [8]. Les patients avaient
consulté dans un même service entre 1993 et 2005, après une
durée moyenne de symptômes de 8,9 années. Cette étude
retrouvait une augmentation importante de la fréquence des
infections fongiques, bactériennes et virales. Le risque de
kératolyse ponctuée, de dermatophytose et de verrue était
particulièrement augmenté. Une corrélation entre l’hyper-
hidrose et la dermatite atopique a également été observée.
Prise en charge psychologique et sociale
Les troubles psychologiques, dont se plaignent les patients,
sont le plus souvent une conséquence de l’hyperhidrose.
Cependant, le traitement de cette cause ne doit pas faire
négliger la prise en charge d’une perte de confiance en soi
et d’une exclusion sociale parfois larvée. Cette prise en
charge peut être réalisée par une attitude rassurante en
consultation, par un entretien auprès d’un psychologue
ou d’un psychiatre, et par le recours aux associations de
patients. Très actives dans le domaine de l’hyperhidrose
primitive et de l’érythrophobie, ces associations peuvent
fournir un soutien important à des patients parfois désorien-
tés. En France, les patients se sont regroupés au sein de
l’association France Hyperhidrose (http://francehyperhi-
drose.org). Une association internationale, l’International
Hyperhidrosis Society, a également été créée (http://www.
sweathelp.org).
Traitements me
´dicaux
Sels d’aluminium
De première intention, les patients reçoivent des antiperspi-
rants. Ces topiques contiennent des sels d’aluminium et des
complexes de métaux qui agissent par kératinisation et
obturation des orifices sudoraux. Ils n’ont qu’une action
limitée aux hypersudations modérées [3]. Pour les hypersu-
dations sévères, des sels d’aluminium plus concentrés
(20 %) peuvent être prescrits. La peau doit être sèche
avant l’application afin d’éviter la formation d’acide
chlorhydrique. Idéalement, le topique doit être appliqué
au coucher afin de profiter de l’inactivité relative des
glandes sudoripares durant la nuit, puis de laver le produit
au petit matin. D’éventuelles irritations cutanées peuvent
être traitées avec des corticoïdes locaux. Les sels d’alumi-
nium doivent être appliqués toutes les nuits jusqu’à effica-
cité, les applications peuvent ensuite être espacées [9].
Anticholinergiques
Les traitements anticholinergiques par voie orale (glyco-
pyrrolate, propanthéline) présentaient un rapport bénéfice/
risque très défavorable. En effet, la posologie nécessaire à
l’assèchement de la transpiration entraîne des effets secon-
daires tels que xérostomie, mydriase, cycloplégie, dysfonc-
tion intestinale ou vésicale, et même des troubles mentaux.
La plupart des patients atteints d’hyperhidrose ne peuvent
supporter ces traitements très longtemps, et les anticholiner-
giques ont été progressivement abandonnés dans cette
indication [9].
Ionophorèses
Le traitement médical le plus actif reste l’ionophorèse, qui a
été popularisé en 1968. Ce traitement est défini comme
l’introduction d’une substance ionisée à travers la peau
intacte grâce à l’application d’un courant électrique. Cepen-
dant, l’ajout d’une substance au bain d’électrophorèse s’est
progressivement révélé inutile. Les ionophorèses actuelles
sont donc réalisées avec de l’eau du robinet, et suivent le
principe de l’électrolyse, même si le mode d’action exacte
de cette technique reste inconnu. Cette méthode induirait
une irritation du pore et la formation d’un bouchon réaction-
nel. Il s’agit d’une méthode efficace, mais contraignante,
nécessitant 10 à 20 séances en traitement d’attaque, puis
des séances d’entretien en continu [3]. L’indication
préférentielle de l’ionophorèse est l’hyperhidrose palmo-
plantaire. Les contre-indications sont la grossesse et le
port d’objets métalliques implantés (ostéosynthèse, pro-
thèse, stérilet). Les effets secondaires du traitement sont
minimes et le plus souvent locaux (prurit, eczéma, éry-
thème, sensation de « picotements d’aiguille »). Cepen-
dant, le traitement est long, astreignant et n’offre qu’une
amélioration symptomatique temporaire. L’apparition de
nouveaux dispositifs sans eau semble prometteuse, mais
n’est pas encore répandue [10].
Toxine botulique
La toxine botulique agit par blocage de la libération d’acé-
tylcholine au niveau des terminaisons nerveuses sympathi-
ques présynaptiques des glandes sudoripares, empêchant la
contraction des cellules myoépithéliales des glandes sudo-
rales, et donc leur vidange. La toxine botulique (Botox
®
)
305
STV, vol. 22, n°6, juin/aou
ˆt 2010
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 03/06/2017.

a reçu l’AMM dans les problèmes d’hypersudation exces-
sive des aisselles de l’adulte et de l’enfant de plus de 12 ans
entraînant un retentissement psychologique important.
Les injections doivent être renouvelées tous les 12 mois.
En pratique, le patient doit arrêter les traitements locaux
quatre jours avant la séance, et avoir rasé les aisselles.
Après une anesthésie de surface, on pratique un test de
Minor qui permet d’objectiver les zones à injecter, qui est
dessinée au crayon dermographique, puis quadrillée en
carrés de 2 cm de côté, où la toxine est injectée en intrader-
mique [3]. Une douleur locale importante est le plus fré-
quent des effets associés. Un autre effet indésirable est la
faiblesse passagère des muscles intrinsèques de la main.
Près de 90 % des patients répondent au traitement pour une
durée moyenne de sept mois, et un quart des patients béné-
ficient d’un effet supérieur ou égal à un an [11]. Une méta-
analyse ne retrouve pas d’effets secondaires systémiques ou
locaux majeurs [12]. La toxine botulique pourrait ainsi
remplacer progressivement les ionophorèses. Cependant,
la place de la toxine botulique vis-à-vis de la sympathec-
tomie chirurgicalereste à préciser[4].Une étude comparative
attribue à la toxine botulique de meilleurs résultats préco-
ces, mais de moins bons résultats tardifs qu’après chirurgie
[13]. De plus, certains ont rapporté que la toxine botulique
était plus efficace au niveau de la transpiration axillaire
plutôt que palmaire [14], si bien que jusqu’ici la Food and
Drug Administration (FDA) américaine et les autorités
françaises n’ont donné leur autorisation que pour cette
localisation.
Traitement chirurgical :
la sympathectomie thoracique endoscopique
L’avènement de la vidéochirurgie a bouleversé le traitement
des hyperhidroses sévères, résistantes au traitement
médical, et la sympathectomie endoscopique s’est
imposée comme la technique chirurgicale de référence.
Nous réalisons une sympathectomie tronculaire bilatérale,
en un temps, sous anesthésie générale avec intubation
sélective [15].
Intervention
Trois orifices de trocart sont nécessaires et disposés aux
trois sommets d’un triangle à base supérieure. L’optique
occupe le sommet inférieur de ce triangle (figure 2). Après
affaissement du poumon, l’opérateur repère la première
côte, incise la plèvre pariétale à proximité du nerf sympa-
thique, le dissèque puis le résèque sur l’étendue souhaitée
en fonction du type d’atteinte : une atteinte palmaire isolée
est traitée par une sympathectomie étendue de D2 à D3, une
atteinte axillaire isolée est traitée par une sympathectomie
de D3 à D4, et une atteinte palmaire et axillaire relève d’une
sympathectomie D2-D4. Le fragment de nerf est alors
réséqué et adressé pour examen anatomopathologique
définitif.
À la fin de l’intervention, le poumon exclu est reventilé et le
pneumothorax exsufflé avant de retirer les trocarts et de
fermer les incisions cutanées. Un drainage pleural conven-
tionnel est inutile, et la mise en place d’un drain aspiratif de
Redon est facultative. Le patient est ensuite installé en décu-
bitus controlatéral et la même intervention est réalisée du
côté opposé. Une radiographie de thorax doit être réalisée
en salle de réveil à la recherche d’un pneumothorax ou d’un
épanchement pleural. En l’absence d’anomalie, le drain de
Redon est retiré le soir de l’intervention, et le patient est
autorisé à quitter l’hôpital le lendemain.
Résultats
La sympathectomie par thoracoscopie est un traitement
efficace de l’hyperhidrose palmaire ou axillaire. Dans la
plupart des études, le taux de succès est compris entre 93
et 100 %, avec des taux de récidive de 0 à 13 % [16-18].
Parmi les séries importantes, Zacherl et al. ont publié
une étude rétrospective incluant 630 sympathectomies
ABC
Figure 2.A) instruments de thoracoscopie ; B) installation au bloc opératoire ; C) position des trocarts.
306 STV, vol. 22, n°6, juin/aou
ˆt 2010
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 03/06/2017.
 6
6
 7
7
 8
8
 9
9
1
/
9
100%









![I] En quoi la toxine botulique est-elle nuisible](http://s1.studylibfr.com/store/data/001631179_1-1c3d501992bf2c546eb864c01681654b-300x300.png)
