Les phosphatonines – des hormones du phosphate d`un type nouveau

Introduction
Le phosphate est essentiel àlastabilité desosdu
squelette, aumétabolisme énergétique de toutes
lescellules, à lasynthèse de l’ADN, etaux cas-
cadesde signalisationsintracellulaires.L’absorp-
tion alimentaire quotidienne de cetélément
s’élèveàenviron 1 gramme et une quantité équi-
valente est éliminée àson tour dansl’urine. L’ab-
sorption etl’élimination doivent satisfaireàune
balance exactecar un déficitou un excèsentraî-
nentdeseffets graves sur lesfonctionscellulaires
etorganiques.Une élimination trop faible de
phosphate parlesmaladesatteints d’insuffisance
rénale etd’insuffisancerénale chroniquetermi-
nale est un problème cliniquesérieux,dontles
conséquences serontl’hyperparathyroïdie secon-
daire,l’ostéomalacie parlibération de calcium et
de phosphate osseux,laprécipitation de phos-
phate etde calcium dansles tissus, accompagnée
de calcificationsetd’artériosclérose. L’artério-
sclérose en particulierélève le risque de morbidité
etde mortalitéchezlespatients souffrantd’insuf-
fisancerénale. Il n’est doncpasétonnantqu’un
grand nombre de facteurs influencentle métabo-
lisme,l’absorption etl’élimination duphosphate.
Le transport du phosphate
Cesontlesprotéinesde transport duphosphate
(NaPi,transport de phosphate inorganique[Pi]
couplé au sodium),qui induisentet règlentl’ab-
sorption digestive etl’élimination rénale de façon
déterminante. Ces transporteurs existent sous
plusieurs isoformes: NaPi-IIa etNaPi-IIc inter-
viennentprincipalementdansle rein (fig. 1 x ),
alors queNaPi-IIb secharge de l’absorption du
phosphate dansl’intestin grêle. L’expression et
l’activité de ces transporteurs sont régléesà court
etàlong terme,notammentparlaparathormone,
lavitamine D3(calcitriol),le phosphate lui-même,
etparcertainesphosphatoninesdécouvertesau
cours de cesdernièresannées.Lesphosphatoni-
nes sont une nouvelle classe d’hormonesquirè-
glent surtout le métabolisme phosphaté, alors
que laparathormone etle calcitriol règlenten
premierlieule métabolisme calcique.
Les phosphatonines
La présence d’une hormone spécifique duphos-
phate,laphosphatonine,ne fut longtempsque
postulée. La preuve de son existence etl’explica-
tion moléculaire en furentfinalementapportées
pardesexamensgénétiqueseffectués sur des
patients souffrantde divers déséquilibresdu
métabolisme duphosphate. On découvritl’exis-
tence de diversesphosphatoninesetil s’avéra
quecelles-ciconstituent une nouvelle classechi-
miquementinhomogène d’hormones.L’étude de
deux formesdifférentesd’hypophosphatémies,la
forme congénitale etlaforme acquise, a permis
d’identifier unréseau régulateur d’untype nou-
veau.Cette étude portaitd’une part sur des
patients atteints d’hypophosphatémie liée au
chromosome X(XLH) etd’hypophosphatémie
autosomique dominante et rachitisme (ADHR).
Cespatients souffrentdudiabète phosphaté, ca-
ractérisé par une fuiteurinaire massive de phos-
phate par voie rénale. Aumoyen de l’examen in-
direct(«linkage analysis»),laméthode génétique
apermisle clonage de deux gènes,le PHEX
(PHosphateregulating gene with homology toEn-
HigHligHts Forum Med Suisse 2008;8:8–10 8
Les phosphatonines – des hormones du phosphate
d’un type nouveau
Carsten A. Wagner, Heini Murer
Institut für Physiologie und Zürcher Zentrum für Integrative Humanphysiologie
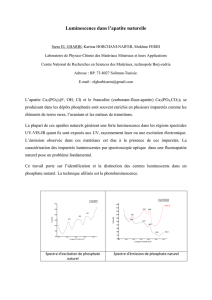
Figure 1
Réabsorption rénale de phosphate:
Le phosphate est librement filtré dans le rein, puis environ 80% de ce filtrat est réabsorbé le long
du tubule proximal par transport actif. Nous connaissons actuellement deux isoformes de transport
de phosphate permettant de réabsorber le phosphate en dépendance du sodium: NaPi-IIa et
NaPi-IIc. Ces transporteurs se différencient par le rapport entre le sodium et le phosphate transporté
et par les facteurs régulant le transport. Certaines mutations rares dans le gène codant pour
NaPi-IIc (SLC34A3) provoquent l’hypophosphatémie, l’hypercalciurie, le rachitisme et des calculs
rénaux chez les patients concernés. Les voies de transport du phosphate de la cellule vers le sang
ne sont pas encore connues. L’activité de la Na-K-ATPase dans la membrane basolatérale maintient
le sodium intracellulaire à un bas niveau, ce qui libère l’énergie nécessaire aux NaPi-IIa et NaPi-IIc.
8-10Wagner 303_f.qxp:Layout 121.12.2007 13:38UhrSeite8

dopeptidaseson the X chromosome) etle FGF-23
(Fibroblast GrowthFactor 23). Lespatients at-
teints d’hypophosphatémie autosomique domi-
nante etde rachitisme yprésentaient une muta-
tion particulière duFGF-23 aucours de laquelle
une séquencespécifique d’acidesaminés(motif
RXXR desacidesaminés176–179) fut détruite.
D’autre part,l’analyse quasisimultanée effectuée
sur despatients atteints d’unsyndrome para-
néoplastiquerare,l’ostéomalacie d’origine tu-
morale (TIO),permitde détecterànouveaudes
FGF-23.Onapudémontrerque les tumeurs
mésenchymateuses(parex. lesostéosarcomes)
produisentet sécrètentdesFGF-23 en grande
quantité, alors que lespatients souffrentde
symptômesidentiquesà ceux dudiabète phos-
phaté. On put encore identifierd’autresfacteurs,
produits dansle cadre de syndromesparanéo-
plastiquesd’origine tumorale,telsque lesFGF-7
(Fibroblast GrowthFactor 7),lesMEPE (Matrix
ExtracellularPhospho-glycoprotein),etles sFRP-4
(secreted Frizzled-Related Protein 4). Bien que
cesfacteurs comportentdespropriétéschimiques
trèsdifférentes,tous diminuentl’expression ré-
nale des transporteurs de phosphate etaugmen-
tentdonclaphosphaturie. Le faitquecesfacteurs
soientdes substancesisoléesàpartirde tumeurs
rend leur fonction physiologique peuclaire, ce qui
afaithésiter sur leur inclusion dansla classe des
phosphatonines.
FGF-23: un régulateur important
de l’homéostasie du phosphate
Lerôle physiologiquetrèsimportantjoué parles
FGF-23 aété élucidé aucours descinq dernières
années,principalementaumoyen de différents
modèlesde sourisquise distinguent tour àtour
par une déficience en FGF-23,une surexpression
en FGF-23,l’expression de mutationsde FGF-23
(en analogie aveclespatients souffrantdudiabète
phosphaté),ouparlasoumission àdes traite-
ments avecdiversesformesde FGF-23.L’ensem-
ble de cesétudesmontre que le FGF-23 est une
phosphatonine et un facteur régulateur impor-
tantdumétabolisme phosphaté. La synthèse du
FGF-23 se produitdansl’osetle contrôle en est
assuré par unsenseur de phosphate non encore
identifié. Lorsque laphosphatémie augmente,
lamise en circuitde FGF-23 augmente, ce qui
diminue l’expression rénale etintestinale des
transporteurs de phosphate (fig. 2x ). Il en ré-
sulteune réduction de l’absorption provenantde
l’alimentation et une augmentation de l’excré-
tion urinaire de phosphate (dansle rein,les trans-
porteurs de phosphate induisentlarésorption du
phosphate quiretourne ainsi de l’urine vers le
sang). Une diminution de laphosphatémie indui-
rait une augmentation compensatoire de lasyn-
thèse de vitamine D 3parl’enzyme rénal 1-alpha
hydroxylase,lavitamine D3stimulantalors la
résorption intestinale de phosphate etlafixation
de phosphate danslesos.Danscecas,le FGF-23
inhibe égalementl’activité de l’enzyme 1-alpha
hydroxylase etempêche ainsiune contre-régu-
lation. LeFGF-23 est lui-même contrôlé parla
vitamine D3activée etparlaphosphatémie. La
vitamine D3stimule lasynthèse duFGF-23 alors
qu’une chute duniveaude phosphatesérique
réduitlamise en circuitde FGF-23.Ainsi,grâce
aux FGF-23,un mécanisme de rétroaction em-
pêche une diminution dangereuse de laphos-
phatémie. Cesontdesprotéasesqui provoquent
ladégradation enzymatique desFGF-23 dans
le sang par unclivage d’une séquence détermi-
née d’acidesaminés.Cetteséquencesetrouve
être modifiée chezlespatients souffrantd’hypo-
phosphatémie autosomique dominante et rachi-
tisme. La mutation provoqueune résistance du
FGF-23 contre ladégradation etprolonge son
action biologique, ce qui produitles symptômes
de lamaladie. D’autre part, chezlespatients
souffrantd’hypophosphatémie liée auchromo-
some X, ladégradation de FGF-23 est ralentie
en raison d’une mutation concernantlaprotéine
PHEX, carcette protéine contribueauprocessus
de dégradation. Ceci explique qu’une mutation de
deux gènesdifférents provoque des symptômes
presque identiqueschezlespatients affectés.
Bien que lesmaladiesen question soient très
rares,ellesontnéanmoinsouvert une voie per-
mettantd’éluciderle mode de fonctionnementde
FGF-23.
HigHligHts Forum Med Suisse 2008;8:8–10 9
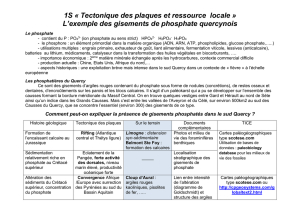
Figure 2
Régulation et fonction du FGF-23:
Le FGF-23 est produit dans l’os lorsque le niveau de phosphate sérique augmente. Le FGF-23
est activé au moyen d’une O-glycosylation par GALNT3 (UDP-N-acétyl-h-D-galactosamine, poly-
peptide N-acétyl-galactosaminyltransférase). Le FGF-23 diminue le taux de phosphate sérique
par la réduction de la quantité de transporteurs de phosphates rénaux (NaPi-IIa et NaPi-IIc), et
intestinaux (NaPi-IIb). De plus le FGF-23 réduit l’activité des 1hrénaux et inhibe ainsi l’activation
de la 1,25 dihydroxy-vitamine D3(calcitriol). Des taux plus élevés de vitamine D3stimulent égale-
ment la synthèse de FGF-23 et constituent ainsi un mécanisme de rétroaction négative. Le FGF-23
est inactivé par clivage grâce à une protéase (subtilisin-like proprotein convertase). Le rôle du gène
PHEX n’est pas encore clair, bien qu’il semble être essentiel dans le processus de dégradation
du FGF-23.
8-10Wagner 303_f.qxp:Layout 121.12.2007 13:38UhrSeite9

Klotho: ce que le vieillissement
et le phosphate ont en commun
Pour produireson effetou seseffets sur lescel-
lulescible etlesorganescible,le FGF-23, cette
hormone d’un nouveau type,doitdisposerd’un
récepteur spécifique. Bien qu’il existeuncertain
nombre de récepteurs de la classe des récepteurs
de fibroblast growth factor, aucun d’entre eux n’a
puêtreactivéin vitroparle FGF-23.Curieuse-
ment une sourisknock out pour Klotho manifesta
une forte hyperphosphatémie et une élévation
importante duniveauduFGF-23.Ces souris
knock outs’étaientparticulièrementillustrées
parleur vieillissementprécoce et rapide ainsi
que parle faitqu’ellesprésententde nombreux
symptômesdégénératifs typiquesduprocessus
de vieillissement.C’est pourquoi on adonné au
gène,respectivementàlaprotéine en question,
ce nom inspiré de celui de ladéesseClotho qui,
selon lamythologie grecque,tisse le fil dudestin.
Klotho est majoritairementproduitparles reins
et semble êtreuncofacteur essentiel pour le
FGF-23 sur le récepteur FGF-1. Pour le reste,on
connaît trèsmal jusqu’ici larelation entre la
régulation de Klotho etle métabolisme duphos-
phate. Cependant unrapport récentindique que
Klotho joueunrôle importantpour ce métabo-
lisme non seulementdanslasouris,maisaussi
chezl’être humain. Lespatients chezqui des
mutationsdansle gène Klotho sesontopéréeset
ontmené àune réduction partielle de l’activité,
présentent une forte hyperphosphatémie,pro-
duisentdescalcificationsectopiqueset souf-
frentd’une artériosclérose grave. Les recherches
futurespermettrontde vérifier siKlotho est
véritablement un «gène de lavieillesse», afin
d’en connaître le rapport aveclesmodifications
danslarégulation dumétabolisme duphosphate
oumême avecles«maladiesdu vieillissement»
comme l’artériosclérose.
Une ou plusieurs phosphatonines?
Tandisque lafonction physiologique duFGF-23
est bien établie, celle de quelquesautresfacteurs
phosphaturiquescomme les sFRP4,lesMEPE, ou
lesFGF-7,est encoreàpréciser.Pour l’instant
nous disposonsde peude donnéesindiquant si
cesfacteurs peuventjouent unrôle physiolo-
gique. L’existence d’autresfacteurs de régulation
duphosphate est toutefois trèsprobable. Cer-
tainesexpériencesin vivoeffectuées sur des rats
révèlentqu’unautre facteur est synthétisé dans
lamuqueuse de l’intestin grêle. L’absorption de
phosphate provenantde l’alimentation libèrece
facteur non encore identifié qui favorise l’élimi-
nation rénale de phosphatevialavoie sanguine.
Onaencore décritoupostulé desformes sem-
blablesd’interaction directe entre l’intestin et
les reinspour d’autrescomposants alimentaires
comme le sodium oule potassium. Cettevoie de
communication permettraitau rein de répondre
de façon adéquate et très rapide àun excèsde
phosphate dansl’organisme,sansque d’autres
systèmeshormonaux oud’autresmécanismes
de régulation agissant sur le long terme ne soient
impliqués.
On nomme collectivement«phosphatonines»
un groupe inhomogène d’hormonesetde fac-
teurs répondantàunconceptnouveauetqui
influencentet régulentle métabolisme duphos-
phate. Comparésaux hormonesclassiques
comme laparathormone oulavitamine D 3 ,les
phosphatonines sontdesfacteurs de régulation
quiagissentde manièrespécifiquesur ce méta-
bolisme. Elles semblentagiràplusieurs niveaux
(reins,intestin) etcontribuerdirectementà
l’adaptation etàla communication entre lesdi-
vers organes.Danscecontexte,le FGF-23 est une
hormone de l’osquisemble favoriseren premier
lieul’adaptation dumétabolisme duphosphate
aux besoinsdu sysstème squelettique. D’autres
facteurs semblentfavoriserla communication
entre l’intestin etle rein etéquilibrerle bilan de
l’ingestion etde l’élimination duphosphate. A cet
égard,lesphosphatoninesapparaissentcomme
deshormonesquicoordonnentlafonction de
divers organesdupointde vue dumétabolisme
duphosphate. En plus de l’importance de leur
rôle physiologique,lesphosphatonines repré-
sententde nouveaux objectifsintéressants pour
lapharmacothérapie de certainespathologiesde
l’équilibre duphosphatetellesque l’insuffisance
rénale avancée. Une autre piste passionnante
àsuivre est l’identification des«senseurs du
phosphate» régulantlaproduction desphospha-
tonines, ce qui permettraitde mesurerlocale-
mentla concentration de phosphate dansles
organesimpliquésdans son métabolisme.
HigHligHts Forum Med Suisse 2008;8:8–10 10
Références
–BerndtT, KumarR.Phosphatoninsand the regulation of
phosphate homeostasis.AnnuRevPhysiol. 2007;69:341–59.
.
–MurerH, Hernando N, ForsterI, BiberJ.Regulation of Na/Pi
transporterin the proximaltubule. AnnuRevPhysiol.
2003;65:531–42.
Correspondance:
Prof. Carsten A. Wagner
Institut für Physiologie und
Zürcher Zentrum für Integrative
Humanphysiologie
Winterthurerstrasse 190
CH-8057 Zürich
8-10Wagner 303_f.qxp:Layout 121.12.2007 13:38UhrSeite 10
1
/
3
100%