antibiotiques

M. Chomarat
ANTIBIOTIQUES
Dr Monique Chomarat
MCU-PH
Faculté de Médecine Lyon-Sud Charles
Mérieux

M. Chomarat
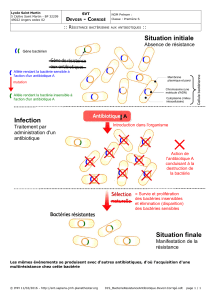
Les conditions de l’activité d’un antibiotique
sur une bactérie
- posséder une cible bactérienne spécifique
- demeurer sous forme active
- accéder à la cible
- interagir efficacement avec la cible, en l’inactivant
1 de ces conditions absentes : souche résistante

M. Chomarat
Résistance naturelle
•Absence de cible
–Mycoplasmes et β
ββ
β-lactamines
•Cible inaccessible
–Bactéries à Gram négatif et glycopeptides
•Inactivation de l’antibiotique
–
Klebsiella
et amoxicilline
•Cibles sans affinité
–Bactéries à Gram + et aztréonam
Cela définit le spectre d’activité d’un antibiotique : cf Vidal
avec liste des espèces sensibles et des espèces résistantes

M. Chomarat
Spectre d’activité d’un antibiotique
Exemple pour l’amoxicilline : extrait du Vidal 2009
SPECTRE
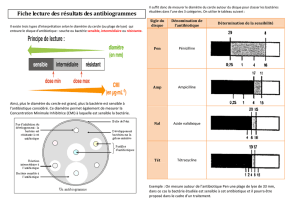
• Les concentrations critiques séparent les souches sensibles des souches de sensibilité intermédiaire et ces dernières, des résistantes :
S <= 4 mg/l et R > 16 mg/l ; CMI pneumocoque : S <= 0,5 mg/l et R > 2 mg/l (à titre provisoire).
La prévalence de la résistance acquise peut varier en fonction de la géographie et du temps pour certaines espèces. Il est donc utile de
disposer d'informations sur la prévalence de la résistance locale, surtout pour le traitement d'infections sévères. Ces données ne peuvent
apporter qu'une orientation sur les probabilités de la sensibilité d'une souche bactérienne à cet antibiotique.
Lorsque la variabilité de la prévalence de la résistance en France est connue pour une espèce bactérienne, la fréquence de résistance
acquise en France (> 10 % ; valeurs extrêmes) est indiquée entre parenthèses.
--- Espèces sensibles :
- Aérobies à Gram + : Corynebacterium diphtheriae, Enterococcus faecalis, Erysipelothrix rhusiopathiae, Listeria monocytogenes,
Nocardia asteroides (50 - 80 %), streptococcus, Streptococcus bovis, Streptococcus pneumoniae (15 - 35 %).
- Aérobies à Gram - : Actinobacillus actinomycetemcomitans, Bordetella pertussis, capnocytophaga, eikenella, Escherichia coli (30 - 50
%), Haemophilus influenzae (20 - 35 %), Haemophilus para-influenzae (10 - 20 %), Helicobacter pylori, Neisseria gonorrhoeae, Neisseria
meningitidis, Pasteurella multocida, Proteus mirabilis (10 - 40 %), salmonella (0 - 40 %), shigella (0 - 30 %), Streptobacillus moniliformis,
Vibrio cholerae.
- Anaérobies : actinomyces, clostridium, eubacterium, fusobacterium, peptostreptococcus, porphyromonas, prevotella (60 - 70 %),
Propionibacterium acnes, veillonella.
- Autres : bartonella, borrelia, leptospira, treponema.
--- Espèces modérément sensibles (in vitro de sensibilité intermédiaire) :
- Aérobies à Gram + : Enterococcus faecium (40 - 80 %).
--- Espèces résistantes :
- Aérobies à Gram + : staphylococcus.
- Aérobies à Gram - : acinetobacter, alcaligenes, Branhamella catarrhalis, campylobacter, Citrobacter freundii, Citrobacter koseri,
enterobacter, Klebsiella oxytoca, Klebsiella pneumoniae, legionella, Morganella morganii, Proteus rettgeri, Proteus vulgaris, providencia,
pseudomonas, serratia, Yersinia enterocolitica.
- Anaérobies : Bacteroides fragilis.
- Autres : chlamydia, mycobacterium, mycoplasma, rickettsia.

M. Chomarat
Résistance acquise
•Certaines souches d’une espèce normalement
sensibles à un antibiotique sont devenues
résistantes à cet antibiotique :
–Cible de l’antibiotique est devenue inaccessible
–Cible de l’antibiotique a disparu
–L’antibiotique n’est plus actif
Cette résistance ne peut être mise en évidence que par des
tests au laboratoire : CMI ou antibiogramme
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
1
/
52
100%