TS-Évaluation n°10 (bac blanc)

TS www.pichegru.net 1
er
mars 2017
- 1 -
Bac Blanc - 3h30
Consignes pour la rédaction
• Noter le numéro complet de la question très lisiblement (encadré ou en couleur)
• Pour les questions dont la réponse se fait sur l’annexe, noter le numéro de la question sur la copie puis noter « Voir annexe »
• Le numéro de l’exercice est à noter ou à souligner en couleur.
Le non respect de ces règles entraînera une pénalité de -0,5 pt par manquement.
.1 La mission Mars Science Laboratory
Le lancement du robot Curiosity de la mission Mars Science Laboratory
(MSL) a eu lieu le samedi 26 novembre 2011. Il s’est posé sur le sol
martien le 6 août 2012. Ce robot transporte du matériel scientifique
destiné à l’analyse de la composition du sol et de l’atmosphère
martienne.
Le but de cet exercice est d’évaluer les conditions à respecter sur les
positions relatives de la Terre et de Mars lors du lancement du robot
Curiosity.
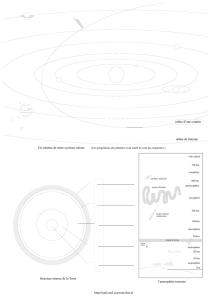
Document 1 : Orbite de Hohmann
Dès les années 1920, Walter Hohmann étudie la manière la plus
économique en énergie pour se rendre d’une planète à une autre.
Pour un voyage interplanétaire entre la Terre et Mars, la trajectoire du
vaisseau est une ellipse de centre O (voir schéma ci-dessous). On appelle
cette ellipse, de demi grand axe a, l’orbite de Hohmann. Le périhélie P
(point le plus proche du Soleil) est sur l'orbite de la Terre et l'aphélie A
(point le plus éloigné du Soleil) sur celle de Mars. Pour simplifier, les
orbites de Mars et de la Terre autour du Soleil sont considérées comme
circulaires et contenues dans le même plan.
Pour que ce voyage interplanétaire soit réussi, il faut d’abord que le
vaisseau échappe à l’attraction de la Terre, puis qu’il utilise l’attraction
du Soleil pour rejoindre le voisinage de Mars en empruntant une orbite
de transfert, dite orbite de Hohmann. Dans l’étape finale c’est
l’interaction gravitationnelle avec Mars qui doit être prépondérante pour
que Curiosity puisse se poser sur son sol.
Orbite de Hohmann
Document 2 : Conditions de rencontre entre Curiosity et Mars
La figure ci-dessous donne les positions de la Terre et de Mars au
moment du départ et de l’arrivée de Curiosity.
Mars accomplit une orbite complète de 360° en 1,88 an.
On suppose que les deux planètes décrivent un mouvement circulaire et
uniforme pendant le temps du voyage. On lance le vaisseau de la Terre
lorsque Mars se trouve au point M1 sur son orbite, position initiale
repérée par l’angle
α
représenté ci-dessous. Le point M2 représente le
lieu de rendez-vous entre le vaisseau et Mars.
On note
β
l’angle (SM1, SM2)
Données :
• Distance Soleil-Terre : R
1
= 1,50×10
8
km ;
• Distance Soleil-Mars : R
2
= 2,28×10
8
km ;
• Période de révolution de Mars autour du Soleil : 1,88 an ;
• Constante de gravitation universelle : G = 6,67×10
-11
m
3
·kg
-1
·s
-2
;
• Masse du Soleil M
S
= 1,99×10
30
kg.
1. Indiquer les différentes phases du voyage de la mission MSL.
2. Sur le schéma du document 1, repasser en couleur le chemin suivi
par MSL et indiquer les distances R
1
et R
2
introduites dans les données.
Montrer que la valeur du demi-grand-axe de l’orbite de Hohmann est a =
1,89×10
8
km.
La troisième loi de Kepler permet d’écrire
S
2
3
2
π4
MG
a
T⋅
=où a est le
demi grand axe de l’ellipse, T la période pour parcourir la totalité de
l’ellipse, G la constante de gravitation universelle et M
S
la masse du
Soleil.
3.1.
Exprimer la durée
∆
t du voyage de Curiosity en fonction de a, G et
M
S
et vérifier l’homogénéité de cette relation par une analyse
dimensionnelle.
3.2.
Calculer la durée
∆
t. Commenter le résultat obtenu par rapport à la
durée de la mission.
4.
Déterminer la valeur de l’angle
α
qui repère la position de Mars au
départ, condition nécessaire à la réussite de la mission.
Le candidat est invité à noter ses pistes de recherche. La démarche
suivie est évaluée et nécessite d’être correctement présentée.
orbite de Hohmann
T1, Terre au
départ
S
α
M1, Mars au
départ
M2, Mars à
l’arrivée
T2, Terre à
l’arrivée
β
orbite de la Terre
orbite de Mars
orbite de Hohmann
A P
Soleil
O
a

TS www.pichegru.net 1
er
mars 2017
- 2 -
.2 Atterrissage de Curiosity sur Mars
Arrivé sur Mars le 6 août 2012, Curiosity, robot mobile (rover) de la
NASA n’a pour le moment pas révolutionné notre connaissance de cette
planète. Pourtant, l’agence spatiale américaine considère déjà la mission
comme un immense succès. Pourquoi ? Parce qu’elle a réussi à faire
atterrir sans encombre le plus gros rover de l’histoire de l’exploration
martienne : longueur = 3 m ; largeur = 2,7 m ; hauteur = 2,2 m ; masse =
900 kg. Et qu’elle a ainsi démontré l'efficacité d’une nouvelle technique
d’atterrissage automatique extraterrestre. Cette technique audacieuse a
mis en œuvre une « grue volante » pour déposer tout en douceur le robot
au bout de trois filins. […]
Faire atterrir une sonde sur Mars est un exercice périlleux, comme l’ont
prouvé les échecs de plusieurs missions. La dernière en date fût Beagle
2, qui s’est écrasée au sol en 2003.
La principale difficulté vient du fait que l’atmosphère martienne est très
ténue : moins de 1 % de la pression de l’atmosphère terrestre. Résultat,
l’utilisation d’un bouclier thermique, qui tire parti de la friction sur les
couches atmosphériques, puis d’un parachute de très grande taille,
comme on le fait pour le retour d’engins sur Terre, ne suffit pas pour
freiner l’engin. Il faut faire appel à un autre dispositif pour le ralentir
encore un peu plus et le poser sans danger. [...]
Dans la tête des ingénieurs de la
NASA a émergé alors une
[nouvelle] idée. Elle était
inspirée par les hélicoptères de
l’armée américaine baptisés
« grue volante », capables de
transporter et de déposer au sol
des charges de plusieurs tonnes
à l’extrémité d’un filin. Dans la
version spatiale de cette grue
volante, c’est un étage de
descente propulsé par huit
rétrofusées qui joue le rôle de
l’hélicoptère.
Les 3 parties de cet exercice sont indépendantes.
Données :
• Célérité de la lumière dans le vide : c = 3,0·10
8
m·s
-1
• Champ de pesanteur au voisinage de la surface de Mars : g = 3,7 m·s
-2
• Dans un champ de pesanteur uniforme, l’équation de la trajectoire d’un
mouvement de chute libre avec vitesse et altitude initiales s’écrit :
Hx
V
xg
xz +⋅+
⋅⋅ ⋅
−=
α
α
tan
cos2
)(
22
0
2
Document 1 : Principales étapes de l'atterrissage de Curiosity
sur Mars
Après sa descente sous un parachute, la capsule allume son radar pour
contrôler sa vitesse et son altitude (1). À 2 kilomètres d’altitude et à une
vitesse de 100 mètres par seconde, l’étage de descente, auquel est
rattaché le rover, se sépare de la capsule (2) et allume ses 8 moteurs
fusées (3) pour ralentir jusqu’à faire du « quasi-surplace » (4). À 20
mètres du sol, l’étage de descente a une vitesse de 75 centimètres par
seconde seulement, il commence alors à descendre le robot au bout de
trois filins de 7,50 mètres (5). L’engin dépose Curiosity en douceur (6).
Les filins sont coupés, ainsi que le « cordon ombilical » qui permettait à
l’ordinateur de bord du rover de contrôler la manœuvre (7). L’étage de
descente augmente alors la poussée de ses moteurs pour aller s’écraser à
150 mètres du lieu d’atterrissage (8).
D’après La recherche n°471- Janvier 2013
α
0
V
r
z
H
x
O
1
2
4
4
5
6
-
7
8
3

TS www.pichegru.net 1
er
mars 2017
- 3 -
1. La descente autopropulsée
Figure 1
On admet que la masse m de l’étage de descente (rover compris) reste à
peu près constante lors de la descente et vaut environ 2,0·10
3
kg, et que
le champ de pesanteur martien est uniforme durant cette phase.
1.1.
Établir l’expression du travail du poids de l’étage de descente, lors
de son déplacement du point A au point B définis sur la figure 1, en
fonction de m, g, AB et de l’angle ); ( ABP noté
θ
.
1.2.
En s’appuyant sur un schéma, établir l’expression du travail du
poids en fonction notamment des altitudes z
A
et z
B
, respectivement du
point A et du point B.
1.3.
Déterminer la valeur du travail du poids entre A et B et commenter
son signe.
Évolution de l’énergie mécanique de l’étage de descente.
1.4.1.
Déterminer la valeur de l’énergie mécanique E
m
de l’étage de
descente au point A et au point B.
1.4.2.
L’énergie mécanique de l’étage de descente évolue-t-elle au cours
du mouvement entre les points A et B ? Interpréter qualitativement ce
résultat.
2. Les secondes les plus longues de la mission.
2.
À partir des données du document 1 et en faisant différentes
hypothèses, estimer la durée
∆
t de la phase de descente du robot entre le
moment où la grue commence à le descendre et son atterrissage sur le
sol martien.
Toute initiative prise pour résoudre cette question, ainsi que la qualité de
la rédaction explicitant la démarche suivie seront valorisées.
3. Dégagement autopropulsé de l’étage de descente
désolidarisé du rover
Une fois le rover déposé, la poussée des moteurs augmente et propulse
verticalement l’étage de descente jusqu’à une altitude de 50 m au-dessus
du sol martien. L’étage s’incline alors d’un angle de 45° par rapport à
l’horizontal et les moteurs se coupent.
3.1.
À partir du moment où les moteurs se coupent, l’étage de descente a
un mouvement de chute libre. Justifier.
3.2.
À l’aide des informations données sur l’équation de la trajectoire
d’un mouvement de chute libre, déterminer la valeur de la vitesse initiale
V
0
minimale permettant d’écarter l’étage de descente d’au moins 150 m
du lieu d’atterrissage du rover.
.3 Teneur en cuivre d’une pièce de 5 centimes
La pièce de 5 centimes d’euro est composée d’un
centre en acier (constitué essentiellement de fer et de
carbone) entouré de cuivre. Elle a un diamètre de
21,25 mm, une épaisseur de 1,67 mm et une masse
de 3,93 g.
On cherche par une méthode spectro-photométrique
à déterminer la teneur en cuivre d’une telle pièce.
Le cuivre, de masse molaire 63,5 g·mol
-1
, est un métal qui peut être
totalement oxydé en ions cuivre (II) par un oxydant puissant tel que
l’acide nitrique selon la réaction d’équation :
3 Cu
(s)
+ 8 H
+(aq)
+ 2 NO
3–(aq)
→ 3 Cu
2+(aq)
+ 4 H
2
O
(ℓ)
+ 2 NO
(g)
Les ions cuivre (II) formés se retrouvent intégralement dissous en
solution ; le monoxyde d’azote NO est un gaz peu soluble.
En pratique, on dépose une pièce de 5 centimes dans un erlenmeyer de
100 mL, on place cet erlenmeyer sous la hotte et on met en
fonctionnement la ventilation.
Équipé de gants et de lunettes de protection, on verse dans l’erlenmeyer
20 mL d’une solution d’acide nitrique d’une concentration environ égale
à 7 mol·L
-1
.
La pièce est alors assez vite oxydée et on obtient une solution notée S
1
.
On transfère intégralement cette solution S
1
dans une fiole jaugée de 100
mL et on complète cette dernière avec de l’eau distillée jusqu’au trait de
jauge. On obtient une solution S
2
qui contient également des ions fer
(III) provenant de la réaction entre l’acide nitrique et le fer contenu dans
le centre d’acier de la pièce.
L’absorbance de la solution S
2
à 800 nm est mesurée, elle vaut 0,575.
1. Étalonnage
1.1.
Déterminer, en argumentant votre réponse, les couleurs attendues
pour une solution d’ions cuivre (II) et pour une solution d’ions fer (III).
Pour quelle raison choisit-on de travailler à une longueur d’onde de 800
nm ?
1.2.
On fait subir à différents échantillons de métal cuivre pur le même
traitement que celui décrit ci-dessus pour la pièce. On obtient alors des
solutions d’ions cuivre (II) dont on mesure l’absorbance à 800 nm.
Montrer, en utilisant le document 2 et en utilisant une feuille de papier
millimétré à rendre avec la copie, que la loi de Beer-Lambert est vérifiée
pour ces solutions d’ions cuivre (II).
2. Détermination de la teneur en cuivre dans la pièce.
2.1.
Déterminer la masse de cuivre contenue dans la pièce de 5 centimes
d’euro.
2.2.
En déduire la teneur (ou « pourcentage massique ») en cuivre dans
la pièce.
3. Incertitude.
10 groupes d’élèves ont déterminé expérimentalement la masse de
cuivre présente dans 10 pièces de 5 centimes de même masse. Leurs
résultats sont les suivants :
Groupe 1 2 3 4 5 6 7 8 9 10
Masse de
cuivre (mg) 260
270
265
263
264
265
262
261
269
267
3.1.
Déterminer, grâce aux valeurs trouvées par les élèves, l’incertitude
élargie (pour un niveau de confiance de 95 %) sur la mesure de la masse
de cuivre dans une pièce.
3.2.
En déduire l’intervalle dans lequel devrait se situer le résultat du
mesurage de la masse de cuivre avec un niveau de confiance de 95 %.
Document 1 : Spectres d’absorption des ions cuivre (II) et fer
(III) dans l’eau.
On donne ci-dessous les spectres d’absorption d’une solution d’ions
cuivre (II) et d’une solution d’ions fer (III), ainsi qu’un tableau reliant
longueur d’onde d’absorption et couleur complémentaire. Le « blanc » a
été fait avec de l’eau pure.
altitude z
sol de Mars
Début de la descente
autopropulsée (rover compris)
Symbolisation de
l’onde émise par le
radar
Rétrofusé
e
Début de la descente
du robot

TS www.pichegru.net 1
er
mars 2017
- 4 -
Solution aqueuse d’ions cuivre (II) Cu
2+
de concentration 7,5·10
-2
mol·L
-1
.
Solution aqueuse d’ions fer (III) Fe
3+
de concentration 5,0·10
-2
mol·L
-1
Couleur absrobée Longueur d’onde
d’absorption
Couleur
complétentaire
violet 400-424 jaune-vert
bleu 424-491 jaune
vert 491-575 pourpre
jaune 575-585 bleu
orange 585-647 vert-bleu
rouge 647-850 bleu-vert
Document 2 : Courbe d’étalonnage
Tableau donnant l’absorbance A à 800 nm de solutions aqueuses
contenant des ions cuivre (II), obtenues à partir de divers échantillons de
métal cuivre pur :
Masse de l’échantillon
de cuivre (mg)
Concentration
mol·L
-1
Absrobance
0 0 0
25,1 3,95·10
-3
0,055
50,6 7,97·10
-3
0,121
103,8 1,63·10
-2
0,231
206,2 3,25·10
-2
0,452
300,6 4,74·10
-2
0,649
Document 3 : Incertitude sur un mesurage
On rappelle les différentes formules intervenant dans la détermination de
l‘incertitude sur le résultat du mesurage d’un ensemble de n valeurs {x
1
,
x
2
… x
n
} :
Écart-type : 1
)(
1
2
1
−
−
=
∑
=
−
n
xx
n
i
i
n
σ
Incertitude-type sur la moyenne :
n
xu
n1
)(
−
=
σ
Intertitude élargie sur la moyenne : )(xU = )(xuk ⋅, avec :
• k = 1 pour un niveau de confiance de 68% ;
• k = 2 pour un niveau de confiance de 95% ;
• k = 3 pour un niveau de confiance de 98% ;
Correction
Ex.1
1.
Décoller de la Terre, puis utiliser l’attraction du soleil pour rejoindre
le voisinage de Mars sur l’orbite de Hohmann. Puis s’approcher de mars
et se poser.
[0,5 pt]
2.
Chemin suivi par MSL
Le grand axe AP est composé des deux rayons R
1
et R
2
. Donc le demi
grand axe vaut (R
1
+ R
2
)/2 = 1,89·10
8
km.
[1 pt]
+1 pour trajectoire
+1 pour R
1
et R
2
3.1.
La durée du voyage correspond à une demi période d’un objet sur
cette orbite elliptique.
S
32
π
4
MG
a
T⋅⋅
=donc ∆t = T/2 =
S
32
π
MG
a
⋅⋅
[1 pt]
+1 pour l’idée que ∆t = T/2
+1 pour expression de T correcte
s
s
1
kgskgm
mπ
2213
3
S
32
==
×⋅⋅
=
⋅⋅
−−−
MG
a. L’expression de ∆t est
bien homogène a des secondes.
[0,5 pt]
3.2.
T = 4,48·10
7
s. donc le voyage vaut la moité de cette durée : soit
environ 8,64 mois. La durée donnée dans l’énoncée est de 8 mois et 10
jours. Ces résultats sont donc tout à fait compatibles entre eux.
[1 pt]
+1 pour durée de l’énoncé donnée.
+1 pour calcul correct de T
4.
Cette question revient à savoir où se trouve mars 8,5 mois avant sa
position M2.
Une demi année martienne avant l’atterrisage de MSL sur Mars, soit
11,3 mois avant,
β
vaudra 180°.
Que vaut
β
8,5 mois avant l’atterissage de MSL ?
β
= 180×8,5/11,3 =
135°.
α
vaudra donc 180-135 = 45 °.
[1 pt]
orbite de la Terre
orbite de Mars
orbite de Hohmann
A P
Soleil
O
a
R
1
R
2
580
480
380
absorbance
2,0
0,5
680
longueur d’onde (nm)
3,0
0
3,5
530
430
630
780
730
830
2,5
1,5
1,0
580
480
380
absorbance
0,6
0,4
0,2
680
longueur d’onde (nm)
0,8
0
1,0
530
430
630
780
730
830

TS www.pichegru.net 1
er
mars 2017
- 5 -
Ex.2
1.1.
θ
cosABAB)(
AB
⋅⋅⋅=⋅= gmPPW
r
r
[0,5 pt]
-3 si AB·cos
θ
devient (z
A
– z
B
)· cos
θ
-2 si expression finale donnée directement
1.2.
On voit sur ce schéma que
BA
)AB;cos(AB zzP −=⋅
r
Donc )()(
BAAB
zzgmPW −⋅⋅=
r
[0,5 pt]
-2 si z
B
– z
A
1.3.
D’après le document 1, A se trouve à 2 km d’altitude, B se trouve à
20 m et g vaut 3,7 m·s
-2
, donc :
=⋅××⋅=−⋅⋅=
33
BAAB
1098,17,3102)()( zzgmPW
r
15 MJ.
Cette valeur est positive car le poids a un travail moteur.
[0,75 pt]
-1 si justification fausse d’un travail du poid résistant
1.4.1.
E
m
(A) = m·g·z
A
+ 0,5·m·v
A2
= 2·10
3
×3,7×2·10
3
+ 0,5×2·10
3
×100
2
= 25 MJ.
E
m
(B) = 0,15 MJ car z
B
= 20 m et v
B
≅ 0.
[0,5 pt]
D si formule E
m
= E
c
+ E
pp
Raisonnement et calcul correct, mais mauvaise exploitation des
données : -2
1.4.2.
L’énergie mécanique diminue au cours de la descente car l’étage
de descente n’est pas soumis qu’à son seul poids : la force de poussée
des rétrofusées n’est pas une force conservative.
[0,5 pt]
-3 si justification fausse ou absente
2.
L’étage de descente a une vitesse de 0,75 m·s
-1
. Au moment où il
commence à descendre le robot grâce à ses filins, il se trouve à 20 m du
sol. Au moment où le robot touche le sol, l’étage de descente se trouve à
7,5 m du sol (on suppose que les filins ont été déroulés de toute leur
longueur). La durée de cette phase de la descente, si la vitesse de l’étage
de descente est constante et verticale, sera de ∆t = d / v = 12,5/0,75 ≅ 17
s.
[1,5 pt]
D si ∆t = 20/0,75
B si aucune hypothèse explicitée
3.1.
Plus de poussée des rétrofusées et peu de frottement (vu que la
vitesse de l’étage est modeste et l’atmosphère de Mars très ténue).
L’étage de descente n’est donc soumis qu’à son poids, ce qui est la
définition d’une chute libre.
[0,25 pt]
3.2.
On veut que z(x) = 0 pour x = 150 m. D’après l’énoncé, H = 50 m et
α
= 45°.
On isole V
0
: )tan(cos2
2
2
0
Hxz
xg
V−⋅−⋅⋅ ⋅−
=
αα
AN : =
−⋅−⋅⋅ ×−
=)5045tan1500(45cos2
1507,3
2
2
0
V20 m·s
-1
[1,5 pt]
D si seulement z (150) = 0
-1 par erreur de valeur ou erreur d’étourderie de calcul.
-3 si grosse erreur de calcul, mais données OK
Ex.3
1.1.
Les ions cuivre II absorbent dans le rouge. Ils seront donc bleu-vert.
Les ions fer III absorbent dans le violet. Ils seront donc jaune-vert.
On travaille à 800 nm car cette longueur d’onde correspond au
maximum d’absorption de l’ion cuivre II. De plus, les ions fer III
n’absorbent pas à cette longueur d’onde.
[0,75 pt]
D si seulement justification des 800 nm
1.2.
Absorbance des solutions en fonction de la concentration en Cu
2+
0
0,05
0,1
0,15
0,2
0,25
0,3
0,35
0,4
0,45
0,5
0,55
0,6
0,65
0,7
0 0,5 1 1,5 2 2,5 3 3,5 4 4,5 5
c ( ×10
-2
mol·L
-1
)
A
On voit que A est proportionnel à c (fonction linéaire). La loi de Beer-
Lamber A = k·c est donc vérifiée.
[1 pt]
C si seulement graphique, y compris A = f (m)
2.1.
C vaut environ 0,043 mol·L
-1
La quantité d’ions cuivre II est : n(Cu
2+
) = C·V = 0,0415×0,1 = 4,15
mmol. Soit une masse m = 264 mg.
[1,75 pt]
B si précision insuffisante
B si calcul de C à partir d’un unique autre point
2.2.
Teneur en cuivre : 0,26/3,93 = 0,066 soit 6,6 %.
[0,5 pt]
3.1.
Faire les calculs en utilisant les fonctions statistiques de la
calculatrice.
Moyenne : 264,6
Écart-type : 3,306559138
Incertitude-type : 1,045625809
Incertitude élargie (95 %) : 2,091251619
[0,5 pt]
3.2.
m = 265 ± 2 mg
[0,5 pt]
A
B
z
A
z
B
AB;P
r
AB·cos (
AB;P
r
)
1
/
5
100%