I - Le système immunitaire

Par Krys3000 (Groupe « The Trust » - http://www.cours-en-ligne.tk/) Page 1
IMMUNOLOGIE
CHAPITRE I : LE SYSTÈME IMMUNITAIRE
Le corps possède un système immunitaire, qui s’illustre par le fait qu’on puisse attraper une maladie, qu’on ne rattrape jamais
ensuite. Il y a donc quelque chose, dans la première infection, qui permet au corps de se souvenir, et de répondre au mieux à
une seconde infection. L’existence de ce système s’est vue à de multiples occasions au cours du temps, notamment lorsque des
épidémies de grippes ne frappaient pas les personnes ayant déjà vécu une autre épidémie de grippe dans leur vie.
On définit comme étant la Dose Létale 50 (DL
50
) la quantité de pathogène (mesurée en ufp, « unité formant plage ») pour
laquelle 50 % des animaux infectés meurent. Les animaux survivants, si on les réinfecte, réagissent bien mieux et survivent alors
à plus de 90 %.
I – L’INVASION
Le système protège contre 4 classes de pathogènes :
• Bactéries/parasites/champignons intracellulaires
• Bactéries/parasites extracellulaires
• Virus
• Vers Parasites
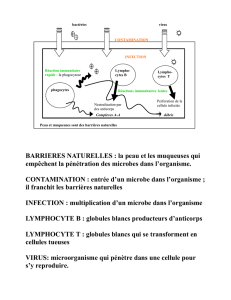
Le pathogène va pouvoir entrer de plusieurs façon dans l’organisme, mais à chaque fois, il devra franchir des barrières – nos
cellules sont jointives et bloquent, quelque soit le système considéré (Peau, Œil, Poumon, Intestin). En plus de cette barrière
physique, les mouvements de mucus (évacuant les pathogènes) et la compétition par la flore normale devraient empêcher toute
invasion. Alors comment les pathogènes entrent ? Ils profitent d’une brèche dans la sécurité qui se fait par exemple par blessure
cutanée.
II – IMMUNITÉ INNÉE
Une écharde perce la peau : les pathogènes entrent et débarquent dans les muqueuses sous-cutanées. Il existe une première
classe de cellules, résidentes de l’endroit, qui vont intervenir : les macrophages, qui expriment la molécule CD11b à leur surface.
Ces cellules sont capables de phagocyter les bactéries, dans l’objectif de les tuer (par acidification ou toxification). Cette attaque
déclenche, au sein du macrophage, la production de deux classes de molécules : les cytokines et les chimiokines.
Les chimiokines vont attirer sur place deux nouveaux types cellulaires, qui vont arriver par extravasation (par voie sanguine,
donc dilatation des vaisseaux, puis écartement des cellules, entrainant rougeur et douleur : c’est l’inflammation)
1. Les neutrophiles qui sont également des phagocyteurs, à la différence qu’ils sont « jetables » et meurent
immédiatement après avoir tué – c’est ce qui est responsable de la formation du pus, amoncellement de neutrophiles
morts. Ces cellules constituent 60 à 70 % des cellules blanches et ont des noyaux lobés. Ils expriment la protéine Gr1 à
leur surface.
2. Les monocytes dont le rôle est de multiplier le nombre de macrophages en se différenciant, et donc de renforcer la
défense. Ces cellules sont bien plus grosses, constituent 3 à 10 % des cellules blanches, et ont un noyau ovale. Comme
elles se différencient en macrophages, elles expriment aussi CD11b.
Cet ensemble de réactions faisant intervenir trois types cellulaires est nommé « immunité innée ». C’est le mécanisme de base,
pour les faibles blessures.
III – IMMUNITÉ ADAPTATIVE
Si l’infection est trop forte, on aura recours à un nouveau type cellulaire, qui est également résident : ce sont les cellules
dendritiques qui sont activés par les cytokines. Ces cellules, qui dérivent des monocytes du sang, peuvent phagocyter des
bactéries durant un court instant. Elles les capturent, et se mettent à synthétiser à la surface des Complexes Majeurs

Par Krys3000 (Groupe « The Trust » - http://www.cours-en-ligne.tk/) Page 2
d’Histocompatibilité (CMH) de classe II, qui sont des « présentoirs à peptides » de la bactérie pathogène phagocytée. Elles
présentent aussi diverses molécules à leur surface comme CD11c.
Cette opération effectuée, la cellule dendritique migre en direction des ganglions lymphatiques, quartier général d’un nouveau
type cellulaire nommé lymphocyte. Les lymphocytes qui sont dedans sont naïfs (n’ont jamais rencontré d’infection) et circulent
entre les différents ganglions. Au sein des ganglions, il y a plusieurs types de lymphocytes :
- Les lymphocytes T de type CD4 possèdent un récepteur nommé TCR (constitué de deux chaines parallèles de taille
identique, une α et une β. Chaque chaine est divisée en deux domaines, un variable et un constant. Il existe
évidemment une région transmembranaire pour l’ancrage et une courte queue cytoplasmique) permettant de
reconnaitre le CMH. Ils « scannent » donc chaque cellule dendritique jusqu’à reconnaitre le bon système. Le contact
entre les cellules dendritiques et le LT active celui-ci (par l’action d’une protéine, par exemple la B7) – le lymphocyte
quitte l’état naïf pour devenir effecteur, produisant alors les Interleukines-2, une cytokine de type proliférative, qui va
autoexciter (système autocrine) les lymphocytes et faire en sorte qu’ils se multiplient. On obtient alors plusieurs types
de CD4, qui, tous, peuvent alors remplir leur fonction d’activation des lymphocytes B (qui siègent dans une autre région
du ganglion). Toutefois, cela ne se fait pas de la même façon selon le type précis de lymphocyte et c’est surtout le type
TH2 qui va activer. Ceci fait, les lymphocytes CD4 délocalisent enfin en direction du site de blessure, ou ils pourront,
selon leur type, secréter des substances. On retrouve ainsi :
o Les TH1 qui produisent notamment de l’Interferon-γ, un « boosteur » pour les macrophages, qui renforce sa
capacité à tuer le pathogène. Pour transmettre ce boost, le TH doit se lier au macrophage, qui exprime
également un CMH pour cela.
o Les TH2 qui produit plusieurs substances dont l’Interleukine 4, 5, et 13.
o Les TH17
o Les Treg
- Les lymphocytes T de type CD8 ou Lymphocyte T Cytotoxique (CTL) qui sont généralement activés par les cellules
dendritiques, soit en même temps et de la même façon que les CD4, soit, si la cellule n’est pas capable de faire ça
directement, elle doit d’abord activer un CD4 avant de pouvoir activer un CD8. Ces cellules peuvent tuer les cellules qui
sont déjà infectées, en se fixant sur celles-ci et en induisant une mort cellulaire par apoptose.
- Les lymphocytes B, une fois activés par les T CD4, deviennent des plasmocytes et se déplacent dans la moelle osseuse,
débitant des anticorps à toute allure. Contrairement aux lymphocytes T qui ne reconnaissent que le CMH + Peptide, le
lymphocyte B reconnait toutes les structures protéiques avec ses récepteurs membranaires, le BCR, qui n’est en fait
qu’une version « transmembranaire » des anticorps qui vont être secretés.
Cette immunité est ultra-spécifique. Tout les lymphocytes T et B ont des spécificités différentes et reconnaissent des types
cellulaires différents pour permettre de couper court au plus grand nombre de maladies. Afin d’éviter toutefois que les
lymphocytes se mettent à attaquer les types cellulaires du corps humain, il y a des mécanismes de sauvegardes qui peuvent
neutraliser ou éliminer les lymphocytes en question – l’absence ou la déficience de ces mécanismes, au sein de maladies dites
alors auto-immunes, provoquent des problèmes d’attaque du corps contre lui-même.
IV – LES ANTICORPS
Libérés par les plasmocytes, les anticorps peuvent agir par 3 façons :
• Neutralisation : les anticorps entourent et se fixent sur le pathogène, empêchant l’adhérence cellulaire.
• Opsonisation : les anticorps entourent et se fixent sur le pathogène, facilitant sa phagocytose par les cellules
concernées.
• Activation par complément : les anticorps entourent et se fixent sur le pathogène, activant des compléments qui vont
permettre soit une opsonisation, soit une lyse du pathogène.
Les anticorps rejoignent en général le combat au bout de 5 à 6 jours. Toutefois, tout les plasmocytes ne sont pas effecteurs
d’anticorps. Certains acquièrent un phénotype de cellule-mémoire. Cette différenciation supplémentaire ne s’effectue qu’en
très petit nombre, mais suffisant pour qu’à la deuxième infection, la différenciation a immédiatement lieu et le processus de
production des anticorps ne prends plus alors que quelques heures.
Les vaccins fonctionnent selon le même système : ce sont en fait des pathogènes, mais peu virulents. L’action de ceux-ci va en
fait être la création de lymphocytes mémoires.
L’anticorps, en forme de Y, est constitué de deux chaines légères et de deux chaines lourdes. Les chaines lourdes sont
composées de 4 domaines, dont 3 constants (C
H
3, C
H
2 et C
H
1) et 1 variable (V
H
). Les chaines légères sont composées de
seulement 2 domaines, dont 1 variable (V
L
) et 1 constant (C
L
). Cela se présente ainsi :

Par Krys3000 (Groupe « The Trust » - http://www.cours-en-ligne.tk/) Page 3
Le site de fixation à l’antigène, nommé paratope, reconnait très spécifiquement une partie de l’antigène, nommée épitope. On
retrouve ce genre de structure sur certains récepteurs des lymphocytes T.
Les régions variables de chaque chaine présentent en fait des régions « Hypervariables » qu’on nomme CDR. Il existe 5 classes
d’anticorps :
1. IgM qui utilise une chaine lourde de type µ et une chaine légère de type λ ou κ. Utilisée dans les activations par
compléments.
2. IgD qui utilise une chaine lourde de type Δ et une chaine légère de type λ ou κ.
3. IgG qui utilise une chaine lourde de type γ et une chaine légère de type λ ou κ. Utilisée dans les activations par
compléments.
4. IgA qui utilise une chaine lourde de type α et une chaine légère de type λ ou κ.
5. IgE qui utilise une chaine lourde de type ε et une chaine légère de type λ ou κ.
V – LA DIVERSITÉ DES RÉCEPTEURS
TCR et BCR se ressemblent donc un peu.
Coté BCR, il y a une énorme diversité au niveau des types de récepteurs, qui se chiffre en milliard, pour occuper tout les types
protéiques. On n’a toutefois pas un milliard de gènes différent pour coder ça, évidemment, il y a donc une diversité qui va se
faire en associant 3 processus :
La diversité combinatoire : chaque chaine est codée par plusieurs segments génétiques qui se réarrangent afin de
former des combinaisons différentes. V
H
, D
H
et J
H
sont les segments composant les chaines lourdes, V
λ
et J
λ
sont les
segments des chaines légères de type λ, et V
κ
et J
κ
sont les segments qui composent les chaines légères de type κ.
Chaque segment est lui-même présent sous plusieurs formes. Ces associations donnent naissance à quelque chose de
l’ordre de 72 millions de combinaisons.
La diversité des jonctions : ce nombre est renforcé par le fait que le « recollage » des segments n’est pas toujours
parfait. On peut avoir des imperfections qui adjoignent des bouts supplémentaire ou font des recoupements.
Mutations : dans le cas des BCR, on a une autre source de diversité qui termine de porter le nombre au milliard de
combinaisons. Cette diversité est en fait les mutations somatiques que peuvent subir parfois les lymphocytes B.
Ce système de diversité est efficace car permet, avec quelques milliers de paires de bases, d’avoir des milliards de protéines
différentes. Toutefois, il y a un revers de médaille, puisque
ଶ
ଷ
des lymphocytes finissent en déchets : En gros, un lymphocyte B
réarrange ses locus de chaines lourdes, mais ne parvient à obtenir une bonne combinaison que dans un tiers des cas. S’il échoue,
il tente avec l’autre chromatide, et en cas de nouvel échec, le lymphocyte meure. Si on réussit au premier coup, il n’est
évidemment pas nécessaire de faire l’autre chromatique – ce serait même encore pire, puisqu’il ne faut pas se retrouver avec
deux chaines lourdes en même temps. Il y a donc un blocage du second chromatide qui a lieu – c’est l’exclusion allélique. Même
principe, en théorie, pour la chaine légère.
Les TCR ont également une variabilité. La zone variable des chaines β est composée de 3 segments Vβ, Dβ et Jβ. La zone
constante est codée par un segment Cβ.

Par Krys3000 (Groupe « The Trust » - http://www.cours-en-ligne.tk/) Page 4
Sur la chaine α, la zone variable est codée par Vα et Jα, et la zone constante par Cα. De la même façon que pour le BCR, ça se
réarrange en des tas de combinaisons possibles, mais au lieu de se faire dans la moelle, cela se fait dans le Thymus.
VI – LE DÉVELOPPEMENT DU SYSTÈME IMMUNITAIRE
Il est sensible aux radiations. Toutes les cellules du système immunitaire dérivent de cellules souches venant du foie (fœtus) ou
de la moelle osseuse (adulte). Elles se répartissent en deux lignées issues d’une même cellule pluripotente :
Myéloïde : le précurseur myéloïde peut lui-même donner deux lignées
o La première sera à l’origine des mégacaryocytes donnant les plaquettes et des érythroblastes donnant les
érythrocytes.
o La seconde sera à l’origine des granulocytes, des monocytes, et des précurseurs des mastocytes.
Lymphoïde : le précurseur lymphoïde se différencie en Lymphocytes T, B, ou NK. Le lymphocyte B passe du stade pro-B
au stade pre-B puis au lymphocyte B immature par l’action d’interleukine-7. Les lymphocytes migrent ensuite vers les
ganglions (entrant par les « high endothelial venules » et sortant par les vaisseaux lymphatiques efférents) et la rate
(entrant par les artérioles centrales et sortant par les veines trabéculaires).
VII – MALADIES
On en arrive parfois à faire des greffes de moelle osseuse, en cas de maladies génétiques, de leucémies, ou
d’immunodéficiences.
Il existe également des maladies auto-immunes, spécifiques d’un organe (diabète, sclérose) ou carrément systémiques (lupus).
Pour guérir des maladies, mis à part les greffes, on peut manipuler le système immunitaire pour soigner des gens. Les
transplantations d’organes concernent surtout les reins, le foie, le cœur et la cornée.
Pour protéger des maladies, on utilise les vaccins. Ceux qui existent de nos jours sont :
- DTC (ou DTP – Diphtérie / Tétanos / Coqueluche)
- Polio
- MMR (Rougeole / Oreillons / Rubéole)
- PCV (Pneumonies)
- HBC (Méningite bactérienne type B)
- Hépatite B
- Varicelle
- Papillomavirus Humain (Cancer du col de l’utérus)
Un vaccin idéal est un vaccin pas dangereux, protecteur, conférant une protection à long terme, qui induit la production
d’anticorps ou de lymphocytes, peu couteux, et facile à administrer.
1
/
4
100%