Le PLA (Poly Lactique Acide) est préparé, comme son nom Q|_| l

Le
PLA
(Poly Lactique Acide)
est
préparé, comme
son nom
Q|_|
l'indique,
à
partir d'acide lactique, lui-même tiré
de la
biomasse,
ce
qui lui
vaut d'être classé parmi
les
biopolymères —OOC—CH-
L
-in
Unité monomère
du PLA
La fabrication d'origine biologique
et
renouvelable
du PLA, sa
biocompatibilité
et sa
biodégradabilité
en
font dans certaines applications
un
concurrent intéressant
des
matières
plastiques
«
classiques
»
issues
de
produits pétroliers.
11-5-
Nommer
la
fonction chimique présente dans
la
chaîne macromoléculaire
du
PLA.
La dégradation
du
PLA
est
aisée, puisqu'on peut
le
dépolymériser
par
simple hydrolyse
en
présence
d'un
acide comme catalyseur.
On
reforme alors
le
monomère
:
l'acide
lactique.
On place
7,20 g de
copeaux
de
PLA,
équivalant
à 0,10 mol
d'unité monomère, dans
1,0 L
d'une solution aqueuse d'acide sulfurique
(de
formule H2S04),
que l'on
porte
à
reflux.
Après
8
heures
de
chauffage,
on
prélève
un
échantillon
de V = 50,0 mL
du
liquide.
On procède alors
à un
dosage
par une
solution étalonnée
de
soude
de
concentration
[NaOH]
= 0,10
mo/.L'1,
que l'on
suit
par
conductimétrie.
La
soude,
en
tant
que
base forte,
réagit d'abord
sur
l'acide
sulfurique,
que l'on
considérera comme
un
diacide fort.
La courbe
a =
f(Vsoude)
qui
porte
la
conductivité
en
fonction
du
volume
de
solution titrante
versée montre deux points anguleux
:
l'un
ayant pour abscisse
Ve-i
= 15,0 mL et le
deuxième
pour
Ve2 = 45,0
mL.
II-6- Ecrire
la
réaction
de
neutralisation
(1)
de
l'acide
sulfurique
par la
soude.
11-7-
Ecrire
la
réaction
de
neutralisation
(2)
de
l'acide
lactique
par
la
soude.
11-8-
Donner
les
variations
de
la
courbe
o-
=
f(Vsoude)
:
11-9-
Calculer
la
concentration d'acide sulfurique présent dans
la
solution d'hydrolyse.
11-10-
Calculer
la
concentration d'acide lactique présent dans
la
solution d'hydrolyse.
11-11-
Quel
est
le
taux d'avancement
de
l'hydrolyse après
8h
?

a.
Une
électrolyse
transforme de
l'énergie
chimique en
énergie électrique.
b. Dans une pile
électrochimique
en fonctionnement, la
réaction
qui se
produit
est
forcée.
c. La
tension à vide aux bornes d'une pile est sa f.e.m.
d.
Lorsqu'une
pile
débite,
une
réaction
de
réduction
a lieu à
l'électrode négative,
a.
Dans une
électrolyse,
la masse de la cathode ne
diminue
jamais.
•
Question n 2
a.
L'absorbance
d'une solution est plus grande si la concentration du
soluté
est
petite.
b.
La
conductance d'une solution est toujours proportionnelle à la concentration du
soluté,
c La fréquence
des collisions diminue si
la
concentration des
réactifs
diminue en solution.
d.
La
vitesse volumique d'une
réaction
chimique diminue
généralement au
cours du temps.
e. Un
catalyseur
augmente le temps de
demi-réaction.
•
Question n° 3
a. L'eau
de brome (ou de
dibrome),
permet de
caractériser
les
dérivés
organiques
halogènes.
b.
L'aspirine
possède
entre autres, un groupe
caractéristique
carboxyle.
c.
L'absorbance
d'une solution ne
dépend
pas de la longueur
d'onde
de
la lumière utilisée.
d. La
conductance d'une solution
dépend
des
électrodes utilisées.
e. Les
électrodes
circulent dans le pont
électrolytiquc
d'une pile qui
débite.
•
Question
n"
4
a. La déshydratation intramoléculaire
d'un alcool produit un alcane.
b.
L'état
liquide est un
état
physique fluide et
condensé.
c. La liquéfaction
est une
transformation
chimique exothermique.
d. Une solution aqueuse basique contient des ions oxonium.
e.
La conductivité
d'une solution s'exprime en m
•
s"1.
Question
n° 5
L'alcène
R-
CH
=
CH2
est
hydraté
en
présence
d'acide
sulfurique.
Pratiquement
un seul
composé
A se forme.
On
oxyde une masse m du
composé
A par un volume V de solution
acidifiée
de dichro-
mate de potassium de concentration C= 1,0 mol
•
L"1.
On obtient une masse m' = 20 g
d'un
composé
B qui donne un
précipité
avec le
DNPH,
mais est sans action sur le
réactif
de
Tollens
(nitrate d'argent
ammoniacal).
Données
:
Le
composé
A est totalement
oxydé.
Couples
d'oxydoréduction : B/A
et
CrjO?^
/
Cr3^.
Masse
molaire du
composé
B
:
M = 58 g
•
mol~'.
Quelle(s)
est (sont) l'(les) affirmation(s) exacte(s)?
a.
le
composé
B
formé
est le
propanai
;
b. le
composé
B
formé
est le butanone ;
c
le
composé
A
formé
est le butan-l-ol ;
d. le
composé
A
formé
est le propan-2-ol ;
e. le volume V de solution oxydante
utilisée
est de
l'ordre
de 0,11 L.
Question
n° 6
On
fait
réagir, à
chaud
et
à
reflux,
0,1 mole d'acide
méthanoïque
avec 0,1 mole de butan-2-ol,
suffisamment
longtemps
pour
que la réaction
soit
parvenue
à
l'équilibre.
Quelle(s)
est (sont) l'(les) affirmation(s) exacte(s) ?
a.
le produit obtenu est du
méthanoate
de butyle ;
b.
le produit obtenu est du
méthanoate
de
1-méthylpropyle
;
c.
la
réaction étudiée
est une saponification ;
d.
le chauffage permet
d'améliorer
le taux d'avancement
final
de
cette
réaction
;
e.
cette
réaction
serait
accélérée
en
présence
d'une faible
quantité
d'acide sulfurique.

4
X ^^ulu^S X ^ct^v
Dans
certaines
étoiles,
la fusion de trois noyaux
d'hélium
4, ne faisant intervenir
aucune
autre
particule,
est une
hypothèse
permettant d'expliquer
l'abondance
de noyaux de carbone.
Données
: c = 3,00.108 m.s"1 ; 1 u = 931,5
MeV/c2
Particule
ÎHe
ïc
14
p
Energie de liaison par
nucléon
(MeV)
7,08 7,68 7,47 7,52
a)
Lors
d'une
réaction nucléaire
quelconque, il y a conservation du nombre de protons.
b)
Le noyau
formé
lors
de cette
fusion
est le carbone 14.
c)
Cette
réaction
s'accompagne (l'une perte de masse.
d)
L
énergie libérée
lors
de la
réaction
a pour valeur
7,2
MeV
On
donne ci-contre le diagramme
énergétique
de l'atome
d'hydrogène.
Données
:
constante
de Planck : h = 6,62.10"34 J.s
célérité
de la
lumière
dans
le vide : c = 3,00.108 m.s"1.
1
eV=
1,6.10-19J
a) Le quantum
d'énergie
associé
une radiation lumineuse de longueur
d'onde dans le vide 662 nm a pour valeur 3,00.1 (T19 J
b)
Dans son
état
fondamental, l'atome
d'hydrogène
peut absorber un
quantum
d'énergie
de 10,2
eVpour
passer
sur son 1er
état excité
Lorsqu'il
est sur son 2eme
état
excité,
l'atome
d'hydrogène
peut :
c)
Absorber un quantum
d'énergie
de 1,9
eVpour
passer
sur son 1"état
excité
d)
Emettre un quantum
d'énergie
de 12,1 eV
lorsqu'il
retourne à son
état
fondamental
0-
-0.85
-1,5
-3,4
£(eV)
niveau fondamental
CD
Un
mobile 5 quasi ponctuel, de
masse
m = 500 g, glisse sur une piste AB
située
dans
un plan
vertical.
Il a
été lâché
du pointa
sans
vitesse
initiale.
La
partie AB est un quart de cercle de rayon R = 20 cm. Les frottements sont
négligeables.
Donnée
: on prendra pour
l'accélération
de la
pesanteur
g = 10m.s"2.
A
40 4cm)
a)
L'énergie
mécanique
du mobile est constante entre A et B.
1
,d6 i
b)
Pour
un angle 6,
l'énergie
cinétique
du mobile a pour expression
:
Ec =
—m(——)
.
2 dt
c)
Si on prend comme origine de I
énergie
potentielle l'altitude z = 0. I
énergie
potentielle initiale a
pour
valeur
1,0
J.
d)
La vitesse du mobile au point B est de 2,0 m.s1.

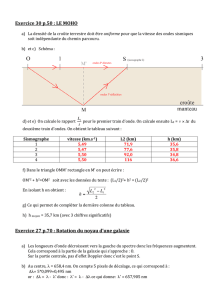
Un
faisceau
laser
éclaire
un fil vertical de
diamètre
a.
Un
ensemble
de
mesures,
réalisées
avec
des
fils
de
différents diamètres,
a
donné
les
résultats résumés
dans
le
graphe
ci
dessous,
où 0
(exprimé
en milliradians) est le
diamètre
angulaire de la
tache
centrale de
diffraction.
6(mrad)
25
20
15
10
10 15 20 \-^
a) La figure de
diffraction, observée
sur un
écran placé
à
l'arrière
du fil et perpendiculairement au
faisceau,
est
constituée
de
cercles
concentriques.
b)
La longueur d'onde de la
lumière émise
par le
laser
est environ X = 700 nm.
c)
La
lumière émise
par le
laser
est bleue.
d)
Si on augmente la longueur d'onde de la
lumière émise
par la source lumineuse, le
diamètre
angulaire
de la tache centrale diminue.
6^uV
(S
Soit
une
onde
de
célérité
v qui se
propage
le long
d'une
corde. La perturbation est
créée
au point S.
amplitude
f\' M
i
i H ^
a) En l'absence d'amortissement, tout point de la
corde
reproduit
la
perturbation
créée
en S.
b) Plus
la masse
linéique
de la
corde
est grande, plus la
célérité
de l'onde est grande.
c) Plus
la tension de la
corde
est grande, plus la
célérité
de l'onde est grande.
,
, , M'M
d)
La perturbation en M à la date t est
celle
qu 'avait le point M a la date t .
Un
haut-parleur
émet
une
onde
sonore
sinusoïdale
dont on peut faire varier la
fréquence.
Dans
le domaine
de
fréquence étudié
et compte tenu des conditions
expérimentales
cette
onde
se
propage
toujours
dans
l'air
avec
une
célérité
de 340 m.s" . Un microphone est
placé
à une
distance
d
=
20 cm du haut-parleur.
a)
L'air
peut
être considéré
comme un milieu non
dispersif lors
de cette
expérience.
b)
La longueur d'onde ne change pas avec
la fréquence.
c)
Si la
fréquence choisie
est
égale
à 1700 Hz, les signaux respectivement
émis
par le haut-parleur et
reçu
par le microphone sont en phase.
d)
Si on choisit une
fréquence égale
à un multiple entier de 1700 Hz les signaux respectivement
émis
par
le
haut-parleur et
reçu
par le microphone sont toujours en phase.
Dans
le
référentiel géocentrique,
on
étudie
un satellite
artificiel
de
masse
m = 2,5 t qui gravite autour de la
terre à une altitude
constante
h = 270 km. La terre est
considérée
comme ayant une
répartition
de
masse
à
symétrie sphérique.
Données
:
masse
de la Terre : MT= 6,0.1024 kg.
rayon de la Terre : /?r= 6,4.103 km.
constante
de gravitation : G = 6,67.10"" S.I.
V6«2,4 ;
V/6Ô«7,75
a) Le
mouvement
du satellite est uniforme.
b) L'accélération
du satellite est inversement proportionnelle à sa masse.
c) L'expression
de la vitesse du satellite et v =
„
I
^T
V
h
d)
La vitesse du satellite est v = 2,4 km.s'1.

On néglige
toutes
les forces dues à
l'air
:
la bille est en chute
libre.
Une
bille de masse m =
100
g est
lancée
verticalement
vers
le haut avec une vitesse initiale v0 = 5,0 m.s'.
Grâce
à un dispositif de chronophotographie, on a
relevé
l'altitude de la bille à intervalles de temps
réguliers.
On a pu
ainsi
tracer sa courbe
d'énergie
potentielle (origine choisie au niveau du sol) et sa
courbe
d'énergie cinétique
en fonction du temps.
Courte
2
•
~t
/
/
X
/
/ \
/
\
\ /
A
/ '\
\ / \
S S
y
\
V
Couttie
1
y
\
•
*r
\
0 0,1 0,2 0,3
0,4
0,5 0,6
0,7
0j8 0,9 1
(M
1,1 1,2 O 1,4
3
2,8
2,8
2,4
2,2
2
S
1.8
1,6
1,4
1,2
1
0,8
0,6
0,4
0,2
0
Données
:
Valeur
du champ de pesanteur
terrestre
g = 10 m.s'2 ; ^54
=»
7,4.
La
courbe 1
représente l'énergie
potentielle
de la
bille.
La
bille
a été
lancée
avec
une énergie mécanique
d'environ 2,7J.
La
bille
a été
lancée
d'un
point
d'altitude
h
égale
à 1,25 nt.
La
bille
retombe
sur le sol
avec
une
vitesse
d'environ 7,4
m.s'1.
Dans
un
référentiel
terrestre, on
considère
la chute d'un parachute de masse m = 20 kg portant une
masse
M.
A l'instant
initial,
le parachute et sa charge sont
abandonnés,
sans vitesse initiale, d'une hauteur
h • 320
m. On négligera
la
poussée d'Archimède.
,
Le
mouvement est
étudié
selon un axe
vertical
ascendant (Oz) dont l'origine O se situe sur le sol.
La
valeur du champ de pesanteur est
:
g - 10
m.s~*.
Le
parachute ne s'ouvre pas, la
résistance
de
l'air
est
négligée.
a) L'équation
horaire
du
parachute
chargé s'écrit
: z = +5,0 i.
b)
Le parachute
arme
au sol à la
vitesse
de 80
m.s~'.
Le
parachute s'ouvre et la
résistance
de
l'air
R est proportionnelle au
carré
de la vitesse
:
R = kv? avec
k = 20
unités
S.l.
Le
parachute et sa charge atteignent maintenant une vitesse limite de
7,0
m.s~'.
c)
La
masse
M
vaut
78
kg.
d) L'accélération
est nulle.
On néglige
toutes
les forces dues à
l'air.
Deux
élèves
de
temùrale
S
réalisent
une
expérience :
Pauline se trouve sur son balcon et
lâche
un ballon
sans vitesse initiale. Agathe se trouve dans la rue et voit le ballon atteindre le sol
/,
1
seconde plus
tard
Données :
Valeur
du champ de pesanteur g = 10 m.s"2 ;
1
2
11*«121;
-^-=0,24;
,/5Ô»7,l
; V5*2.23 ; ,/5\5*0,71
a)
le
ballon
a été
làclié
d'une hauteur h = 2,4 m
b)
Le
ballon
heurte le sol
avec
une
vitesse
de 39,6 km.h'1.
Les
deux
élèves
assistent ensuite à un spectacle de jonglage. D'une hauteur correspondant à sa stature, un
jongleur lance verticalement une balle.
Celle-ci
atteint une altitude de 2,5 m par rapport au sol avant de
redescendre.
c)
La
vitesse
initiale
de la
balle
est
inférieure
à 7,1 m.s'.
d)
La
balle
a mis 0,71 s pour
atteindre
son
altitude
maximale.
 6
6
1
/
6
100%