Voir l`invisible pour mieux soigner

24 heures avec
«Notre projet consiste à détruire la tumeur à
l’intérieur du corps en élevant sa tempéra-
ture au-dessus de 50 °C pendant quel-
ques minutes, sous contrôle de l’IRM. Comparée à l’écho-
graphie actuellement utilisée, l’imagerie par résonance
magnétique offre deux avantages : elle fournit des infor-
mations sur la température de la tumeur et permet une
précision de ciblage supérieure au millimètre. Les méthodes
thermiques sont moins traumatisantes que la chirurgie.
Elles sont comparables à la radiothérapie, sans le risque
des rayonnements ionisants sur les tissus voisins. »
Chrit Moonen, directeur du Laboratoire imagerie molé-
culaire et fonctionnelle (CNRS, UMR 5543, Inserm ERT
IMF), sait expliquer en peu de mots ce projet soutenu par
la Ligue contre le cancer et laisse volontiers ses étudiants
poursuivre son propos, avec la même simplicité – une
caractéristique de son laboratoire. Au détour de la conver-
sation, on apprend que Chrit Moonen, chercheur d’ori-
gine néerlandaise, a présidé en 2005 l’International Society
of Magnetic Resonance in Medicine et a travaillé dans plu-
sieurs laboratoires et universités des États-Unis, de Suisse
et de Grande-Bretagne avant de s’installer à Bordeaux.
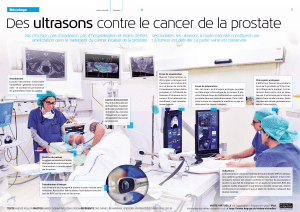
L’élimination d’une tumeur
par hyperthermie (chauffage)
est aujourd’hui une méthode
couramment employée. À
l’université Bordeaux 2, l’équipe de
Chrit Moonen innove en contrôlant
cette opération grâce à l’imagerie
par résonance magnétique (IRM)
qui permet de visualiser le contour
précis et la température exacte
de la zone à traiter.
32_VIVRE_DÉCEMBRE 2005
AL’équipe de Chrit Moonen
de l’université Bordeaux 2
au grand complet.
AL’IRM permet une précision
de ciblage de la tumeur
supérieure au millimètre.
ALes compétences sont variées au
sein de l’équipe qui comprend des
biologistes, des physiciens, des
informaticiens et des physiologistes.
VOIR L’INVISIBLE POUR

La première méthode utilise
des ultrasons d’une
fréquence de 1 mégahertz,
dirigés vers la zone à traiter
par une sorte de parabole de
la taille d’une assiette.
Charles Mougenot, qui
termine sa thèse de physique
au laboratoire sur cet
appareil, explique : « Comme
avec une loupe, nous
concentrons les ultrasons
sur un point focal, dont la
température augmente, et
ceci sans aucune intrusion
dans le corps. Comme
l’organe à traiter bouge
à chaque respiration,
l’IRM réoriente l’outil
automatiquement. »
Autre méthode
de chauffage : les
radiofréquences. Elles
consistent à glisser une
aiguille dans la tumeur
et à appliquer un courant
alternatif entre cette aiguille
et une seconde aiguille ou
une plaque de métal placée
sur la cuisse qui joue le rôle
de prise de terre. Les
mouvements des ions
provoquent une élévation
de la température.
Ces deux méthodes se
pratiquent déjà sous
contrôle échographique.
L’objectif de l’équipe de Chrit
Moonen est de remplacer
l’échographie
par l’imagerie par résonance
magnétique, qui permet
d’optimiser les protocoles
d’hyperthermie locale, et
par conséquent d’améliorer
les résultats cliniques.
VIVRE_DÉCEMBRE 2005_33
AAssocier recherche
fondamentale et recherche
clinique permet d’obtenir
des résultats plus
rapidement.
MIEUX SOIGNER
DEUX MÉTHODES D’HYPERTHERMIE (CHAUFFAGE) :
ULTRASONS ET RADIOFRÉQUENCES Chrit Moonen, au
premier plan, d’origine
néerlandaise, a
travaillé dans plusieurs
laboratoires à travers
le monde avant de
s’installer à Bordeaux.

34_VIVRE_DÉCEMBRE 2005
24 heures avec Reportage
L’objectif de
cette
manipulation
génétique
pourrait sembler
farfelu. Il ne faut pas
s’imaginer ces souris,
génétiquement
modifiées, briller dans
l’obscurité. Seul un
capteur très sensible
détecte leur luminosité.
Comme l’explique
Claire Rome, chercheuse
en biologie moléculaire
et en pharmacologie :
« Les souris luminescentes
obtenues par transgenèse
dégagent de la lumière
lorsqu’on élève leur
température de quelques
degrés. Il est donc
possible de visualiser avec
une caméra très sensible
l’effet des thérapies
thermiques appliquées sur
leurs organes. »
Concrètement, le gène
qui donne le caractère
lumineux est multiplié
dans des cultures de
bactéries, puis injecté
dans un œuf de souris ;
la gestation se déroule
dans l’utérus de la mère
porteuse.
Franck Couillaud,
chercheur en biologie
moléculaire, souhaite
perfectionner l’animal :
« Nous voulons créer une
souris qui serait à la fois
luminescente et
fluorescente, avec laquelle
nous espérons obtenir
une image en trois
dimensions.» Les données
précises (localisation et
degré de chaleur atteint
par la tumeur) sont
nécessaires pour mieux
circonscrire et détruire
les cellules cancéreuses.
Réunir toutes les compétences
Le concept est clair mais sa mise en œuvre complexe.
Travailler avec l’aimant d’une IRM (cette force invisible
qui vous arrache des mains tout objet ferreux, qui déma-
gnétise les téléphones portables et les cartes bancaires)
exige d’adapter outils et méthodes. Outre le contour de
la tumeur fourni par l’IRM, le logiciel d’origine a été modi-
fié pour établir la carte des températures des tissus, en
temps réel, toutes les deux ou trois secondes. Pratiquée
en concertation étroite avec des médecins, cette recherche
exige le rassemblement de compétences variées, celles de
physiciens, d’informaticiens, de biologistes et de
physiologistes. Le professeur Chrit Moonen confie : «Le
problème de toute équipe pluridisciplinaire, c’est l’absence
ALe logiciel d’origine de l’IRM
a été modifié pour établir, en plus
du contour de la tumeur, la carte
des températures des tissus en
temps réel.
POURQUOI CRÉER
DES SOURIS LUMINESCENTES
ET FLUORESCENTES ?
6
patients ont été
traités par
radiofréquence
depuis novembre
2004

VIVRE_DÉCEMBRE 2005_35
d’un langage commun. Un effort particulier est donc nécessaire
pour bien communiquer. Médecins ou radiologues doivent
expliquer exactement ce qu’ils veulent faire, physiciens et
informaticiens doivent traduire leurs problèmes en langage
clair. C’est pourquoi nous organisons des réunions chaque
mardi, de 17 h à 19 h, dans un esprit très peu formel. »
Une méthode appliquée début 2006
Associer la recherche fondamentale et la recherche clinique
permet d’obtenir des résultats plus rapidement. Ainsi,
deux méthodes de chauffage : les ultrasons focalisés et
les radiofréquences (voir encadré p. 33), sous contrôle
IRM, ont été testés sur des souris, des rats, des lapins puis
sur des porcs. Des souris génétiquement modifiées ont
ALe laboratoire vit au rythme de la multiplication des cultures de cellules
humaines tumorales ou saines et des bactéries Escherichia coli porteuses
de gênes à introduire dans les animaux.
ALa Ligue contre le cancer
a participé au fonctionne-
ment de l’animalerie
où vivent les 4 500 souris
nécessaires aux
expérimentations.
AToutes les données issues de l’IRM
sont ensuite traitées et observées
sur ordinateur.
été créées pour visualiser facilement l’effet de ces méthodes
de chauffage (voir encadré p. 34). Six patients ont été
traités par radiofréquence depuis novembre 2004 pour
une tumeur au foie, une seule
récidive est apparue.
Le CCPPRB (Comité consultatif de protection des per-
sonnes dans la recherche) et le ministère de la Santé vien-
nent de donner leur accord pour l’utilisation des ultra-
sons focalisés pour traiter les tumeurs du sein.
«L’appli-
cation commencera début 2006,
dès que les radiologues se
sentiront à l’aise avec cette technique », annonce Chrit
Moonen. Le laboratoire développe d’autres méthodes de
thérapies localisées, sans ablation, toujours visualisées
par IRM. Une compétence désormais reconnue dans le
monde entier. PIERRICK BOURGAULT
UNE
ÉQUIPE PLURI-
DISCIPLINAIRE
« Pour nous, il est très
important d’associer la
recherche fondamentale et
la recherche clinique dans une
même équipe. » Chrit Moonen
réunit autour de lui une
vingtaine de chercheurs,
ingénieurs et doctorants.
Plusieurs médecins et
chefs de service du CHU,
comme Jean Palussière,
Nicolas Grenier ou
Hervé Trillaud, les rejoignent
une ou deux demi-journées
par semaine.

L’une des forces de la cellule
cancéreuse est sa grande
capacité à échapper au
système immunitaire. En
particulier, elle passe pour
normale aux yeux des
cellules dendritiques, dont
le rôle est précisément
d’initier la réponse
immunitaire en repérant
puis en « présentant » les
antigènes (molécules
reconnues comme
étrangères) à d’autres
cellules du système
immunitaire. Pourtant, une
équipe de chercheurs de
l’université de Pittsburgh*
a réussi, chez la souris, à
« forcer la main » de cellules
dendritiques au contact de
cellules d’un mélanome
(B16), en les « provoquant »
à l’aide de fragments
de bactéries et virus non
pathogènes. Une réponse
a été observée. Des
lymphocytes T se sont
attaqués à la tumeur,
laquelle a régressé.
Ces travaux pourraient
déboucher sur un nouveau
type d’immunothérapie.
*Cancer Research 65, pp. 10 059-
10 067, 1er novembre 2005.
Aux États-Unis, le National
Cancer Institute et le
National Human Genome
Research Institute ont lancé
en décembre 2005 le projet
« Atlas génomique du
cancer », dont le coût final
pourrait dépasser le milliard
de dollars.
L’objectif est très ambitieux :
décrypter et cataloguer
l’ensemble des anomalies
génétiques qui provoquent
les cancers. Or on dénombre
aujourd’hui plus de
200 cancers distincts. Les
techniques de séquençage
rapide qui ont permis en
2003 de décrypter le génome
humain seront mises à
contribution sur des milliers
d’échantillons de tissus
cancéreux et sains. Dans un
premier temps, un projet
pilote, doté de 100 millions
de dollars (83 millions
d’euros) sur trois ans, aura
pour objectif de tester des
méthodes de travail sur un
petit nombre de tumeurs.
36_VIVRE_DÉCEMBRE 2005
« Atlas génomique »
Plus de 200 cancers
SÉQUENÇAGE
DU GÉNOME
HUMAIN.
New-York
Un nid accueille la métastase
Une équipe de l’université de Cornell* a découvert, chez la souris, un mécanisme fondamental dans la dissémination
des métastases. Elle a montré que les cellules tumorales mobilisent tout d’abord des cellules de la moelle osseuse
et contrôlent leur migration vers des sites où ces cellules de la moelle osseuse préparent le terrain pour les
métastases à venir. Ce mécanisme est contrôlé par des signaux chimiques émis par les cellules tumorales. De
nouvelles techniques de lutte contre les métastases pourraient consister à perturber ces mécanismes.
*Nature 438, pp. 820-827, 8 décembre 2005.
Organisme
Réponse
immunitaire
forcée
TUMEURS
CANCÉREUSES
GROSSIES
7 500 FOIS
ANTIGÈNE
c’est une molécule
reconnue comme
étrangère
EnBreF
 6
6
1
/
6
100%