Les maladies auto-immunes : quand les chirurgiens

Dental Tribune Édition Française | Novembre 2016
26 CONFÉRENCE À VENIR
SPÉCIAL ADF
UN POINT – E128 |SAMEDI 26 NOVEMBRE|9H–12H
Responsable scientifique : Pr Jacques-Olivier Pers (UFR d’Odontologie UBO Brest)
Intervenants: Sylvie Boisramé,Sophie-Myriam Dridi, Hervé Boutigny,
Vincent Blasco-Baque, Hubert Marotte
Les maladies auto-immunes : quand
les chirurgiens-dentistes s’en mêlent
Encore mal connues du grand public, les
maladies auto-immunes touchent pour-
tant près de 5 % de la population et sont à
l’origine de manifestations cliniques va-
riées n’épargnant pas la sphère orofaciale.
Par exemple, dans le syndrome de Gouge-
rot-Sjögren, qui est caractérisé par une at-
teinte des glandes exocrines et en particu-
lier des glandes salivaires, les manifesta-
tions buccales sont au premier plan avec
l’existence d’une xérostomie impactant
souvent fortement la qualité de vie des pa-
tients. Dans le groupe des dermatoses bul-
leuses auto-immunes, l’atteinte de la mu-
queuse buccale peut être inaugurale et
rester longtemps isolée, menant parfois à
un retard de diagnostic. De plus, plusieurs
études suggèrent que la présence de Por-
phyromonas gingivalis, une des principa-
les bactéries parodontopathogènes, pour-
rait être impliquée dans le développe-
ment de la polyarthrite rhumatoïde. Le
lien entre diabète et santé bucco-dentaire
est également très important car le traite-
ment parodontal peut avoir le même effet
qu’un médicament sur le diabète. Ces
quelques éléments mettent bien en évi-
dence le rôle clé du chirurgien-dentiste
dans la prise en charge pluridisciplinaire de
ces patients mais également dans la stabili-
sation voire la prévention de certaines de
ces pathologies.
Quel est le dénominateur commun entre la
polyarthrite rhumatoïde (PR), le syndrome
de Gougerot-Sjögren (SGS), le diabète ou cer-
taines dermatoses bulleuses ? Il s’agit de mal-
adies auto-immunes ayant des répercus-
sions sur la sphère oro-faciale. Le rôle du chi-
rurgien-dentiste sera donc déterminant dans
le diagnostic et la prise en charge pluridisci-
plinaire des patients atteints par ces mal-
adies auto-immunes.
Pour cela, il doit connaître les différentes
pathologies auto-immunes d’intérêt en mé-
decine bucco-dentaire, il doit savoir les iden-
tifier, être en mesure d’accompagner les pa-
tients par une prise en charge adaptée et
considérer les risques et les effets indésira-
bles de leurs traitements.
Quel lien entre
Porphyromonas gingivalis
et polyarthrite rhumatoïde ?
L’association entre la PR et la parodontite a
été suspectée depuis plus d’un siècle avec
comme conséquence « l’édentation théra-
peutique » des patients. Depuis plusieurs
décennies, cette association a été confirmée
par des études épidémiologiques avec d’un
point de vue physiopathologique des fac-
teurs génétiques et environnementaux
communs (tabagisme, excès de cytokines
pro-inflammatoires comme le TNF-α...) [1].
Récemment, une bactérie de la flore dentaire
a été identifiée comme étant le chaînon
manquant entre ces deux maladies. Il s’agit
de Porphyromonas gingivalis (Pg) [2], une
bactérie gram négatif anaérobie détectable
notamment chez les patients atteints de pa-
rodontites agressives. Elle a deux caractéris-
tiques expliquant son implication dans la
physiopathologie de la PR. La première est
l’expression d’une peptidylarginine déimi-
nase (PAD) qui est une enzyme intervenant
dans la modification post-traductionnelle
de l’arginine en citrulline. La seconde est
l’expression d’une gingipaïne qui dégrade
les protéines en peptides libérant ainsi des
arginines qui pourront être citrullinées. Ces
deux mécanismes entraînent un excès de
protéines citrullinées dans la gencive et fa-
vorisent la production d’anticorps anti-pro-
téines citrullinées (ACPA). Ces fameux ACPA
peuvent être détectés plusieurs années
avant les signes cliniques de la PR. Un des en-
jeux serait l’amélioration de la PR par le trai-
tement de la maladie parodontale et inverse-
ment. Ainsi, quelques données suggèrent un
effet bénéfique d’un traitement parodontal
sur la l’évolution de la PR [3, 4] mais des étu-
des complémentaires sont nécessaires.
Quoiqu’il en soit, l’instauration de mesures
d’hygiène dentaire et un suivi parodontal
sont particulièrement importants chez ces
patients susceptibles d’être traités par im-
munothérapies, qui sont à l’origine d’un état
d’immunodépression, mais également par
biphosphonates.
Le syndrome de Gougerot
Sjögren : Heureusement que
l’odontologie s’en mêle !
Le SGS est une maladie sournoise car pro-
gressive qui se caractérise par l’accumulation
d’infiltrats lymphocytaires au niveau des
glandes exocrines aboutissant à leur destruc-
tion et donc à une diminution de leur sécré-
tion [5]. Au niveau de la cavité orale, ce SGS est
caractérisé par une diminution salivaire signi-
ficative aboutissant à des manifestations
bucco-dentaires liées à la modification de l’é-
cologie microbienne de la cavité orale. La
perte de la lubrification, du pouvoir tampon
salivaire, des effets antimicrobiens entraî-
nent une altération de la qualité de vie et en-
gendrent des lésions carieuses, des patholo-
gies parodontales, des candidoses mais aussi
une fragilité de la muqueuse buccale.
Déjà en 2009, Antoniazzi et al. ont rapporté
dans leur étude comparative SGS versus té-
moins des indices parodontaux aggravés (in-
dice de plaque, indice gingival, indice de sai-
gnement) et de plus grandes profondeurs de
poche [6].
Une étude prospective récente, comparant
des patients atteints de SGS et des patients at-
teints d’hyposialie, a montré une augmenta-
tion de l’indice CAO et une plus grande sévé-
rité de la maladie parodontale chez les pa-
tients atteints de SGS, en lien avec une dimi-
nution significative du pH salivaire [7].
La connaissance de cette maladie permet
de la dépister précocement, de proposer des
thérapeutiques comme la stimulation sali-
vaire, de surveiller de façon rapprochée ces
patients et de pouvoir les adresser vers un
centre compétent pour une prise en charge
pluridisciplinaire et optimale.
Quand le traitement
parodontal améliore le
contrôle glycémique d’un
patient diabétique…
Le diabète est une affection chronique mé-
tabolique fréquente caractérisée par une
hyperglycémie (taux de sucre dans le sang
trop élevé). Cette pathologie est liée à une des-
truction auto-immune des cellules pancréa-
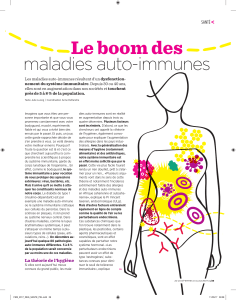
Fig. 1 : Interrelations entre maladie parodontale et polyarthrite rhumatoïde.
Fig. 2 : Perlèches (atteinte candidosique des commissures labiales) liées à l’hyposyalie chez un patient souffrant d’un syndrome de Gougerot Sjögren. |Fig. 3 : Patient diabétique atteint de parodontite chronique gé-
néralisée. |Fig. 4 : Manifestations gingivales d’une dermatose bulleuse auto-immune.
Infection à Porphyromonas
gingivalis (PG)
Maladie parodontale
Syndrome inflammatoire
local et systémique
Production enzyme PAD
et protéases (gingipains)
Rupture de tolérance:
production Ac anti-protéines
citrullinées (ACPA)
2 3 4

tiques chargées de la production de l’insu-
line. En France, le nombre de diabétiques est
d’environ 2,9 millions de personnes soit envi-
ron 4,4 % de la population. Le patient diabé-
tique est caractérisé par de nombreuses com-
plications comme les maladies cardio-vascu-
laires, néphropathies, neuropathies et réti-
nopathies mais également les infections
buccales. La maladie parodontale est même
considérée comme la sixième complication
du diabète. En effet, les personnes diabé-
tiques sont plus fréquemment atteintes de
maladies parodontales, et de plus elles sont
plus sévères que chez les autres patients. De
nombreuses études suggèrent un rôle im-
portant des infections buccales dans le
contrôle glycémique des patients. L’effet du
détartrage/surfaçage radiculaire et de l’en-
seignement à l’hygiène diminuerait de
0,40 % le taux d’hémoglobine glyquée
(HbA1c), qui est un paramètre de suivi du dia-
bète, après 3 à 4 mois chez les patients diabé-
tiques [8]. Il existe des preuves en faveur
d’une amélioration du contrôle glycémique
chez les patients diabétiques après un traite-
ment de la parodontite [9]. De ce fait, le chi-
rurgien-dentiste devient un acteur médical
majeur de la prise en charge spécifique des
patients diabétiques. Nous discuterons com-
ment le chirurgien-dentiste pourra optimi-
ser le diagnostic et le traitement de ces pa-
tients.
Dermatoses bulleuses
auto-immunes : les
odontologistes aussi
sont concernés !
Les dermatoses bulleuses auto-immunes
constituent un groupe hétérogène de mal-
adies à expression cutanéo-muqueuse, peu
répandu et de pronostic variable [10]. Pour
un grand nombre de ces maladies, l’atteinte
des muqueuses buccales est fréquente, par-
ticulière et s’accompagne d’importants si-
gnes fonctionnels (saignements spontanés,
douleurs intenses) avec des répercussions
néfastes sur la qualité de vie et la santé géné-
rale (dénutrition, amaigrissement, dépres-
sion).
Lorsque l’atteinte des muqueuses buccales
est inaugurale ou prédominante, les patients
consultent généralement leur chirurgien-
dentiste. Malheureusement ces derniers
semblent mal connaître ces dermatoses et
n’ont pas toujours une stratégie thérapeu-
tique bien définie. L’atteinte gingivale exclu-
sive est par ailleurs souvent confondue avec
les formes cliniques sévères des gingivites in-
duites par la plaque dentaire.
Par conséquent, afin d’optimiser leur prise
en charge, le chirurgien-dentiste devra
connaître la sémiologie des manifestations
buccales des dermatoses bulleuses auto-im-
munes, comprendre son rôle dans la démar-
che diagnostique afin d’éviter les retards de
diagnostic et les actes iatrogènes, s’adapter
au stade évolutif de la dermatose et à sa sévé-
rité et connaître les récentes recommanda-
tions professionnelles.
Ainsi, ces différentes pathologies auto-im-
munes et l’implication du chirurgien-den-
tiste dans leur prise en charge buccodentaire
seront explicitées par 4 conférenciers spécia-
listes au travers d’exemples concrets et de
nombreux cas cliniques.
Références :
1 Marotte H, Farge P,Gaudin P, Alexandre
C,Mougin B, Miossec P. The association bet-
ween periodontal disease and joint des-
truction in rheumatoid arthritis extends
the link between the HLA-DR shared epi-
tope and severity of bone destruction. Ann
Rheum Dis 2006;65:905-9.
2 Salemi S, Biondo MI, Fiorentino C et al.
Could early rheumatoid arthritis resolve
after periodontitis treatment only?: case
report and review of the literature. Medi-
cine (Baltimore) 2014;93:e195.
3 Mikuls TR, Payne JB, Yu F et al. Periodontitis
and Porphyromonas gingivalis in patients
with rheumatoid arthritis. Arthritis Rheu-
matol 2014;66:1090-100.
4 Kaur S, Bright R, Proudman SM, Bartold
PM. Does periodontal treatment influence
clinical and biochemical measures for
rheumatoid arthritis? A systematic review
and meta-analysis. Semin Arthritis
Rheum 2014;44:113-22.
5 Youinou P, Pers JO. Primary Sjögren’s syn-
drome at a glance today. Joint Bone Spine.
2015 Mar;82(2):75-6.
6 Antoniazzi, R. P., L. A. Miranda, et al. (2009).
"Periodontal conditions of individuals
with Sjogren’s syndrome." J Periodontol
80(3): 429-435.
7 Le Gall M, Cornec D, Pers JO, Saraux A;
Jousse-Joulin S, Cochener B, Roguedas-
Contios AM, Devauchelle-Pensec V, Bois-
ramé S. A prospective evaluation of dental
and periodontal status in patients with
suspected Sjögren’s syndrome. Joint Bone
Spine. 2016; 83 (2) : 235-236.
8 Teeuw WJ, Gerdes VE, Loos BG. Effect of per-
iodontal treatment on glycemic control of
diabetic patients: a systematic review and
meta-analysis. Diabetes Care. 2010
Feb;33(2):421-7
9 Simpson TC, Weldon JC, Worthington HV,
Needleman I, Wild SH, Moles DR, Stevenson
B, Furness S, Iheozor-Ejiofor Z. Treatment
of periodontal disease for glycaemic
control in people with diabetes mellitus.
Cochrane Database Syst Rev. 2015 Nov
6;(11):CD004714.
10 Ramos-e-Silva M, Ferreira A, Jacques Cd.
Oral involvement in autoimmune bullous
diseases. Clin Dermatol. 2011 Jul-
Aug;29(4):443-54.
Sophie Jung
Pôle de Médecine et de Chirurgie Bucco-Dentaires,
Hôpitaux Universitaires de Strasbourg, Faculté de
Chirurgie Dentaire, Université de Strasbourg,
France
Hubert Marotte
Départment de Rhumatologie, CHU de Saint-
Étienne, Inserm 1059/LBTO, Université Jean-Mo-
net, Université de Lyon, 42270 Saint-Étienne,
France
Sylvie Boisramé
Laboratoire Universitaire de Biodiversité et d’Eco-
logie Microbienne (LUBEM-EA 3882), Université de
Bretagne Occidentale, UBL, CHRU de Brest, Faculté
de Chirurgie Dentaire, Brest, France
Vincent Blasco-Baque
INSERM, UMR 1048, Institut de Maladies Métabo-
liques et Cardiovasculaires, L.U. 51 « Parodontites et
Maladies Générales », Université Paul Sabatier, Fa-
culté de Chirurgie Dentaire, Toulouse, France
Sophie-Myriam Dridi
Service d’Odontologie, Hôpital Albert Chenevier-
Henri Mondor, Université Paris 5 René Descartes,
Paris, France
Hervé Boutigny
Centre Abel Caumartin - Service d’Odontologie
CHRU de Lille Faculté de chirurgie dentaire,Lille,
France
Jacques-Olivier Pers
CHRU Morvan, Université de Brest, Labex « immu-
notherapy, graft, oncology », laboratoire d’immu-
nothérapies et pathologies lymphocytaires B,
EA2216, Inserm ESPRI ERI29, Brest, France
T
A
B
L
E
T
T
E
T
R
A
N
S
T
H
O
R
A
C
I
Q
U
E
M
O
D
U
L
E
C
O
R
D
O
N
S
P
E
N
D
A
N
T
S
M
O
D
U
L
E
O
R
T
H
O
D
O
N
T
I
E
la nouvelle vision du confort
pour votre quotidien et vos patients.
Le nouveau PACIFIC
est maintenant en
version ambidextre,
LE FAUTEUIL MONOCOQUE
Avec plus de 300 couleurs au choix,
une ergonomie de travail optimale,
et pour vos patients, un confort inégalé.
Plus dinformations sur www.airel-quetin.com
Airel Quetin 917, Rue Marcel Paul 94500 Champigny-sur-Marne Tél : 01 48 82 22 22 [email protected]
Dispositif médical : Classe IIa# !$"!
Pour toute information complémentaire, se référer à la notice dutilisation
Dental Tribune Édition Française | Novembre 2016 CONFÉRENCE À VENIR
1
/
2
100%