Télécharger le PDF

Gènéthique - n°34 octobre 2002
...
Lettre d’information et d’analyse sur l’actualité scientifique
N°34 : octobre 2002
Essais interrompus : quel avenir pour la thérapie génique ?
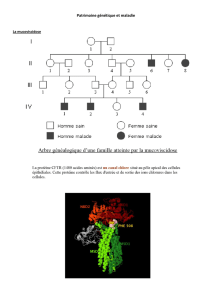
Le 4 octobre la presse annonçait que
l'essai de thérapie génique mené en
France sur des "enfants bulles"
souffrant d'un déficit immunitaire
sévère était suspendu. Doit-on en
conclure que la thérapie génique n’a
pas d’avenir ?
Comment ça marche ?
Depuis plus de dix ans maintenant, la
thérapie génique suscite beaucoup
d’espoirs. Son principe est simple sur le
plan théorique : pour les maladies liées
à l’altération d’un gène par exemple, il
s’agit de remplacer un gène muté par le
gène normal, si l’on en connaît la
séquence et le mode de régulation,
parfois très complexe. On peut aussi
imaginer introduire des gènes
produisant des substances toxiques
pour les cellules cancéreuses, ou
déclenchant un programme d’apoptose
(autodestruction).
Les difficultés rencontrées
Différents problèmes techniques sont
alors apparus rendant difficile, voire
impossible pour certaines maladies, le
recours à cette thérapie. La première
condition déjà évoquée est la
connaissance du gène et son mode de
régulation ; si celui-ci est trop
complexe, ou trop fin, on risque de ne
pas pouvoir maîtriser suffisamment
l’expression du gène introduit. Dans la
faisabilité technique, intervient aussi
l’accessibilité des cellules cibles :
lorsqu’il s’agit de cellules sanguines,
l’accessibilité est facile, puisqu’on va
prélever des cellules souches
hématopoïétiques de la moelle osseuse
pour les « guérir », et les réinjecter aux
patients (essais ex vivo). Lorsqu’il s’agit
de pathologie musculaire, ou d’autres
cellules qui ne poussent pas en culture,
il faut trouver un vecteur pour
transporter le gène au bon endroit
(essais in vivo). L’adénovirus
recombinant peut être utilisé : on lui
enlève certaines parties de sa
séquence (ce qui l’empêche ainsi de
produire de nouveaux virus), pour
insérer à la place le gène normal, ou du
moins les parties absolument
indispensables au fonctionnement de
ce gène : c’est le cas pour la
dystrophine, gène de très grande taille,
qu’il faut « réduire afin qu’il puisse
« entrer » dans le virus. Une autre
difficulté réside dans la durée de
l’expression de ce gène, une fois inséré
dans les bonnes cellules : même dans
des cellules ne se divisant pas, comme
les hépatocytes, l’expression du gène
se réduit au fil du temps. Enfin, si le
vecteur est un rétrovirus, il peut, en
s’insérant au hasard dans le génome,
altérer un gène ou « réveiller » un
gène de multiplication cellulaire ; c’est
ce qui semble s’être produit, avec
l’essai jusqu’ici très positif, de thérapie
génique des bébés bulles atteints d’un
déficit immunitaire combiné sévère lié à
l’X (SCID-X) ; ce risque était considéré
comme théorique, mais peut s’être
manifesté chez cet enfant présentant
une prolifération de globules blancs.
Cependant, il reste à démontrer qu’il
s’agit bien de ce mécanisme, et non
d’un autre phénomène. Les essais de
thérapie génique, qui avaient été
suspendus aux USA à la suite de cette
annonce ont repris.
Les résultats
Les problèmes techniques cités plus
haut expliquent le faible taux de
réussite, malgré un grand nombre
d’essais en cours : depuis 1989, plus
de 500 essais ont été lancés : les 2/3
pour des cancers, 14% pour des
maladies héréditaires et 9% pour des
maladies infectieuses. Les difficultés
techniques rencontrées, comme
certains effets indésirables graves ont
fait retomber l’enthousiasme initial.
Cependant, même si la thérapie
génique n’est pas la panacée espérée,
elle reste certainement une voie
thérapeutique, au moins pour certaines
maladies bien ciblées, compte tenu de
tous les impératifs techniques évoqués.
Par ailleurs, elle peut aussi être très
utilisée en étant couplée à d’autres
techniques comme la thérapie
cellulaire, par exemple pour des
maladies héréditaires de la peau
(cf : février 2001).
Recherche sur l’embryon : débats au Parlement européen !
Programme 2002-2006
En avril dernier, le Parlement Européen
adoptait le VIème Programme Cadre
Recherche et Développement (VI°
PCRD), pour la période 2002-2006 et
pour un montant de 17,5 millions
d’euros, ce qui en fait le troisième
budget de l’Union européenne.
Après un an de débat, en commission
Industrie et Recherche, et le vote en
première et deuxième lectures, en
séance plénière, les échanges furent

Gènéthique - n°34 octobre 2002
très animés sur la partie
« biotechnologies et sciences du
vivant ». Les partisans de la recherche
sur l’embryon humain refusèrent de
rouvrir le débat qui avait eu lieu au sein
de la commission temporaire de
génétique humaine sur « les enjeux
économiques, juridiques et éthiques de
la médecine moderne », pendant toute
l’année 2001. Cette commission avait
adopté une résolution tout à fait
claire en refusant de financer la
recherche sur les embryons
humains, le clonage thérapeutique et
reproductif et avait ainsi réaffirmé la
position constante des Institutions
européennes sur le respect de la
dignité et de la vie humaines.
Cependant en session plénière, la
résolution, rendue incompréhensible
et contradictoire par le jeu des
amendements, avait été finalement
rejetée, faute d’une majorité dans un
sens ou dans l’autre, preuve qu’aucun
compromis n’est possible sur cette
question si sensible.
En avril, donc, le VI° PCRD est adopté
selon une procédure de codécision
entre le Conseil (chefs d’Etats et de
gouvernements) et le Parlement
européen. Les programmes spécifiques
(comme les biotechnologies et les
sciences du vivant) sont eux adoptés
par le Conseil, à la majorité qualifiée.
Contre le financement
La présidence danoise, (le Danemark
préside l’Union européenne du 1er
Juillet au 31 Décembre 2002) suite à
l’initiative d’un ancien député européen,
Rocco Butiglione, aujourd’hui ministre
italien des affaires européennes, et
suivant la procédure, a proposé le 30
juillet dernier de geler tout
financement de la recherche sur les
embryons humains. Elle a souhaité ce
compromis après avoir constaté que
l’opinion de nos sociétés n’est pas
encore prête à accepter, pour des
raisons éthiques, la recherche sur les
embryons humains (toujours considéré
dans les débats comme un être
humain). Cette proposition a été
soutenue par l’Autriche, le Portugal,
l’Irlande, et l’Italie, l’Allemagne
s’abstenant.
Pour le financement
Mais avant l’adoption finale des
programmes spécifiques, étape ultime
pour débloquer les crédits européens
de la Recherche, plusieurs rencontres
avaient eu lieu entre le rapporteur, le
français Gérard Caudron, la
Commission européenne et le Conseil
des ministres de la Recherche en vue
d’une position commune sur le respect
de la dignité humaine, formule assez
floue qui peut permettre l’utilisation des
embryons humains pour traiter des
maladies incurables. Le rapporteur
français et quelques députés de la
Commission Industrie ont déclaré
que cette position commune devait être
considérée comme un accord
justifiant le financement de la
recherche embryonnaire et motivant
leur refus de soutenir le compromis
du ministre danois.
Que dit la procédure ?
Lors d’une conférence de presse le 26
septembre, un autre groupe de
députés, favorables au respect de l’être
humain quelque soit son stade de
développement : l’allemande Hiltrud
Breyer, l’irlandaise Dana Scallon, la
française Elizabeth Montfort, l’italien
Mario Mauro et le Portugais José
Ribeiro e Castro, a contesté la
légitimité de « l’accord » conclu entre le
rapporteur français et quelques
députés de la Commission Industrie au
motif que les programmes spécifiques
relevaient de la décision du Conseil et
non d’une codécision avec le
Parlement européen, et qu’il n’était
donc pas conforme à la procédure. Ils
ont, par ailleurs, indiqué que cette
bataille de procédure cachait la
question de fond : « Peut-on utiliser
l’être humain comme matériau pour
soigner d’autres êtres humains, atteints
de maladies incurables ? »
Recherche sur l’embryon : la décision du Conseil européen
C’est dans le contexte polémique décrit
plus haut que le Conseil des ministres
européens de la Recherche a adopté,
le 30 septembre dernier, la décision
finale qui stipule dans l’article 3,
Application des principes éthiques :
« Le Conseil et la Commission sont
convenus que les dispositions
d’application précises concernant les
activités de recherche comportant
l’utilisation d’embryons humains et de
cellules souches embryonnaires
humaines qui peuvent être financées
au titre du sixième programme cadre
seront définies d’ici le 31 décembre
2003. La Commission déclare que,
dans l’intervalle et en attendant la
définition des dispositions
d’application précises, elle ne
proposera pas de financer ces
activités de recherche, à l’exception
de l’étude de cellules souches
embryonnaires humaines mises en
réserve dans des banques ou
isolées en culture. La Commission
suivra les progrès et les besoins de la
science…en tenant compte des avis du
Groupe européen d’éthique et du
Groupe européen des conseillers pour
l’éthique de la biotechnologie ».
(Document du Conseil de l’Union
européenne. 12374/02 ADD1)
Un rapport sera présenté au
Parlement européen pour avis, au
premier semestre 2003.
On reste stupéfait du contenu de cette
décision : ce n’est pas la recherche sur
les embryons qui est mise en cause,
puisqu’il est possible de financer
l’études de cellules souches
embryonnaires déjà disponibles, mais
la manière de la faire admettre à
l’opinion de nos sociétés. On est loin de
la position commune arrêtée par le
Conseil le 28 Janvier 2002.
Il est nécessaire d’ajouter que la
France, représentée par le ministre des
affaires européennes, Noëlle Lenoir,
ancienne présidente du Groupe
européen d’éthique, connue pour son
soutien à ce type de recherche, a rejeté
le compromis danois pourtant conforme
à la législation française aujourd’hui en
vigueur : la révision des lois de
bioéthique n’étant pas terminée, c’est la
loi de 1994 qui s’applique, elle
n’autorise pas la recherche sur
l’embryon.
En outre, selon cette décision certains
Etats membres (France, Portugal,
Irlande, Autriche, Allemagne, Italie et
Espagne), devront financer la
recherche sur les cellules souches
embryonnaires disponibles, par leur
contribution au budget communautaire
alors qu’ils interdisent ces recherches
sur leur territoire…
lettre mensuelle gratuite, publiée par la Fondation Jérôme Lejeune.

Gènéthique - n°34 octobre 2002
Directeur de la publication et Rédacteur en chef : Jean-Marie Le Méné
Contact : Aude Dugast - 31 rue Galande 75005 Paris - Tél/Fax : 01.55.42.55.14
adugast@fondationlejeune.org

Gènéthique - n°34 octobre 2002
1
/
4
100%