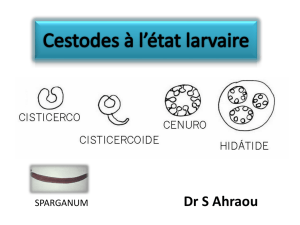
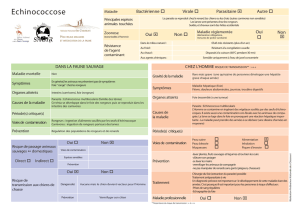
Échinococcose alvéolaire

Échinococcose alvéolaire
L’échinococcose alvéolaire est une anthropozoonose
due àl’infection par la forme larvaire d’un cestode :
Echinococcus multilocularis.
Agent causal
Ce ver adulte est un petit tænia de 1,2 à4mm, très
semblable morphologiquement àEchinococcus granu-
losus.Ledéveloppement de ce cestode nécessite le pas-
sage chez deux hôtes successifs.
Une seule et même espèce est responsable de la maladie.
Épidémiologie
Cette parasitose sévit dans les régions froides de l’hémi-
sphère nord. Des foyers ont été identifiés en Alaska, au
Japon, en Chine, dans la plupart de la Russie et de
l’Asie centrale. En Europe, les principales zones sont
situées au centre :Allemagne, Suisse, Autriche. En
France, certaines régions sont plus particulièrement
touchées :Alsace, Lorraine, Alpes et Auvergne. L’inci-
dence annuelle dans les pays d’Europe atteint au maxi-
mum 0,74 pour 100 000 habitants. Un élargissement
de la zone d’endémie aété observé en France avec le
signalement de cas dans le Morvan, les Ardennes,
l’Aveyron et la Bourgogne. Elle reste majoritairement
une maladie du monde rural.
L’homme peut s’infester indirectement en ingérant des
œufs, par consommation de baies sauvages ou de crudi-
tés souillées par les déjections de renard, ou directe-
ment, par contact avec le pelage de l’animal souillé ou
encore en manipulant des fourrures ou en dépeçant des
renards.
La transmission au nouveau-né n’est pas connue.
Cycle évolutif
L’hôte définitif, généralement un Canidae (le renard et
le chien) ou un Felidae,héberge le cestode adulte dans
son intestin grêle et élimine les œufs dans ses excré-
ments. Les hôtes intermédiaires, habituellement des
rongeurs (campagnols), se contaminent en ingérant les
œufs et hébergent la forme larvaire du parasite dans
le foie. Le renard se contamine en ingérant les viscères
parasités de l’hôte intermédiaire.
L’homme est un hôte intermédiaire accidentel et une
impasse parasitaire :ilnejoue aucun rôle dans la pro-
pagation du parasite et dans la contamination. L’hyda-
tide chez l’homme est principalement localisée dans le
foie. L’homme est assez peu réceptif. La larve d’Echino-
Guide des analyses spécialisées
coccus multilocularis,comme tout cestode, se déve-
loppe selon un mode vésiculeux. Elle est composée de
trois éléments :une enveloppe externe double (cuticule
et membrane proligère), un contenu liquidien et des élé-
ments germinatifs ;contrairement àEchinococcus
granulosus,lalarve n’a pas une cuticule continue, ce
qui favorise un bourgeonnement périphérique et un
envahissement de proche en proche de l’organe para-
sité. L’ensemble de la larve est donc très ramifié, avec
un aspect polyvésiculaire. Le liquide hydatique est sou-
vent en contact avec le parenchyme hépatique, qu’il
nécrose. La réaction de défense au niveau du foie pro-
voque une fibrose disséminée enserrant de façon dis-
continue les multiples vésicules.
L’échinococcose alvéolaire est une maladie caractérisée
par une évolution lente (5 à10ans, voire 15 ans après
la contamination).
Clinique
Durant cette période d’invasion, les malades souffrent
tout au plus de vagues douleurs épigastriques. Parasi-
tose avant tout hépatique, d’allure pseudo-tumorale, le
foie est gros, douloureux et irrégulier. L’ictère cholesta-
tique est souvent le premier signe d’appel et s’accom-
pagne de prurit. Une fièvre modérée, des douleurs
abdominales et une altération de l’état général peuvent
s’observer. Les complications majeures sont :méta-
stases parasitaires des tissus voisins (poumons ou encé-
phale), rupture accidentelle du kyste, hypertension
portale avec risque hémorragique.
Diagnostic biologique
Le diagnostic est maintenant plus aisé ;ilassocie les
aspects en imagerie médicale (échographie, tomo-
densitométrie), qui révèlent des kystes très évocateurs,
et les données biologiques.
—Signes non spécifiques
Ils montrent une élévation des transaminases, des
gamma glutamyl transférases, des phosphatases alca-
lines et éventuellement de la bilirubine totale et conju-
guée de manière inconstante. Dans 50 %des cas, il
existe une hypergammaglobulinémie et une augmenta-
tion des IgE. L’hyperéosinophilie est très inconstante.
—Sérologie
Le diagnostic sérologique devra mettre en évidence les
anticorps spécifiques et permettre un diagnostic diffé-
rentiel entre échinococcose alvéolaire et échinococcose
kystique.

L’antigène d’ Echinococcus granulosus (liquide de kyste
hydatique) alongtemps été utilisé pour effectuer le séro-
diagnostic de l’échinococcose alvéolaire, en raison de
nombreuses communautés antigéniques entre ces deux
parasites. La tendance actuelle s’oriente vers l’utilisa-
tion de l’antigène homologue d’ Echinococcus multi-
locularis,qui permet un diagnostic plus sensible et plus
spécifique. De nombreuses techniques sont proposées.
Chacune étudie des types d’anticorps différents. Il est
donc conseillé d’associer deux méthodes de dépistage
différentes et de confirmer les réactions positives ou dis-
cordantes.
•Techniques de dépistage
–L’immunofluorescence utilise des antigènes figurés :
coupes de foie de gerbille infectée par Echino-
coccus multilocularis ou coupes de scolex d’
Echinococcus granulosus obtenus àpartir de sable
hydatique provenant de kyste de chameau :leseuil
de positivité est le 1/40.
–L’hémagglutination passive utilise des hématies
sensibilisées avec des antigènes solubles préparés à
partir de liquides hydatiques d’Echinococcus
granulosus.Elle n’est positive que dans 75 %des
cas. Des réactions croisées sont observées avec les
helminthiases provoquées par les vers plats (échino-
coccose kystique, distomatose, bilharzioses). Un
titre égal ou supérieur à1/320 est significatif.
–L’électrosynérèse s’effectue sur membrane d’acétate
de cellulose, en faisant migrer dans un champ élec-
trique le sérum du patient et l’extrait soluble d’un
antigène provenant d’un lyophilisat de sable hyda-
tique de chameau. Cette technique ne permet pas la
différenciation des deux espèces. Elles ne se posi-
tivent que dans 30 %des échinococcoses
alvéolaires.
–Des progrès considérables ont été obtenus avec
l’Elisa utilisant différents types d’antigènes :extrait
de liquide hydatique d’Echinococcus granulosus
ou, mieux, antigène fractionné d’Echinococcus
multilocularis :l’antigène Em2, qui apermis la
réalisation d’un test spécifique et sensible. Cet
antigène Em2 permet de diagnostiquer 95 à100 %
des échinococcoses alvéolaires.
•Techniques de confirmation
–L’immunoélectrophorèse permet la mise en évi-
dence d’anticorps dirigés contre la fraction anti-
génique 5spécifique du genre Echinococcus,
confirmant le diagnostic. Mais cet arc 5seretrouve
seulement dans 30 %des patients porteurs d’Echi-
nococcus multilocularis.Deplus, cette technique
est longue, de lecture délicate et sa sensibilité est
inférieure àcelle de l’immunoempreinte.
–Latechnique de l’immunoempreinte aété appliquée
àl’échinococcose alvéolaire. Les protéines des
larves d’Echinococcus multilocularis sont séparées
par électrophorèse sur gel de polyacrylamide et
transférées sur membrane de nitrocellulose. Les
sérums sont incubés avec les bandes de nitro-
cellulose et les anticorps spécifiques révélés par un
conjugué anti-IgG humaines lié àlaphosphatase
alcaline. Les bandes spécifiques sont :7,16, 18,
26–28 kDa. La présence des bandes 7kDa et/ou
26–28 kDa est spécifique du genre Echinococcus ;
des profils spécifiques sont observés avec Echino-
coccus granulosus et Echinococcus multilocularis.
Cette technique présente une sensibilité de 97 %
pour le genre Echinococcus, de 98 %pour Echino-
coccus granulosus et de 96 %pour Echinococ-
cus multilocularis.Son pouvoir discriminatif entre
les deux espèces est de 70 %.
Traitement
Le pronostic s’est amélioré grâce àundiagnostic plus
précoce. Le traitement de choix reste chirurgical. L’exé-
rèse des formes larvaires par hépatectomie partielle
n’est possible que lorsque le parasite n’occupe qu’une
partie limitée du foie. La greffe de foie est le seul geste
possible si le stade est trop avancé, mais elle reste
exceptionnelle.
Les traitements semblent stabiliser les lésions. L’alben-
dazole (Eskazole
®
)est prescrit lorsque le patient est
inopérable ou en cas de résections partielles, mais aussi
après un traitement radical.
Ce médicament ne doit pas être administré pendant la
grossesse, car il est potentiellement tératogène et
embryotoxique.
La prévention individuelle consiste àéviter les contacts
avec des hôtes définitifs :sauvages (renards, loups) ou
domestiques (chien, chat). Le traitement des animaux
domestiques par praziquantel peut être efficace.
☞Échinococcose kystique
(Bronstein JA,Klotz F.
Cestodoseslarvaires.
EMC –Maladiesinfectieuses2005 ;8-511-A-12, 18 p.
Piarroux M, Bresson-Hadni S, Capek I, KnappJ,Watelet J, Dumortier J,
AbergelA,Minello A, GérardA,Beytout J, Piarroux R, Kantelip B, Dela-
brousseE,Vaillant V, Vuitton DA.
Surveillancedel’échinococcose alvéolaireenFrance:bilandecinq
annéesd’enregistrement, 2001-2005.
BEH –Bulletin épidémiologique hebdomadaire 2006 ;N
o
27-28 :
206-207.
1
/
2
100%