vieillissement cardiaque - Longue Vie et Autonomie

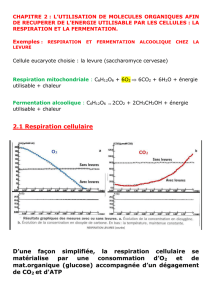
VIEILLISSEMENT
CARDIAQUE
MATHIAS MERICSKAY, CHARGÉ DE RECHERCHE INSERM
UNITE ADAPTATION BIOLOGIQUE ET VIEILLISSEMENT
UPMC UNIVERSITE PARIS 6 - CNRS UMR 8256 - INSERM U1164
7 QUAI SAINT BERNARD 75005 PARIS

VIEILLISSEMENT
PATRIMOINE ENVIRONNEMENT
GÉNÉTIQUE STYLE DE VIE
ERREURS/DÉGRADATIONS
CAPACITÉS D’ADAPTATION RÉDUITES
PATHOLOGIES
MORT

VIEILLISSEMENT
ERREURS/DÉGRADATIONS
• La théorie des radicaux libres (Harman 1956) : atteinte des
macromolécules (protéines, ADN, ARN)
• La théorie de la sénescence réplicative (limite de Hayflick,
1961): perte des télomères au cours de la division mitotique.
• La théorie mitochondriale postule que la dysfonction
mitochondriale est primaire : ppales sources d’espèces
réactives de l’oxygène, et principales « victimes
• La théorie de l’inflammation à bas bruit associée au
vieillissement (découle en partie des 3 théories précédentes)

Lakatta E G , and Levy D Circulation. 2003;107:346-354
Copyright © American Heart Association, Inc. All rights reserved.
VIEILLISSEMENT
ET PATHOLOGIES CARDIAQUES
left ventricular hypertrophy
Atrial Fibrillation

VIEILLISSEMENT CARDIAQUE PATHOLOGIQUE:
LA QUADRATURE DU CERCLE
VIEILLISSEMENT
INTRINSÈQUE
COMORBIDITÉS
(HTA, mal. coronariennes)
INSUFFISANCE
CARDIAQUE
FIBRILLATION
ATRIALE
MORT
(AVC, ACR, FV)
Atrésie/Hypertrophie, Fibrose
Désensibilisation adrénergique
Dysfonction mitochondriale
Troubles de la conduction/rythme
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
1
/
29
100%