L`adipocyte est-il un macrophage

Mini-revue
L’adipocyte est-il un macrophage ?
Béatrice Cousin, Guillaume Charrière, Louis Casteilla, Luc Pénicaud
UMR 5018 CNRS UPS, IFR31, CHU Rangueil, 1, avenue J. Poulhès, 31403 Toulouse cedex, France
Les adipocytes se différencient à partir de préadipocytes qui
sont présents au sein du tissu adipeux. Une littérature abon-
dante montre que les cellules du lignage adipocytaire ont des
caractéristiques communes avec celles du lignage macrophagi-
que. Ces caractéristiques communes incluent à la fois une
communauté moléculaire qui révèle une proximité phénotypi-
que importante, mais aussi et surtout, une communauté de
fonctions telles que la sécrétion d’un nombre non négligeable
de cytokines, une activité de phagocytose ou encore un méta-
bolisme lipidique. Comme les macrophages, les préadipocytes
sont capables de phagocyter des corps apoptotiques, et des
micro-organismes qui seront par la suite tués grâce à des
mécanismes en partie oxygène dépendants. L’activité
macrophage-like
des préadipocytes est néanmoins moins impor-
tante que celle des phagocytes professionnels, mais elle est augmen-
tée dans certaines conditions physiopathologiques associées à un
état inflammatoire. Par ailleurs, les préadipocytes ont la capacité de
se convertir en macrophages dans certaines conditions, ils vont alors
exprimer des marqueurs spécifiques du macrophage.
L’ensemble de ces données suggère que le tissu adipeux pour-
rait participer au remodelage tissulaire dans certaines condi-
tions et jouer un rôle actif dans la réponse immunitaire, notam-
ment au cours de la réaction inflammatoire.
Mots clés : adypocyte, macrophage, plasticité, immunité, inflammation
L’analyse de la bibliographie, notamment celle des dernières
années, permet de mettre en évidence un grand nombre de
points communs entre les cellules des lignages adipocytaire et
macrophagique. Ces ressemblances sont à la fois phénotypi-
ques et fonctionnelles, et posent un certain nombre de questions sur la significa-
tion biologique d’une telle proximité.
La première difficulté lorsqu’on pose une telle question est de définir les types
cellulaires auxquels on s’intéresse. Le lignage adipocytaire comporte au moins
2 types cellulaires identifiés, que sont l’adipocyte et son précurseur, le préadipo-
cyte. L’adipocyte a été classiquement décrit comme une cellule capable de jouer
le rôle de réservoir énergétique c’est-à-dire d’accumuler des lipides et de les
mobiliser en fonction des besoins de l’organisme. Les préadipocytes sont des
cellules d’aspect fibroblastique, définis à l’origine uniquement sur leur capacité
Correspondance et tirés à part :
Sang Thrombose Vaisseaux 2004 ;
16, n° 6 : 295-301
STV, n° 6, vol. 16, juin 2004 295
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

à se différencier en adipocytes. De nombreux travaux de
recherche ont été menés afin d’identifier des marqueurs
moléculaires spécifiques de ce type cellulaire, mais à
l’heure actuelle il n’en existe aucun. Les macrophages
représentent un système de défense important contre les
invasions de l’organisme par une grande variété de micro-
organismes. Ils sont définis par l’expression de marqueurs
antigéniques spécifiques mais aussi par leurs fonctions
particulières et notamment leur capacité de phagocytose,
largement impliquée dans tous les mécanismes de défense,
et notamment les réactions inflammatoires.
A priori, rien ne pouvait laisser penser qu’il existe une
proximité entre ces deux lignages et pourtant....
Phénotype commun
Nous ne chercherons pas ici à définir une liste exhaustive de
marqueurs de surface ou intracellulaire communs aux deux
types cellulaires, mais plutôt à montrer la proximité phéno-
typique à travers un certain nombre d’exemples (tableau 1).
Marqueurs cellulaires
Il existe un nombre non négligeable de protéines de surface
classiquement décrites comme spécifiques du macrophage,
et qui ont été récemment retrouvées à la surface des cellules
du lignage adipocytaire. Parmi ces protéines, on peut citer
plusieurs récepteurs impliqués dans la phagocytose tels que
le CD36 décrit à l’origine comme faisant partie de la famille
des récepteurs scavengers et à ce titre impliqué dans les
processus de phagocytose, mais exprimé aussi dans les
adipocytes où il joue le rôle de transporteur d’acides gras
[1]. D’autres récepteurs de la famille TLR (toll like recep-
tor) ont été identifiés sur les deux types cellulaires. Ces
récepteurs seraient impliqués dans la réponse immunitaire
innée et peuvent lier une grande variété de substrats [2]. Les
récepteurs TLR2 et TLR4 peuvent lier le LPS et participer
ainsi à la détection des bactéries gram-négatives par les
macrophages. Une étude récente montre que les préadipo-
cytes et les adipocytes expriment les récepteurs TLR 2 et 4,
et présentent ainsi une grande sensibilité au LPS [3].
D’autres marqueurs tels que Moma-2 utilisé depuis long-
temps pour caractériser les cellules du lignage myéloïde a
été mis en évidence sur les préadipocytes [4].
Les macrophages activés sont connus pour leur production
importante d’espèces actives de l’oxygène au cours du
burst oxydatif. Cette production de radicaux oxygénés est
assurée en partie par un complexe enzymatique, le NADPH
oxydase membranaire. Les adipocytes possèdent eux aussi
une NADPH oxydase membranaire dont l’activité est dé-
pendante du magnésium comme c’est le cas pour les phago-
cytes professionnels et qui permet, via une stimulation par
l’insuline, la production d’H
2
O
2
. Toutefois, le rôle de ce
complexe enzymatique dans une situation inflammatoire
n’a pas été étudié [5, 6].
Tableau 1. Communauté moléculaire et fonctionnelle des lignages adipocytaire et macrophagique.
Les niveaux d'expression ou d'activité sont quantifiés de manière approximative
Macrophages Préadipocytes Adipocytes
Métabolisme énergétique
PPARc++ +++ +/-
aP2 + +/- +++
CD36/FAT +++ +/- +++
Récepteur de l’insuline + + ++
Récepteurs adrénergiques + ++ ++
Récepteurs aux glucocorticoïdes + + +
Lipoprotéine lipase + + ++
Lipase hormono-sensible + - +
Fonctions immunitaires
Moma-2 ++ ++ ++
Cytokines inflammatoires +++ +/- ++
Chémokines +++ ND ++
Protéines du complément +++ ND ++
Activité NADPH-oxydase +++ ND ++
Activité de phagocytose +++ + -
Activité microbicide +++ + -
Prostaglandines + + +
Récepteur au LPS (TLR) +++ ++ ++
STV, n° 6, vol. 16, juin 2004
296
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

À l’inverse, des marqueurs que l’on pensait spécifiques du
lignage adipocytaire sont exprimés dans les macrophages.
C’est notamment le cas pour aP2, transporteur d’acide gras
dans l’adipocyte et marqueur du stade différencié de cette
cellule. Cette protéine est aussi exprimée dans le macro-
phage, de même qu’un grand nombre d’enzymes impli-
quées dans le métabolisme des triglycérides.
Facteurs de transcription
Parmi les protéines communes aux deux lignages, il faut
citer le facteur de transcription PPARc. Celui-ci a été décrit
pour la première fois dans l’adipocyte, dans lequel il joue
un rôle clé dans la régulation de la différenciation. PPARca
longtemps été considéré comme marqueur spécifique des
cellules du lignage adipocytaire, jusqu’à ce que son expres-
sion soit mise en évidence dans les macrophages [7]. Si ce
facteur de transcription ne semble pas indispensable à la
différenciation des macrophages, il joue néanmoins un rôle
important d’activation de ces cellules et de régulation de
leur métabolisme lipidique en favorisant la formation de
macrophages spumeux [8, 9].
Une autre famille de facteurs de transcription, la famille des
C/EBP, est largement impliquée dans le contrôle de la
différenciation des cellules adipocytaires et myéloïdes.
Dans les préadipocytes, l’expression de C/EBPbest transi-
toire et diminue après la phase d’expansion clonale, alors
qu’elle est augmentée au cours de la différenciation des
macrophages [10]. Ces facteurs de transcription, et notam-
ment C/EBPa, sont impliqués dans le contrôle du métabo-
lisme ainsi que dans la réponse inflammatoire via la régula-
tion de l’expression de gènes clés de ces deux grandes
fonctions [10].
Fonctions Communes
Sécrétion
Les cellules des lignages adipocytaires et macrophagique
possèdent des capacités sécrétoires importantes (figure 1).
Par ses propriétés sécrétoires, le tissu adipeux blanc parti-
cipe activement à l’homéostasie énergétique de l’orga-
nisme comme cela a été abondamment démontré, mais il est
aussi impliqué dans d’autres fonctions comme les fonctions
cardiovasculaires ou l’immunité innée. En effet, le tissu
adipeux est une source importante de protéines de la voie
alterne du complément, de cytokines inflammatoires, de
chémokines et de prostaglandines. Il faut souligner que le
tissu adipeux représente près de 15 % du poids corporel
Figure 1.Sécrétions communes aux cellules des lignages adipocytaire et macrophagique, et leur implication dans plusieurs
fonctions physiologiques.
STV, n° 6, vol. 16, juin 2004 297
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

chez un individu sain. Il est de ce fait, une source impor-
tante voire principale de ces différents facteurs pour l’orga-
nisme.
Parmi les protéines de la voie alterne du complément, les
facteurs B, C3, et D (ou adipsine) ainsi que l’ASP (acyla-
tion stimulating protein) sont sécrétés par le tissu adipeux
[11, 12]. L’adipsine a été le premier facteur de cette voie à
avoir été mise en évidence dans les adipocytes. Plus récem-
ment, un facteur impliqué dans la voie classique d’activa-
tion du complément a été mis en évidence dans le tissu
adipeux. Ce facteur est similaire au facteur C1q, et a été
appelé Acrp30 ou adiponectine [13]. La sécrétion de nom-
breuses protéines du complément par les macrophages a été
largement décrite et participe à la réponse humorale de
l’immunité innée.
Les cellules du lignage adipocytaire secrètent aussi un
certain nombre de cytokines inflammatoires, parmi lesquel-
les on trouve, outre le TNFaqui a été largement étudié,
l’interleukine 6, et l’interleukine 1b. Ces cytokines inflam-
matoires sont également sécrétées par les macrophages et
sont de puissants activateurs des fonctions immunitaires
des leucocytes [14]. D’autres chémokines, telles que le
MIF, le M-CSF, le MIP1aet le MCP1, connues pour être
impliquées dans la réaction inflammatoire et réguler les
fonctions leucocytaires sont également sécrétées par le
tissu adipeux [15] et les cellules macrophagiques. Grâce à
ces chémokines, les macrophages stimulent le recrutement
des cellules inflammatoires, et le renouvellement des cellu-
les du lignage myéloïde. Enfin, d’autres produits de nature
non protéique, comme les prostaglandines PGE2 et PGD2
ont été depuis longtemps décrits dans le tissu adipeux et
peuvent moduler les réponses immunitaires en jouant sur
l’activité des leucocytes [16]. La prostaglandine E2 est
aussi sécrétée par les macrophages, et grâce à son effet
anti-inflammatoire, elle participe à la résolution de la réac-
tion inflammatoire.
Si le rôle de ces différents facteurs sécrétés par les macro-
phages a été largement étudié et est donc bien défini, on ne
peut qu’émettre des hypothèses quant à l’action des fac-
teurs sécrétés par le tissu adipeux. Il semblerait logique que
l’ensemble de ces facteurs ait le même rôle quel que soit le
type cellulaire qui le sécrète, mais cela reste à confirmer.
Métabolisme lipidique
Le tissu adipeux semble donc impliqué par les facteurs
décrits ci-dessus dans la réponse inflammatoire au même
titre que les macrophages. D’autres parallèles peuvent être
faits entre les cellules de ces deux lignages puisqu’elles
jouent toutes deux un rôle important dans le métabolisme
lipidique. Celui-ci a été mis en évidence dans les macropha-
ges par l’étude de l’implication de ces cellules lorsqu’elles
se gorgent de lipides et se transforment en cellules dites
spumeuses au cours de la pathologie de l’athérosclérose.
Les macrophages tout comme les adipocytes expriment en
effet des récepteurs pouvant lier les lipoprotéines de type
LDL, et notamment les LDL oxydées via CD36 [17]. Ils
sont également capables de capter le cholésterol provenant
des LDL grâce à l’expression et à la sécrétion de la lipopro-
téine lipase (LPL). Le métabolisme lipidique des macro-
phages ne se restreint pas au métabolisme du cholésterol.
En effet, comme les adipocytes, il semble que les macro-
phages expriment une isoforme de la lipase hormono-
sensible (LHS) [18] mais également d’autres enzymes im-
pliquées dans les voies de lipogenèse et lipolyse.
Phagocytose, activité microbicide
La phagocytose est le processus par lequel une cellule
internalise des particules de diamètre supérieur à 1 µm. On
distingue habituellement les phagocytes professionnels
(macrophages, neutrophiles et cellules dendritiques) des
phagocytes non professionnels (cellules épithéliales et fi-
broblastes) [19]. Nous avons montré que les préadipocytes
en culture présentent une activité de phagocytose impor-
tante qui décroît à l’arrêt de la prolifération. Cette capacité
de phagocytose a été retrouvée dans les préadipocytes
murins et humains qu’ils soient en culture primaire ou
qu’ils proviennent de lignées, et semble spécifique des
préadipocytes puisque les fibroblastes de peau ou la lignée
myoblastique C2C12 ne présentent pas les mêmes caracté-
ristiques. Cette activité de phagocytose est présente quel-
que soit le substrat (zymosan ou levure) et est suivie d’une
activité microbicide qui conduit à la destruction des micro-
organismes ingérés par des mécanismes en partie au moins
oxydatifs. De plus, les préadipocytes humains présentent
une activité de phagocytose de corps apoptotiques. L’en-
semble de ces résultats suggère que le tissu adipeux pour-
rait être comme les macrophages impliqué dans un certain
nombre de mécanismes de défense, ainsi que dans des
processus de remodelage [4, 20].
Lignage
La multiplicité de propriétés communes entre préadipocy-
tes et macrophages nous a conduits à émettre l’hypothèse
que ces deux types cellulaires provenaient probablement
d’un même lignage. Afin de tester cette hypothèse, nous
avons choisi une approche de comparaison génique à
grande échelle, grâce à l’utilisation de micro-arrays. Cette
technique très puissante permet de comparer l’expression
de quelques milliers de gènes dans deux populations dis-
tinctes. L’analyse informatique de ces données nous a
STV, n° 6, vol. 16, juin 2004
298
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

permis de définir la parenté qui existe entre les populations
macrophagiques et adipocytaires en séparant les cellules
issues de lignées, de celles issues de culture primaire. Que
ce soit au sein des lignées ou des cultures primaires, les
deux profils qui sont les plus proches sont ceux des préadi-
pocytes et des macrophages, ce qui renforce l’hypothèse
d’un lignage commun [21].
Nous avons ensuite cherché à déterminer in vivo s’il pou-
vait exister une transformation d’un type cellulaire en
l’autre. Pour cela, des préadipocytes, préalablement mar-
qués au DAPI, ont été injectés dans la cavité péritonéale de
souris Nude. Six heures après leur injection, la grande
majorité des préadipocytes possède une activité de phago-
cytose et surtout exprime les marqueurs spécifiques des
macrophages Mac-1 et F4/80. Cette « transdifférenciation »
est stable puisque les mêmes observations ont été faites une
semaine après l’injection. Outre les marqueurs spécifiques
de macrophages que sont Mac-1 et F4/80, les préadipocytes
acquièrent aussi l’expression des molécules de costimula-
tion que sont CD80 et CD86 [21].
Ce travail montre qu’il existe une proximité phénotypique
importante entre préadipocytes et macrophages, les préadi-
pocytes étant même capables de se transformer en macro-
phages dans certaines conditions.
Questions en suspens
Mécanisme cellulaire ?
L’ensemble de ces données montre que plus qu’une proxi-
mité entre ces deux types cellulaires, il existe une véritable
capacité de conversion du préadipocyte en macrophage.
Ces résultats rejoignent le champ d’étude très discuté ac-
tuellement qu’est la plasticité cellulaire. Plusieurs hypothè-
ses permettent d’expliquer cette conversion, mais les études
que nous avons faites permettent d’affirmer que la conver-
sion du préadipocyte en macrophage résulte d’une réelle
transdifférenciation et non d’une fusion ou de la phagocy-
tose par le macrophage du préadipocyte. Quoiqu’il en soit,
le mécanisme cellulaire n’a pas été décrit.
Rôle en physiologie
Les préadipocytes possèdent donc des fonctions macropha-
giques aussi bien chez le rongeur que chez l’homme, et ces
fonctions varient selon les conditions physiologiques ou
pathologiques. À la lumière de ces données, on peut émet-
tre l’hypothèse que les préadipocytes participent à la dé-
fense immunitaire de l’organisme. Cette hypothèse est ren-
forcée par la capacité des préadipocytes à se convertir en
macrophages et à acquérir ainsi de nouvelles propriétés de
macrophages dont ils étaient exempts avant leur conver-
sion. Les préadipocytes en exprimant notamment les molé-
cules de co-stimulation CD80 et CD86 pourraient moduler
l’activité des cellules immunitaires, mais cela reste cepen-
dant à démontrer. De plus par ses capacités sécrétoires, le
tissu adipeux pourrait avoir une action humorale dans la
réponse immunitaire. Enfin, grâce à leur capacité de phago-
cyter des corps apoptotiques dans certaines conditions, les
cellules du tissu adipeux pourraient participer activement
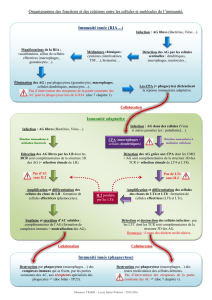
aux processus de remodelage tissulaire (figure 2).
Ces propriétés du tissu adipeux semblent avoir leur impor-
tance dans les réactions inflammatoires et notamment cel-
les décrites lors de modifications de la masse adipeuse.
Ainsi, l’obésité est en effet depuis quelques années associée
à un phénomène inflammatoire. Nous avons mis en évi-
dence que l’activité macrophage-like des préadipocytes
peut varier en fonction des conditions physiopathologi-
ques. En effet, si l’on considère le potentiel cytotoxique des
cellules (c’est-à-dire leur capacité à ingérer et à tuer les
particules ingérées), celui-ci augmente au cours d’une in-
flammation dans les macrophages et dans les préadipocy-
tes. Chez des animaux obèses, le potentiel cytotoxique des
macrophages diminue alors que celui des préadipocytes
augmente ce qui suggère que les préadipocytes pourraient
dans certains cas prendre le relais des macrophages pour
assurer un rôle de défense de l’organisme [22]. Cela aurait
d’autant plus d’importance que, outre le déficit d’activation
des phagocytes professionnels, les individus obèses présen-
tent un déficit général du nombre de monocytes qui matu-
rent en macrophages [23]. Il a été montré très récemment
que l’obésité chez la souris est associée à une augmentation
des signaux inflammatoires, et une augmentation du nom-
bre de macrophages dans les dépôts adipeux [24, 25]. Ces
macrophages seraient pour la plupart d’origine médullaire,
mais il n’est pas exclu qu’un certain nombre d’entre eux
proviennent d’une conversion de préadipocytes. Enfin, il
est possible que la transformation inverse puisse se pro-
duire et que, une fois le problème inflammatoire résolu, les
macrophages issus de la transformation des préadipocytes
reviennent à un phénotype adipocytaire. En effet, il existe
de grandes similitudes entre les adipocytes et les macropha-
ges spumeux observés au sein des plaques athéromateuses.
Le problème immunitaire deviendrait alors une cause pos-
sible de l’amplification du syndrome d’obésité.
Il faut souligner une fois encore que même si l’activité
macrophage-like des préadipocytes reste inférieure à celle
des phagocytes professionnels, la masse que représente le
tissu adipeux dans l’organisme et donc la proportion de
cellules préadipocytaires peuvent compenser le déficit d’ac-
tivité intrinsèque.
Le tissu adipeux est un tissu complexe dont les cellules
présentent une certaine plasticité phénotypique et fonction-
STV, n° 6, vol. 16, juin 2004 299
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
 7
7
1
/
7
100%